从能量的变化和反应的快慢等角度研究化学反应具有重要意义。
(1)已知一定条件下,反应 为放热应:
为放热应:
①下图能正确表示该反应中能量变化的是__________ ;

②根据下表数据,计算生成 时该反应放出的热量为
时该反应放出的热量为__________  :
:
(2)某兴趣小组为研究原电池原理,设计如图装置。
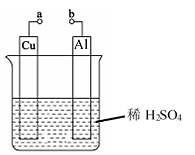
① 和
和 用导线连接,
用导线连接, 极为原电池
极为原电池________ (填“正”或“负”)极,电极反应式是________ ; 极发生
极发生________ (填“氧化”或“还原”)反应,其电极反应式为________ ,溶液中 移向
移向________ (填“ ”或“
”或“ ”极)。当负极金属溶解
”极)。当负极金属溶解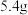 时,通过导线的电子数为
时,通过导线的电子数为________ 。
②不将 连接,请问如何加快
连接,请问如何加快 与稀硫酸的反映速率?
与稀硫酸的反映速率?____________________ 。
(1)已知一定条件下,反应
 为放热应:
为放热应:①下图能正确表示该反应中能量变化的是

②根据下表数据,计算生成
 时该反应放出的热量为
时该反应放出的热量为 :
:| 化学键 |  |  |  |  |  |
断开 键所吸收的能量 键所吸收的能量 | 415 | 498 | 343 | 798 | 465 |

①
 和
和 用导线连接,
用导线连接, 极为原电池
极为原电池 极发生
极发生 移向
移向 ”或“
”或“ ”极)。当负极金属溶解
”极)。当负极金属溶解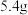 时,通过导线的电子数为
时,通过导线的电子数为②不将
 连接,请问如何加快
连接,请问如何加快 与稀硫酸的反映速率?
与稀硫酸的反映速率?
18-19高三·浙江·期中 查看更多[1]
(已下线)【新东方】高中化学140
更新时间:2019-11-12 09:00:18
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)在一定条件下N2与H2反应生成NH3,请回答:
①若反应物的总能量为E1,生成物的总能量为E2,且E1>E2,则该反应为___________  填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。
②已知拆开1molH-H键、1molN-H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___________ 。
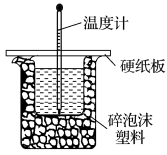
(2)实验室用50mL0.50mol/L盐酸与50mL某浓度的NaOH溶液在如图所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。该装置有两处明显的错误,其中一处是缺少一种玻璃仪器,该仪器的名称为___________ ;实验室提供了0.50mol/L和0.55mol/L两种浓度的NaOH溶液,应选择___________ mol/L的溶液进行实验。
(3)写出下列反应的热化学方程式:
①16gCH4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出890.3kJ热量___________ 。
②0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态的三氧化二硼和液态水,放出649.5kJ热量,其热化学方程式为___________ 。
(1)在一定条件下N2与H2反应生成NH3,请回答:
①若反应物的总能量为E1,生成物的总能量为E2,且E1>E2,则该反应为
 填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。②已知拆开1molH-H键、1molN-H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(2)实验室用50mL0.50mol/L盐酸与50mL某浓度的NaOH溶液在如图所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。该装置有两处明显的错误,其中一处是缺少一种玻璃仪器,该仪器的名称为

(3)写出下列反应的热化学方程式:
①16gCH4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出890.3kJ热量
②0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态的三氧化二硼和液态水,放出649.5kJ热量,其热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)依据事实,写出下列反应的热化学方程式。
①在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为:___________________________________________ 。
②若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量__________________ 。
③已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为:________________________________ 。
(2)氢气是一种清洁能源。用甲烷制取氢气的两步反应的能量变化如下图所示:
①甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是____________ 。
②第II步为可逆反应。在800℃时,若CO的起始浓度为2.0 mol/L,水蒸气的起始浓度为3.0 mol/L,达到化学平衡状态后,测得CO2的浓度为1.2 mol/L,则此反应的平衡常数为____ ,CO的平衡转化率为_____ 。
①在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为:
②若适量的N2和O2完全反应,每生成23g NO2需要吸收16.95kJ热量
③已知拆开1mol H-H键,1molN-H键,1molN≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为:
(2)氢气是一种清洁能源。用甲烷制取氢气的两步反应的能量变化如下图所示:

①甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是
②第II步为可逆反应。在800℃时,若CO的起始浓度为2.0 mol/L,水蒸气的起始浓度为3.0 mol/L,达到化学平衡状态后,测得CO2的浓度为1.2 mol/L,则此反应的平衡常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1)已知25℃时: Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-12。取一定量含有I-、Cl-的溶液向其中滴加AgNO3溶液,当AgCl 和AgI同时沉淀时,溶液中 为
为_______ 。
(2)下列粒子:①CS2;②PCl3;③H2S ;④CH2O;⑤H3O+;⑥ ;⑦BF3;⑧SO2。价层电子对的立体构型和粒子的立体构型一致的是
;⑦BF3;⑧SO2。价层电子对的立体构型和粒子的立体构型一致的是_______ ,②③⑥的键角从大到小的顺序是_______ 。
(3)已知拆开1mol H-H键、lmolN≡N 和lmol N-H键分别需要的能量是436kJ、948kJ、391 kJ。则N2、H2合成NH3的热化学方程式为_______ 。
(1)已知25℃时: Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-12。取一定量含有I-、Cl-的溶液向其中滴加AgNO3溶液,当AgCl 和AgI同时沉淀时,溶液中
 为
为(2)下列粒子:①CS2;②PCl3;③H2S ;④CH2O;⑤H3O+;⑥
 ;⑦BF3;⑧SO2。价层电子对的立体构型和粒子的立体构型一致的是
;⑦BF3;⑧SO2。价层电子对的立体构型和粒子的立体构型一致的是(3)已知拆开1mol H-H键、lmolN≡N 和lmol N-H键分别需要的能量是436kJ、948kJ、391 kJ。则N2、H2合成NH3的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】草酸(H2C2O4)是一种易溶于水的二元有机弱酸,常用作还原剂、沉淀剂等,可与酸性KMnO4溶液发生反应,以下为探究外界条件对反应速率的影响。请回答下列问题:
(1)硫酸酸化的高锰酸钾溶液与草酸溶液反应的离子方程式为_______ 。
(2)完成此实验设计,其中:V1=_______ ,V2=_______ 。
(3)对比实验1、2可探究_______ 对反应速率的影响。
| 实验编号 | 所加试剂及用量/mL | 条件 | 溶液颜色褪至无色所需时间/min | |||
| 0.01mol·L-1H2C2O4溶液 | 0.01mol·L-1KMnO4溶液 | 3.0mol·L-1稀H2SO4 | 水 | 温度/℃ | ||
| 1 | 12.0 | 2.0 | 3.0 | 3.0 | 20 | t1 |
| 2 | 6.0 | 2.0 | 3.0 | V1 | 20 | t2 |
| 3 | V2 | 2.0 | 3.0 | 9.0 | 30 | t3 |
(2)完成此实验设计,其中:V1=
(3)对比实验1、2可探究
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】可逆反应2SO2(g)+O2(g)  2SO3(g)是工业上制取H2SO4的重要反应。
2SO3(g)是工业上制取H2SO4的重要反应。
(1)在恒压条件下,该反应分组实验的有关条件如下表:
已知Ⅰ、Ⅱ两组实验过程中,SO3气体的体积分数φ(SO3)随时间t的变化曲线如图所示。
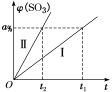
①Ⅱ组与Ⅰ相比不同的条件是___________ ;
②将Ⅰ组实验中温度变为800 ℃,则φ(SO3)达到a%所需时间___________ t1(填“小于”“大于”或“等于”)。
(2)向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时,按反应速率由大到小排列的是___________。
甲:在500 ℃时,10 mol SO2和10 mol O2反应
乙:在500 ℃时,用V2O5作催化剂,10 mol SO2和10 mol O2反应
丙:在450 ℃时,8 mol SO2和5 mol O2反应
丁:在500 ℃时,8 mol SO2和5 mol O2反应
 2SO3(g)是工业上制取H2SO4的重要反应。
2SO3(g)是工业上制取H2SO4的重要反应。(1)在恒压条件下,该反应分组实验的有关条件如下表:
| 反应条件 | 温度 | 容器容积 | 起始n(SO2) | 起始n(O2) | 其他条件 |
| Ⅰ组 | 500 ℃ | 1 L | 1 mol | 2 mol | 无 |
| Ⅱ组 | 500 ℃ | 1 L | 1 mol | 2 mol |

①Ⅱ组与Ⅰ相比不同的条件是
②将Ⅰ组实验中温度变为800 ℃,则φ(SO3)达到a%所需时间
(2)向四个体积相同的密闭容器中分别充入一定量的SO2和O2,开始反应时,按反应速率由大到小排列的是___________。
甲:在500 ℃时,10 mol SO2和10 mol O2反应
乙:在500 ℃时,用V2O5作催化剂,10 mol SO2和10 mol O2反应
丙:在450 ℃时,8 mol SO2和5 mol O2反应
丁:在500 ℃时,8 mol SO2和5 mol O2反应
| A.甲、乙、丙、丁 | B.乙、甲、丙、丁 |
| C.乙、甲、丁、丙 | D.丁、丙、乙、甲 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题:
CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g) 2CO(g)+2H2(g)
2CO(g)+2H2(g)
①已知上述反应中相关的化学键键能数据如下:
分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是___ (填“A”或“B”)。
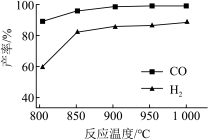
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图所示。此反应优选温度为900℃的原因是___ 。
CO2与CH4经催化重整,制得合成气:CH4(g)+CO2(g)
 2CO(g)+2H2(g)
2CO(g)+2H2(g)①已知上述反应中相关的化学键键能数据如下:
| 化学键 | C—H | C=O | H—H | C O(CO) O(CO) |
| 键能/kJ·mol-1 | 413 | 745 | 436 | 1075 |
分别在VL恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH4和CO2各1mol的混合气体。两容器中反应达平衡后放出或吸收的热量较多的是
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图所示。此反应优选温度为900℃的原因是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.为了探究原电池的工作原理,某研究性学习小组进行了如下实验。
(1)按下图中甲、乙所示装置进行实验,甲中两个烧杯中的溶液为同浓度的稀硫酸。_______ (填字母)。
A.甲中锌片是原电池的负极,乙中铜片是原电池的正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向
D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极_______ (填实验现象),其对应的电极反应式为_______ 。
(2)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______。
Ⅱ.化学反应 的能量变化如图所示。
的能量变化如图所示。_______ (填“能”或“不能”)将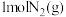 和
和 全部转化为
全部转化为 。
。
(4)该反应属于_______ (填“吸热”或“放热”)反应。
(5)一定量的 和
和 充分反应生成
充分反应生成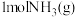 时,释放
时,释放_______  能量。
能量。
(1)按下图中甲、乙所示装置进行实验,甲中两个烧杯中的溶液为同浓度的稀硫酸。

A.甲中锌片是原电池的负极,乙中铜片是原电池的正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向

D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极
(2)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______。
A.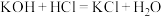 |
B. |
C. |
D.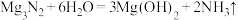 |
Ⅱ.化学反应
 的能量变化如图所示。
的能量变化如图所示。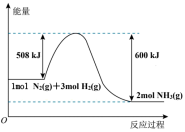
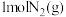 和
和 全部转化为
全部转化为 。
。(4)该反应属于
(5)一定量的
 和
和 充分反应生成
充分反应生成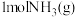 时,释放
时,释放 能量。
能量。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
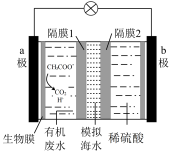
【推荐2】微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废水获得电能,同时可实现海水淡化。现以 溶液模拟海水,采用惰性电极,用如图装置处理有机废水(含
溶液模拟海水,采用惰性电极,用如图装置处理有机废水(含 )。
)。
2.负极的电极反应式为:___________ 。
3.隔膜1为___________ 离子交换膜。
A.正 B.负
4.正、负极产生气体的物质的量之比为___________。
 溶液模拟海水,采用惰性电极,用如图装置处理有机废水(含
溶液模拟海水,采用惰性电极,用如图装置处理有机废水(含 )。
)。
| A.正 | B.负 | C.阳 | D.阴 |
3.隔膜1为
A.正 B.负
4.正、负极产生气体的物质的量之比为___________。
A. | B. | C. | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)某种氢氧燃料电池是用固体金属化物陶瓷作电解质,两极上发生的电极反应分别为:A极:2H2+2O2--4e-=2H2O;B极:O2+4e-=2O2-
则A极是电池的________ 极;电子从该极________ (填“流入”或“流出”)。
(2)有人以化学反应:2Zn+O2+4H+=2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是________ ,发生的电极反应为__________________ 。
(3)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片,可观察到铜片上________ (填“有”或“没有”)气泡产生,再用导线把锌片和铜片连接起来,组成一个原电池,正极的电极反应式为____________________ 。
则A极是电池的
(2)有人以化学反应:2Zn+O2+4H+=2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是
(3)把一块纯净的锌片插入装有稀硫酸的烧杯里,可观察到锌片上有气泡,再平行插入一块铜片,可观察到铜片上
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)以下反应:①木炭与水制备水煤气,②氯酸钾分解,③炸药爆炸,④酸与碱的中和反应,⑤生石灰与水作用制熟石灰,⑥Ba(OH)2•H2O 与 NH4Cl ,⑦浓硫酸溶于水, 属于放热反应__________ .(填序号)
(2)Mg-Al-NaOH 电池中的负极反应:___________ .
(3)FeCl3 溶液常用于腐蚀印刷电路铜板,发生 2FeCl3+Cu=2FeCl2+CuCl2,若将 此反应设计成原电池,则负极所用电极材料为___________ ,当线路中转移 0.2mol 电 子时,则被腐蚀铜的质量为___________ g.
(4)已知拆开 1mol H-H 键、1mol N≡N、1mol N-H 键分别需要吸收的能量为 436kJ、946k J、391k J.则由 N2 和 H2 反应生成 1mol NH3 需要放出___________ 的热量。
(5)用序号回答:①HCl ②NaOH ③Cl2 ④H2O ⑤NH4Cl ⑥P4 ⑦NH3•H2O ⑧Na2O2 ⑨HClO⑩CaO⑪HF⑫MgCl2
属于共价化合物的是___________ ,存在非极性键的是___________ 。
(2)Mg-Al-NaOH 电池中的负极反应:
(3)FeCl3 溶液常用于腐蚀印刷电路铜板,发生 2FeCl3+Cu=2FeCl2+CuCl2,若将 此反应设计成原电池,则负极所用电极材料为
(4)已知拆开 1mol H-H 键、1mol N≡N、1mol N-H 键分别需要吸收的能量为 436kJ、946k J、391k J.则由 N2 和 H2 反应生成 1mol NH3 需要放出
(5)用序号回答:①HCl ②NaOH ③Cl2 ④H2O ⑤NH4Cl ⑥P4 ⑦NH3•H2O ⑧Na2O2 ⑨HClO⑩CaO⑪HF⑫MgCl2
属于共价化合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铬是常见的过渡金属之一,研究铬的性质具有重要意义。回答下列问题:
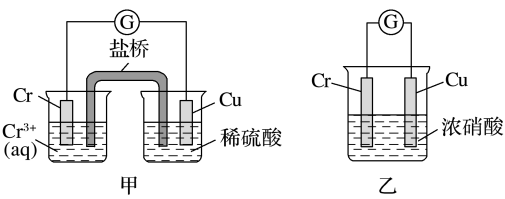
(1)在如图装置中,观察到装置甲中铜电极上产生大量的无色气体,而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由此可知,金属活动性Cr________ Cu(填“>”“<”或“=”);装置乙中正极的电极反应式为________ 。
(2)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(Ⅵ)转化为Cr(Ⅲ)常见的处理方法是电解法。将含Cr2O 的废水加入电解槽内,用石墨和铁做电极,在酸性环境中,加入适量的NaCl进行电解。
的废水加入电解槽内,用石墨和铁做电极,在酸性环境中,加入适量的NaCl进行电解。
①铁做________ 极(填“阳”或“阴”)。
②Cr2O 转化为Cr3+的离子方程式为
转化为Cr3+的离子方程式为________ 。
③阴极上Cr2O 、H+、Fe3+都可能放电。若Cr2O
、H+、Fe3+都可能放电。若Cr2O 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为______ ;若H+放电,则阴极区形成Fe(OH)3和Cr(OH)3沉淀,已知:常温下,Cr3+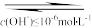 Cr(OH)3
Cr(OH)3 CrO
CrO ,则阴极区溶液pH的范围为
,则阴极区溶液pH的范围为________ 。

(1)在如图装置中,观察到装置甲中铜电极上产生大量的无色气体,而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由此可知,金属活动性Cr
(2)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(Ⅵ)转化为Cr(Ⅲ)常见的处理方法是电解法。将含Cr2O
 的废水加入电解槽内,用石墨和铁做电极,在酸性环境中,加入适量的NaCl进行电解。
的废水加入电解槽内,用石墨和铁做电极,在酸性环境中,加入适量的NaCl进行电解。①铁做
②Cr2O
 转化为Cr3+的离子方程式为
转化为Cr3+的离子方程式为③阴极上Cr2O
 、H+、Fe3+都可能放电。若Cr2O
、H+、Fe3+都可能放电。若Cr2O 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为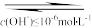 Cr(OH)3
Cr(OH)3 CrO
CrO ,则阴极区溶液pH的范围为
,则阴极区溶液pH的范围为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol/L的H2SO4溶液中,乙同学将电极放入6mol/L的NaOH溶液中,如图所示。

(1)甲中SO 移向
移向______ (填“铝片”或“镁片”),写出甲中正极的电极反应式_____ 。
(2)乙中负极为______ (填“铝片”或“镁片”)写出其电极反应式式:______ 。
(3)铅蓄电池中,正极材料为PbO2,负极材料为Pb,电解液为硫酸,放电时其正极反应式为_____ 。
(4)如图为绿色电源“二甲醚(CH3OCH3)燃料电池”的工作原理示意图,请写出负极的电极反应式:_____ 。


(1)甲中SO
 移向
移向(2)乙中负极为
(3)铅蓄电池中,正极材料为PbO2,负极材料为Pb,电解液为硫酸,放电时其正极反应式为
(4)如图为绿色电源“二甲醚(CH3OCH3)燃料电池”的工作原理示意图,请写出负极的电极反应式:

您最近一年使用:0次



