I.为了探究原电池的工作原理,某研究性学习小组进行了如下实验。
(1)按下图中甲、乙所示装置进行实验,甲中两个烧杯中的溶液为同浓度的稀硫酸。_______ (填字母)。
A.甲中锌片是原电池的负极,乙中铜片是原电池的正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向
D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极_______ (填实验现象),其对应的电极反应式为_______ 。
(2)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______。
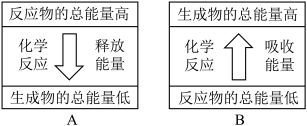
Ⅱ.化学反应 的能量变化如图所示。
的能量变化如图所示。_______ (填“能”或“不能”)将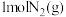 和
和 全部转化为
全部转化为 。
。
(4)该反应属于_______ (填“吸热”或“放热”)反应。
(5)一定量的 和
和 充分反应生成
充分反应生成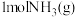 时,释放
时,释放_______  能量。
能量。
(1)按下图中甲、乙所示装置进行实验,甲中两个烧杯中的溶液为同浓度的稀硫酸。

A.甲中锌片是原电池的负极,乙中铜片是原电池的正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向

D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极
(2)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______。
A.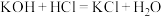 |
B. |
C. |
D.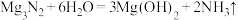 |
Ⅱ.化学反应
 的能量变化如图所示。
的能量变化如图所示。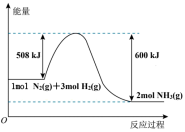
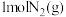 和
和 全部转化为
全部转化为 。
。(4)该反应属于
(5)一定量的
 和
和 充分反应生成
充分反应生成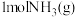 时,释放
时,释放 能量。
能量。
更新时间:2024-05-06 20:08:14
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】I、化学反应中伴随着能量变化。下列属于吸热反应的是___________ (填序号)。
a.燃烧CO b.Ba(OH)2·8H2O晶体和NH4Cl晶体反应 c.铝和稀盐酸反应 d.NaOH溶液和稀盐酸反应 e.液态水变为水蒸气 f.水蒸气冷凝为液态水
II、用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
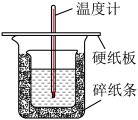
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是_________________ 。
(2)烧杯间填满碎纸条的作用是_____________________________ 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值_______ (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量_______ (填“相等、不相等”),所求中和热_______ (填“相等、不相等”)
III、盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-25 kJ·mol-1
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH=-47 kJ·mol-1
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH=+19 kJ·mol-1
写出FeO(s)与CO反应生成Fe(s)和 的热化学方程式:
的热化学方程式:___________________________ 。
a.燃烧CO b.Ba(OH)2·8H2O晶体和NH4Cl晶体反应 c.铝和稀盐酸反应 d.NaOH溶液和稀盐酸反应 e.液态水变为水蒸气 f.水蒸气冷凝为液态水
II、用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是
(2)烧杯间填满碎纸条的作用是
(3)大烧杯上如不盖硬纸板,求得的中和热数值
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量
III、盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-25 kJ·mol-1
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH=-47 kJ·mol-1
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH=+19 kJ·mol-1
写出FeO(s)与CO反应生成Fe(s)和
 的热化学方程式:
的热化学方程式:
您最近一年使用:0次
【推荐2】化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于放热反应的是_______(填字母)。
(2)向 的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的热效应(对应反应中各物质的化学计量数均为1)分别为
的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的热效应(对应反应中各物质的化学计量数均为1)分别为 、
、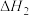 、
、 ,则三者由大到小的顺序为
,则三者由大到小的顺序为_______ 。
(3)在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和反应的反应热。
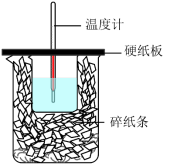
从实验装置上看,图中缺少的一种玻璃仪器是_______ 。若大烧杯上不盖硬纸板,求得的中和反应反应热
_______ (填“偏大”“偏小”或“无影响”)。
(4)获取能量变化的途径
①通过化学键的键能计算。已知:
计算可得:2H2(g)+O2(g)=2H2O(g) ΔH=_______ 。
②通过物质所含能量计算。已知反应中M+N=P+Q中M、N、P、Q所含能量依次可表示为EM、EN、EP、EQ,该反应ΔH=_______ 。
(5)硝酸厂的尾气直接排放将污染空气,日前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为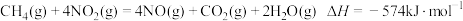

则甲烷直接将 还原为
还原为 的热化学方程式为
的热化学方程式为_______ 。
(1)下列反应中,属于放热反应的是_______(填字母)。
| A.碳与水蒸气反应 | B.铝和氧化铁反应 |
| C.CaCO3受热分解 | D.锌与盐酸反应 |
 的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的热效应(对应反应中各物质的化学计量数均为1)分别为
的NaOH溶液中分别加入下列物质:①浓硫酸;②稀硝酸;③稀醋酸。恰好反应完全时的热效应(对应反应中各物质的化学计量数均为1)分别为 、
、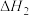 、
、 ,则三者由大到小的顺序为
,则三者由大到小的顺序为(3)在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和反应的反应热。

从实验装置上看,图中缺少的一种玻璃仪器是

(4)获取能量变化的途径
①通过化学键的键能计算。已知:
| 化学键种类 | H-H | O=O | O-H |
| 键能/kJ·mol-1 | 436 | 496 | 463.4 |
②通过物质所含能量计算。已知反应中M+N=P+Q中M、N、P、Q所含能量依次可表示为EM、EN、EP、EQ,该反应ΔH=
(5)硝酸厂的尾气直接排放将污染空气,日前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为
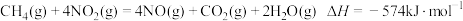

则甲烷直接将
 还原为
还原为 的热化学方程式为
的热化学方程式为
您最近一年使用:0次
【推荐1】根据化学能和热能、电能相关的知识,请回答下列问题:
I.已知31g白磷(P4)变为31g红磷(P)时释放能量。上述变化属于__________ 变化(填“物理”或“化学”);稳定性白磷_________ 红磷(填“>”或“<”);
II.氢气是一种清洁能源,在我国航天工程中也有应用。
(1)已知1g氢气燃烧生成气态水放出热量121kJ,其中断裂1mol H—H键吸收436kJ,断裂1mol O=O键吸收496kJ,那么形成1mol H—O键放出热__ 。
(2)航天技术上使用的氢-氧燃料电池原理可以简单看作下图“氢-氧燃料电池的装置图” 则:
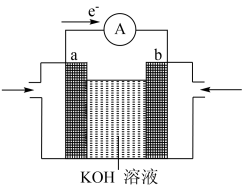
①a极为电池的______ (填“正极”或“负极”);溶液中OH-移向_______ 电极(填“a”或“b”)。
②放电时,b电极附近pH_______ 。(填增大、减小或不变)。
③如把H2改为甲烷,总反应为:CH4+ 2O2 + 2OH- = CO32- + 3H2O,则负极电极反应式为:_________ 。
I.已知31g白磷(P4)变为31g红磷(P)时释放能量。上述变化属于
II.氢气是一种清洁能源,在我国航天工程中也有应用。
(1)已知1g氢气燃烧生成气态水放出热量121kJ,其中断裂1mol H—H键吸收436kJ,断裂1mol O=O键吸收496kJ,那么形成1mol H—O键放出热
(2)航天技术上使用的氢-氧燃料电池原理可以简单看作下图“氢-氧燃料电池的装置图” 则:

①a极为电池的
②放电时,b电极附近pH
③如把H2改为甲烷,总反应为:CH4+ 2O2 + 2OH- = CO32- + 3H2O,则负极电极反应式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知化学反应N2+3H2=2NH3的能量变化如图所示,
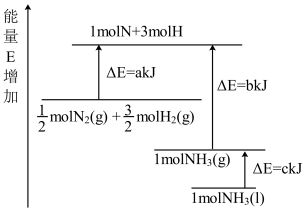
(1)1mol N 和3mol H 生成1mol NH3(g)是_________ 能量的过程(填“吸收”或“释放”)。
(2) N2(g)+
N2(g)+ H2(g)=NH3(g) △H =
H2(g)=NH3(g) △H =_________ ;

(1)1mol N 和3mol H 生成1mol NH3(g)是
(2)
 N2(g)+
N2(g)+ H2(g)=NH3(g) △H =
H2(g)=NH3(g) △H =
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】蕴藏在海底的大量“可燃冰”,其开发利用是当前解决能源危机的重要课题。CH4(g)+2H2O(g) CO2(g)+4H2(g)ΔH3=+akJ·mol-1
CO2(g)+4H2(g)ΔH3=+akJ·mol-1
(1)写出甲烷的结构式___________
(2)C=O的键能为_______________ kJ/mol(用含a、b、c、d的式子表示)
(3)恒温条件下,在体积恒为0.5L的密闭容器中通入一定量甲烷和水蒸气,发生上述反应。测得甲烷物质的量随时间变化如下表所示。0~10min内用H2O的浓度表示该反应的平均速率为υ(H2O)=_____________
(4)恒温恒容情况下,下列叙述能说明此反应达到平衡状态的是_______________ 。
a.混合气体的平均相对分子质量保持不变b.CO2和H2的体积分数比为1﹕4
c.混合气体的密度保持不变d.1molCO2生成的同时有4molH-H键断裂
(5)写出甲烷燃料电池,以KOH溶液为介质时,负极的电极反应式______
 CO2(g)+4H2(g)ΔH3=+akJ·mol-1
CO2(g)+4H2(g)ΔH3=+akJ·mol-1| 化学键 | C—H | H—H | H—O |
| 键能kJ/mol | b | c | d |
(1)写出甲烷的结构式
(2)C=O的键能为
(3)恒温条件下,在体积恒为0.5L的密闭容器中通入一定量甲烷和水蒸气,发生上述反应。测得甲烷物质的量随时间变化如下表所示。0~10min内用H2O的浓度表示该反应的平均速率为υ(H2O)=
| 时间/min | 0 | 10 | 20 | 40 | 50 | 60 |
| n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 | 0.10 |
(4)恒温恒容情况下,下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均相对分子质量保持不变b.CO2和H2的体积分数比为1﹕4
c.混合气体的密度保持不变d.1molCO2生成的同时有4molH-H键断裂
(5)写出甲烷燃料电池,以KOH溶液为介质时,负极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】实验小组探究铝片做电极材料时的原电池反应,设计下表中装置进行实验并记录。
【实验1】
(1)实验1中,电解质溶液为盐酸,镁条做原电池的___________ 极。
【实验2】将实验1中的电解质溶液换为NaOH溶液进行实验2。
(2)该小组同学认为,此时原电池的总反应为 ,据此推测应该出现的实验现象为
,据此推测应该出现的实验现象为___________ 。
实验2实际获得的现象如下:
(3)ⅰ中铝条表面放电的物质是溶解在溶液中的O2,则该电极反应式为___________ 。
(4)ⅱ中“电流计指针逐渐向零刻度恢复”的原因是___________ 。
【实验3和实验4】
为了排除Mg条的干扰,同学们重新设计装置并进行实验3和实验4,获得的实验现象如下:
(5)根据实验3和实验4可获得的正确推论是___________(填字母序号)。
(6)由实验1~实验4可推知,铝片做电极材料时的原电池反应与___________ 等因素有关。
【实验1】
| 装置 | 实验现象 |
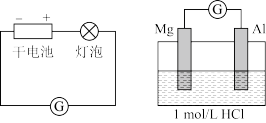 | 左侧装置电流计指针向右偏转,灯泡亮 右侧装置电流计指针向右偏转,镁条、铝条表面产生无色气泡 |
【实验2】将实验1中的电解质溶液换为NaOH溶液进行实验2。
(2)该小组同学认为,此时原电池的总反应为
 ,据此推测应该出现的实验现象为
,据此推测应该出现的实验现象为实验2实际获得的现象如下:
| 装置 | 实验现象 |
 | ⅰ.电流计指针迅速向右偏转,镁条表面无气泡,铝条表面有气泡 ⅱ.电流计指针逐渐向零刻度恢复,经零刻度后继续向左偏转。镁条表面开始时无明显现象,一段时间后有少量气泡逸出,铝条表面持续有气泡逸出 |
(4)ⅱ中“电流计指针逐渐向零刻度恢复”的原因是
【实验3和实验4】
为了排除Mg条的干扰,同学们重新设计装置并进行实验3和实验4,获得的实验现象如下:
| 编号 | 装置 | 实验现象 |
| 实验3 | 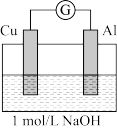 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象;约10分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
| 实验4 | 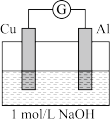 煮沸冷却后的溶液 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象:约3分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
| A.上述两装置中,开始时铜片表面得电子的物质是O2 |
| B.铜片表面开始产生气泡的时间长短与溶液中溶解氧的多少有关 |
| C.铜片表面产生的气泡为H2 |
| D.由“铝条表面气泡略有减少”能推测H+在铜片表面得电子 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据下列要求回答问题。
(1)我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
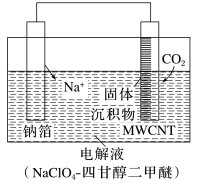
①放电时,正极的电极反应式为___________ 。
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28 g时,转移电子的物质的量为___________ 。
③可选用高氯酸钠-四甘醇二甲醚作电解液的理由是___________ 。
(2)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。
①M极发生的电极反应式为___________ 。
②质子交换膜右侧的溶液在反应后pH___________ (填“增大”“减小”或“不变”)。
③当外电路通过0.2 mol e-时,质子交换膜左侧的溶液质量___________ (填“增大”或“减小”)___________ g。
(1)我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2
 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
①放电时,正极的电极反应式为
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28 g时,转移电子的物质的量为
③可选用高氯酸钠-四甘醇二甲醚作电解液的理由是
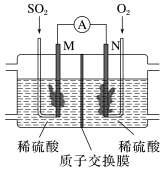
(2)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。

①M极发生的电极反应式为
②质子交换膜右侧的溶液在反应后pH
③当外电路通过0.2 mol e-时,质子交换膜左侧的溶液质量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】原电池是化学对人类的一项重大贡献。回答下列问题:
(1)铁是用途最广的金属材料之一,但生铁易生锈。请讨论电化学实验中有关铁的性质。
①某原电池装置如图所示,右侧烧杯中的电极反应式为___________ 。
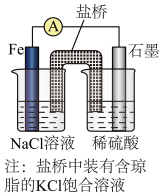
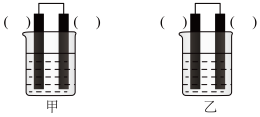
②已知下图甲、乙两池的总反应式均为Fe+H2SO4=FeSO4+H2↑,且在同侧电极(指均在“左电极”或“右电极”)产生H2。请在两池上标出电极材料___________ (填“Fe”或“C”)。
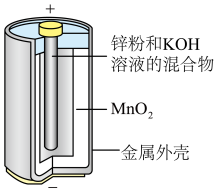
(2)碱性锌锰干电池的剖面图如图所示,已知电池放电后的产物是Zn(OH)2和MnOOH,则其总反应式为___________ ,负极电极反应式为___________ 。
(3)用高铁(Ⅵ)酸盐设计的高铁(Ⅵ)电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应为3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH。
①写出正极电极反应式:___________ 。
②用高铁(Ⅵ)电池作电源,以Fe作阳极,以Cu作阴极,对足量KOH溶液进行电解,当电池中有0.2 mol K2FeO4反应时,则在电解池中生成___________ L(标准状况) H2。
(1)铁是用途最广的金属材料之一,但生铁易生锈。请讨论电化学实验中有关铁的性质。
①某原电池装置如图所示,右侧烧杯中的电极反应式为

②已知下图甲、乙两池的总反应式均为Fe+H2SO4=FeSO4+H2↑,且在同侧电极(指均在“左电极”或“右电极”)产生H2。请在两池上标出电极材料

(2)碱性锌锰干电池的剖面图如图所示,已知电池放电后的产物是Zn(OH)2和MnOOH,则其总反应式为

(3)用高铁(Ⅵ)酸盐设计的高铁(Ⅵ)电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应为3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH。
①写出正极电极反应式:
②用高铁(Ⅵ)电池作电源,以Fe作阳极,以Cu作阴极,对足量KOH溶液进行电解,当电池中有0.2 mol K2FeO4反应时,则在电解池中生成
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:

(1)以下叙述中,正确的是____ 。
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液的 均增大 D.乙中电子从铜片经导线流向锌片
均增大 D.乙中电子从铜片经导线流向锌片
E.乙溶液中 向锌片方向移动
向锌片方向移动
(2)变化过程中能量转化的形式主要是:甲为____ (填写选项字母)。
A.将化学能转化成热能 B.将电能转化成为化学能 C.将化学能转化成电能
(3)若反应过程中有 电子发生转移,则生成的氢气在标况下的体积为
电子发生转移,则生成的氢气在标况下的体积为____ L。
(4)下列反应可以作为原电池工作时发生的反应的是:_______。
(5)乙中负极电极反应方程式为:________ 。

(1)以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液的
 均增大 D.乙中电子从铜片经导线流向锌片
均增大 D.乙中电子从铜片经导线流向锌片E.乙溶液中
 向锌片方向移动
向锌片方向移动(2)变化过程中能量转化的形式主要是:甲为
A.将化学能转化成热能 B.将电能转化成为化学能 C.将化学能转化成电能
(3)若反应过程中有
 电子发生转移,则生成的氢气在标况下的体积为
电子发生转移,则生成的氢气在标况下的体积为(4)下列反应可以作为原电池工作时发生的反应的是:_______。
A.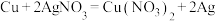 | B.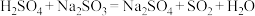 |
C. | D.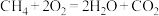 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图所示,甲、乙两装置电极材料都是铁棒与碳棒,请回答下列问题:
(1)若两装置中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲装置中的________ 棒,乙装置中的________ 棒。
②乙装置中阳极的电极反应式是:_______________________________ 。
(2)若两装置中均为饱和NaCl溶液:
①写出乙装置中总反应的离子方程式:__________________________________ 。
②甲装置中碳极的电极反应式是____________________ ,乙装置碳极的电极反应属于________ (填“氧化反应”或“还原反应”)。
③将湿润的淀粉KI试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因:____________________ 。
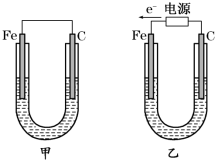
(1)若两装置中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲装置中的
②乙装置中阳极的电极反应式是:
(2)若两装置中均为饱和NaCl溶液:
①写出乙装置中总反应的离子方程式:
②甲装置中碳极的电极反应式是
③将湿润的淀粉KI试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学电源在日常生活和工业生产中有着重要的应用。
Ⅰ.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:
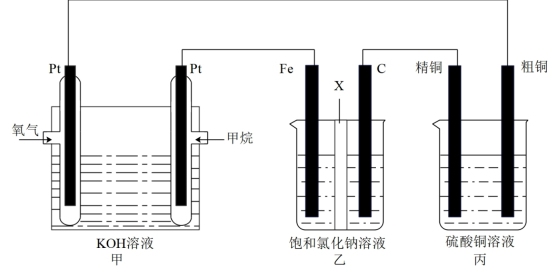
(1)甲烷燃料电池负极的电极反应式为___________ 。
(2)C极的电极反应式为___________ 。
(3)若有2.24L(标准状况下)氧气参加反应,则乙装置中铁极上生成的气体体积为___________ L(标准状况下);丙装置中阴极析出铜的质量为___________ g。
Ⅱ.科学家发明的一种光化学电池可充分利用太阳能,其结构如图所示,电池总反应为AgCl(s)+Cu+(aq) Ag(s)+Cu2+(aq)+Cl-(aq)
Ag(s)+Cu2+(aq)+Cl-(aq)
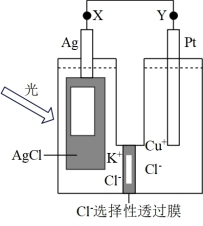
(4)①Cl-的迁移方向为___________ (填“正极到负极”或“负极到正极”)。
②正极的电极反应式为___________ 。
③若用该光化学电池为手机充电并将手机电池从零电量充满,若该手机电池容量为3200mA/h,则理论上消耗AgCl的质量为___________ g(保留一位小数)(已知:1库仑约为1.0×10-5mol电子所带的电量)。
Ⅰ.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:

(1)甲烷燃料电池负极的电极反应式为
(2)C极的电极反应式为
(3)若有2.24L(标准状况下)氧气参加反应,则乙装置中铁极上生成的气体体积为
Ⅱ.科学家发明的一种光化学电池可充分利用太阳能,其结构如图所示,电池总反应为AgCl(s)+Cu+(aq)
 Ag(s)+Cu2+(aq)+Cl-(aq)
Ag(s)+Cu2+(aq)+Cl-(aq)
(4)①Cl-的迁移方向为
②正极的电极反应式为
③若用该光化学电池为手机充电并将手机电池从零电量充满,若该手机电池容量为3200mA/h,则理论上消耗AgCl的质量为
您最近一年使用:0次