下列事实不能用勒夏特列原理解释的是( )
| A.工业制硫酸采用二氧化硫催化氧化,高压可以提高单位时间SO3的产量 |
| B.打开可乐瓶盖后看到有大量气泡冒出 |
| C.用饱和食盐水除去氯气中氯化氢杂质 |
| D.容器中有2HI(g) ⇌ H2(g)+I2(g),增大压强颜色变深 |
更新时间:2019-11-20 13:44:01
|
相似题推荐
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】下列有关速率与平衡的说法正确的是
| A.化学反应速率改变,平衡一定移动 | B.平衡发生移动,平衡常数一定变化 |
| C.增加某种反应物的量,平衡一定正向移动 | D.平衡正向移动,反应物的转化率不一定增大 |
您最近半年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】下面是四位同学在学习“化学反应的速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是
| A.化学反应速率理论可指导怎样提高原料的平衡转化率 |
| B.化学有效碰撞理论可用来解释改变外界条件反应速率的影响 |
| C.化学平衡理论可指导怎样使用有限原料多出产品 |
| D.研究化学反应进行的方向可指导判断反应在某个方向发生的可能性 |
您最近半年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】在新制的氯水中存在平衡:Cl2+H2O H++Cl-+HClO,若向氯水中投入少量碳酸钙粉末,溶液中发生的变化是
H++Cl-+HClO,若向氯水中投入少量碳酸钙粉末,溶液中发生的变化是
 H++Cl-+HClO,若向氯水中投入少量碳酸钙粉末,溶液中发生的变化是
H++Cl-+HClO,若向氯水中投入少量碳酸钙粉末,溶液中发生的变化是| A.H+浓度减小,HClO浓度减小 | B.H+浓度增大,HClO浓度增大 |
| C.H+浓度减小,HClO浓度增大 | D.H+浓度增大,HClO浓度减小 |
您最近半年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】已知:2Fe3+(aq)+2I-(aq) 2Fe2+(aq)+I2(aq),向试管中滴加1mL0.1mol/LKI溶液与5mL0.1mol/LFeCl3溶液,反应达到平衡时,下列说法错误的是
2Fe2+(aq)+I2(aq),向试管中滴加1mL0.1mol/LKI溶液与5mL0.1mol/LFeCl3溶液,反应达到平衡时,下列说法错误的是
 2Fe2+(aq)+I2(aq),向试管中滴加1mL0.1mol/LKI溶液与5mL0.1mol/LFeCl3溶液,反应达到平衡时,下列说法错误的是
2Fe2+(aq)+I2(aq),向试管中滴加1mL0.1mol/LKI溶液与5mL0.1mol/LFeCl3溶液,反应达到平衡时,下列说法错误的是A.该反应平衡常数K=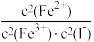 |
| B.加入FeSO4固体,平衡逆向移动 |
| C.加入苯,振荡,平衡正向移动 |
| D.经苯两次萃取分离后,在水溶液中加入KSCN,溶液呈红色,则该化学反应存在限度 |
您最近半年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】已知反应CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是
CO2(g)+H2(g) ΔH<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是
 CO2(g)+H2(g) ΔH<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是
CO2(g)+H2(g) ΔH<0。在一定温度和压强下于密闭容器中,反应达到平衡。下列叙述正确的是| A.升高温度,K减小 | B.减小压强,n(CO2)增加 |
| C.更换高效催化剂,α(CO)增大 | D.充入一定量的氮气,n(H2)减小 |
您最近半年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】如图为可逆反应。A(s)+D(g) E(g);△H<0的逆反应速率随时间变化情况,试根据图中曲线判断下列说法中不正确的是
E(g);△H<0的逆反应速率随时间变化情况,试根据图中曲线判断下列说法中不正确的是

 E(g);△H<0的逆反应速率随时间变化情况,试根据图中曲线判断下列说法中不正确的是
E(g);△H<0的逆反应速率随时间变化情况,试根据图中曲线判断下列说法中不正确的是
| A.t3时刻可能采取的措施是减小c(D) | B.t5时刻可能采取的措施是降温 |
| C.t7时刻可能采取的措施是减小压强 | D.t5~t6时间段平衡向逆反应方向移动 |
您最近半年使用:0次
单选题
|
容易
(0.94)
名校
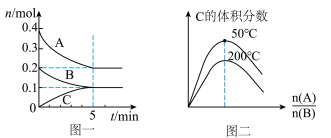
【推荐3】在2L恒容密闭容器中加入一定量A和B,发生反应aA(g)+bB(g) cC(g)。100℃时容器中A、B、C物质的量随时间的变化关系如图一所示。不同温度下平衡时C的体积分数与A、B起始时的投料比的变化关系如图二所示。则下列结论正确的是
cC(g)。100℃时容器中A、B、C物质的量随时间的变化关系如图一所示。不同温度下平衡时C的体积分数与A、B起始时的投料比的变化关系如图二所示。则下列结论正确的是
 cC(g)。100℃时容器中A、B、C物质的量随时间的变化关系如图一所示。不同温度下平衡时C的体积分数与A、B起始时的投料比的变化关系如图二所示。则下列结论正确的是
cC(g)。100℃时容器中A、B、C物质的量随时间的变化关系如图一所示。不同温度下平衡时C的体积分数与A、B起始时的投料比的变化关系如图二所示。则下列结论正确的是
A.aA(g)+bB(g) cC(g) △H>0 cC(g) △H>0 |
| B.100℃时达平衡的体系中充入少量C(g),达新平衡前v(逆)>v(正) |
| C.100℃时前5min平均化学反应速率v(A)=0.04mol•L-1•min-1 |
D.某温度下平衡时B的转化率随起始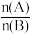 的增大而减小 的增大而减小 |
您最近半年使用:0次
单选题
|
容易
(0.94)
【推荐1】下列事实不能用勒夏特列原理解释的是
| A.使用铁触媒,加快合成氨的反应速率 |
B.溴水中存在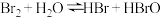 ,当加入硝酸银溶液后,溶液颜色变浅 ,当加入硝酸银溶液后,溶液颜色变浅 |
C.合成氨工业采用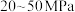 高压 高压 |
D.反应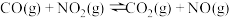 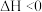 ,达到平衡后,升高温度体系颜色变深 ,达到平衡后,升高温度体系颜色变深 |
您最近半年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】下列事实不能 用勒夏特列原理来解释的是
| A.实验室中常用排饱和食盐水的方法收集Cl2 |
| B.鼓入过量空气有利于SO2转化为SO3 |
| C.开启啤酒瓶后,瓶中立刻泛起大量泡沫 |
| D.煅烧硫铁矿时先将矿石粉碎 |
您最近半年使用:0次

 2SO3正反应放热,为了提高二氧化硫的转化率,下列措施可行的是
2SO3正反应放热,为了提高二氧化硫的转化率,下列措施可行的是

