已知NaHSO3溶液呈酸性、NaHCO3溶液呈碱性。现有浓度均为0.1 mol/L-1的NaHSO3溶液和NaHCO3溶液,溶液中各粒子的物质的量浓度存在下列关系(R表示S或C),其中一定正确的是
| A.c(Na+)>c(HRO3-)>c(H+)>c(RO32-)>c(OH-) |
| B.c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-) |
| C.c(RO32-)+c(HRO3-)+c(H2RO3)=c(Na+) |
| D.两溶液中c(Na+)、c(HRO3-)、c(RO32-)分别相等 |
更新时间:2019-12-19 19:23:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素X、Y、Z、R、T的原子半径与原子序数关系如图所示。R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的化合物Z2T能破坏水的电离平衡。下列推断正确的是


| A.原子半径和离子半径均满足:Y>Z |
| B.氢化物的沸点不一定是:Y>R |
| C.最高价氧化物对应水化物的酸性:T<R |
| D.由X、R、Y、Z四种元素组成的化合物水溶液一定显碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】0.1mol·L-1Na2CO3溶液和0.1mol·L-1NaHCO3溶液的pH的大小关系是
| A.前者大 | B.相等 | C.前者小 | D.不能肯定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】浓度均为0.01 mol·L-1Na2CO3和NaHCO3的混合溶液中,下列说法正确的是
A.c(HCO )略大于c(CO )略大于c(CO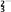 ) ) |
| B.c(H2CO3)略大于c(OH-) |
C.c(Na+)等于c(CO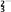 )与c(HCO )与c(HCO )之和 )之和 |
| D.c(OH-)略大于c(HCO3-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列溶液中各微粒的浓度关系正确的是
A.常温下,将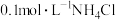 溶液与 溶液与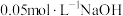 溶液等体积混合溶液显碱性, 溶液等体积混合溶液显碱性, |
B.在纯碱溶液中存在: |
C.常温下,向 溶液中加入适量的NaOH,得到 溶液中加入适量的NaOH,得到 的混合溶液: 的混合溶液: |
D. 的一元酸HX和 的一元酸HX和 的一元碱MOH等体积混合: 的一元碱MOH等体积混合: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】pC类似于pH,是指极稀溶液中的溶质浓度的常用对数的负值。如某溶液中某溶质的浓度为1×10-3mol/L,则该溶液中该溶质的pC=-lg(1×10-3)=3。如图为25℃时H2CO3溶液的pC-pH图(若离子浓度小于10-5mol/L,可认为该离子不存在)。下列说法不正确的是


| A.某温度下,CO2饱和溶液的浓度是0.05 mol•L-1,其中1/5的CO2转变为H2CO3,若此时溶液的pH约为5,据此可得该温度下CO2饱和溶液中H2CO3的电离度为0.1% , |
| B.25℃时,H2CO3一级电离平衡常数的数值Ka1=10-6 |
| C.向Na2CO3溶液中滴加盐酸至pH等于11时,溶液中:c(Na+)+c(H+)=2c(CO32﹣)+c(OH﹣)+c(HCO3﹣) |
| D.25℃时,0.1mol/LNa2CO3中c(HCO3﹣)比0.1mol/LH2CO3中c(HCO3﹣)大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,向1L0.1mol/LH2A溶液中加入NaOH固体,所得溶液中所有含A元素的微粒的物质的量分数随溶液pH的变化如图所示(忽略溶液体积变化)。下列叙述正确的是


| A.HA-水解方程式为H2O+HA-⇌H2A+OH- |
| B.A2-的水解平衡常数Kh=10-3 |
| C.NaHA溶液中:c(Na+)=c(H2A)+c(HA-)+c(A2-) |
| D.pH=5时,在NaHA和Na2A的混合溶液中:2c(A2-)+c(HA-)-c(Na+)=(10-5-10-9)mol/L |
您最近一年使用:0次

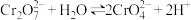 向右移动
向右移动 溶液中加入
溶液中加入 固体,溶液红色变浅
固体,溶液红色变浅 转化为
转化为
 时,向
时,向 溶液中滴加甲基橙溶液,溶液变红
溶液中滴加甲基橙溶液,溶液变红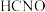 的电离平衡常数大于
的电离平衡常数大于 的电离平衡常数
的电离平衡常数

