对于0.1 mol·L-1 Na2SO3溶液,正确的是( )
| A.升高温度,溶液的pH降低 |
| B.c(Na+)=2c(SO32-)+c(HSO3-)+c(H2SO3) |
| C.c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-) |
| D.加入少量NaOH固体,c(SO32-)与c(Na+)均增大 |
更新时间:2020-01-10 12:39:51
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列关于 水解的说法错误的是( )
水解的说法错误的是( )
 水解的说法错误的是( )
水解的说法错误的是( )A.浓度相同时, 溶液在30℃时的水解程度大于20℃时的水解程度 溶液在30℃时的水解程度大于20℃时的水解程度 |
B.温度相同时,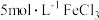 溶液的水解程度大于 溶液的水解程度大于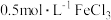 溶液的水解程度 溶液的水解程度 |
C. 溶液在保存时,可加入少量的盐酸抑制 溶液在保存时,可加入少量的盐酸抑制 的水解 的水解 |
D.用 固体配制溶液时,先溶在盐酸中,然后再稀释到所需的浓度 固体配制溶液时,先溶在盐酸中,然后再稀释到所需的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
| A.一般情况下,盐类越稀越易水解,所以稀释盐溶液,Kh(水解平衡常数)变大 |
| B.一般情况下,一元弱碱的Kb值越大碱性越弱 |
| C.Kw随着溶液中c(H+)和c(OH-)的改变而改变 |
| D.一般情况下,Ksp越大,难溶电解质在水中的溶解程度就越高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】向仅含SO 、I-、Br-且物质的量分别为m、n、6mol的钠盐溶液中通入适量氯气,溶液中这三种离子的物质的量的变化如图所示。下列说法中正确的是
、I-、Br-且物质的量分别为m、n、6mol的钠盐溶液中通入适量氯气,溶液中这三种离子的物质的量的变化如图所示。下列说法中正确的是

 、I-、Br-且物质的量分别为m、n、6mol的钠盐溶液中通入适量氯气,溶液中这三种离子的物质的量的变化如图所示。下列说法中正确的是
、I-、Br-且物质的量分别为m、n、6mol的钠盐溶液中通入适量氯气,溶液中这三种离子的物质的量的变化如图所示。下列说法中正确的是
| A.曲线II代表Br-的变化情况 |
B.曲线I对应的反应:SO +Cl2+H2O=2H++SO +Cl2+H2O=2H++SO +2Cl- +2Cl- |
| C.m=1、n=4、a=5 |
D.溶液中n(Na+)=n(SO )+n(I-)+n(Br-) )+n(I-)+n(Br-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温,已知电离常数:Kb(NH3·H2O)=1.81×10-5,Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5.下列说法中正确的是
A.(NH4)2C2O4溶液中,c(NH )=2c(C2O )=2c(C2O ) ) |
| B.等物质的量浓度的氢氧化钠溶液和H2C2O4溶液等体积混合,所得溶液呈碱性 |
| C.pH=11的氢氧化钠溶液与pH=3的H2C2O4溶液等体积混合,所得溶液呈碱性 |
D.用H2C2O4溶液中和氨水至中性时,溶液中c(NH4+)=2c(C2O ) + c(HC2O ) + c(HC2O ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列溶液,加热后颜色变浅的是
| A.稀氨水和酚酞溶液 | B.滴有酚酞的Na2CO3溶液 |
| C.溶有氯气的品红溶液 | D.溶有SO2的品红溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验事实不能 用平衡移动原理解释的是
A. | ||||||
B.
| ||||||
C.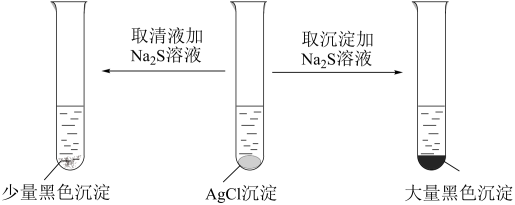 | ||||||
D.
|
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定条件下的CH3COONa溶液中。下列说法不正确的是
| A.加入少量NaOH固体,c(CH3COO-)增大 |
| B.加入少量FeCl3固体,c(CH3COO-)减小 |
| C.稀释溶液,溶液的pH减小 |
| D.加入适量醋酸得到的酸性混合溶液:c (Na+)>c(CH3COO-)>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】 溶液中存在水解平衡:
溶液中存在水解平衡: 。下列说法错误的是
。下列说法错误的是
 溶液中存在水解平衡:
溶液中存在水解平衡: 。下列说法错误的是
。下列说法错误的是A.通入 ,溶液pH减小 ,溶液pH减小 | B.升高温度,平衡常数增大 |
| C.加水稀释,溶液中所有离子的浓度都减小 | D.加入 固体, 固体,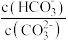 减小 减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列各溶液中,微粒的物质的量浓度关系正确的是
| A.0.lmol/LNa2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| B.0.1mol·L-1NH4Cl溶液:c(NH4+)=c(Cl-) |
| C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.等物质的量浓度的①NH4Cl溶液②(NH4)2SO4溶液 ③NH4HSO4溶液 ④(NH4)2CO3溶液中NH4+浓度的大小关系是②>④>①>③ |
您最近一年使用:0次

 溶液,沉淀变黑,说明相同条件下溶解度CuS比ZnS更小
溶液,沉淀变黑,说明相同条件下溶解度CuS比ZnS更小 是一种常见二元弱酸,用
是一种常见二元弱酸,用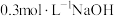 溶液滴定20mL同浓度的
溶液滴定20mL同浓度的 、
、 ,下列说法错误的是
,下列说法错误的是
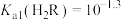
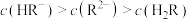

 HCO3-+OH-
HCO3-+OH-

