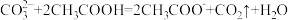NH4HSO4在水溶液中的电离方程式为:NH4HSO4=NH4++H++SO42﹣.现向100mL 0.1mol/LNH4HSO4溶液中滴加0.1mol/LNaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示.下列说法中不正确的是
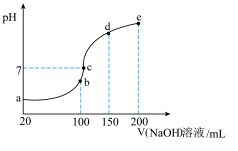

| A.a点的溶液中:c(SO42﹣)>c(NH4+)>c(H+)>c(Na+)>c(OH﹣) |
| B.b点的溶液中:c(Na+)=c(SO42﹣)>c(H+)>c(NH4+)>c(OH﹣) |
| C.c点的溶液中:c(Na+)>c(SO42﹣)>c(NH4+)>c(OH﹣)=c(H+) |
| D.d、e点对应溶液中,水电离程度大小关系是d>e |
更新时间:2019-12-24 11:25:34
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列各组离子在指定溶液中一定能大量共存的是
A. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
B.常温下,由水电离产生的c(OH-)=1×10-12mol·L-1的溶液中: 、 、 、 、 、 、 |
C.无色透明的溶液中: 、Mg2+、 、Mg2+、 、 、 |
D.c(SO )=0.1mol·L-1的溶液:K+、MnO )=0.1mol·L-1的溶液:K+、MnO 、SO 、SO 、H+ 、H+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,在0.1mol/LNaX溶液中,水电离出的OH-浓度浓度为 ;在0.1mol/L盐酸中,水电离出的OH-浓度为
;在0.1mol/L盐酸中,水电离出的OH-浓度为 ,若
,若 ,则NaX溶液的pH值为
,则NaX溶液的pH值为
 ;在0.1mol/L盐酸中,水电离出的OH-浓度为
;在0.1mol/L盐酸中,水电离出的OH-浓度为 ,若
,若 ,则NaX溶液的pH值为
,则NaX溶液的pH值为| A.5 | B.10 | C.11 | D.13 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】H2C2O4(草酸)为二元弱酸,在水溶液中H2C2O4、HC2O4-和C2O42-物质的量分数与pH关系如图所示,下列说法不正确的是
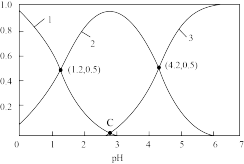

| A.由图可知,草酸的Ka=10-1.2 |
| B.0.1 mol·L—1NaHC2O4溶液中c(Na+)>c(HC2O4-)>c(H+)>c(OH-) |
| C.向草酸溶液中滴加氢氧化钠溶液至pH为4.2时c(Na+)+c(H+)=3c(C2 O42-)+c(OH-) |
| D.根据图中数据计算可得C点溶液pH为2.8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.40g 34%的过氧化氢催化分解,生成0.15mol氧气时转移电子数为0.3 |
B.1L 0.1mol/L磷酸钠溶液含有的 数目为0.1 数目为0.1 |
C.1L  的稀硫酸中含有的氢离子数目为0.2 的稀硫酸中含有的氢离子数目为0.2 |
D.0.1mol/L的氯化铵溶液中 和 和 的粒子数之和为0.1 的粒子数之和为0.1 |
您最近一年使用:0次

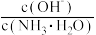 中减小
中减小 ,则该溶液可能是稀盐酸
,则该溶液可能是稀盐酸 的
的 溶液稀释10倍,稀释后溶液的
溶液稀释10倍,稀释后溶液的
 可先用
可先用 处理,使其转化为易溶于酸的
处理,使其转化为易溶于酸的 除去。室温下,用
除去。室温下,用 溶液浸泡
溶液浸泡 分别为
分别为 、
、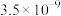 。下列说法正确的是
。下列说法正确的是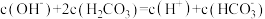
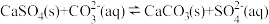 正向进行,需满足
正向进行,需满足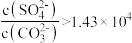
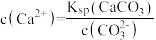 且
且