在20 mL 0.1 mol·L-1的醋酸溶液中,能使溶液的c(H+)增大,而且使醋酸的电离平衡向逆反应方向移动,可加入的试剂是( )
| A.20 mL水 | B.浓盐酸 | C.冰醋酸 | D.NaOH溶液 |
更新时间:2020-01-07 15:34:44
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列因素能影响水的电离平衡,且能使水的电离平衡向右移动的是
| A.CH3COOH | B.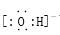 | C.升高温度 | D.bX-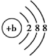 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】醋酸在水中电离方程式可表示为:CH3COOH⇌CH3COO-+H+△H>0,下列操作能使H+浓度增大的是( )
| A.加入少量NaOH固体 | B.加入固体CH3COONa |
| C.加入锌粉 | D.加热升温10℃ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列方法中不能使0.10mol/L氨水中NH3·H2O电离程度增大的是
| A.加水稀释 | B.微热溶液 |
| C.滴加少量浓盐酸 | D.加入少量氯化铵晶体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列叙述正确的是
| A.稀醋酸中加入少量浓醋酸能增大醋酸的电离程度 |
B.若NH4Cl溶液与 NH4HSO4溶液的 相等,则 相等,则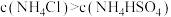 |
C.向盐酸中加入氨水至中性,溶液中 |
| D.AgCl固体在100mL 0.01mol/L NaCl溶液中的 Ksp比在100mL 0.01moL BaCl2中的Ksp大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】室温下,往0.1 mol·L-1的氨水中滴入酚酞溶液时,溶液将呈现粉红色。现采取下列措施,滴有酚酞的氨水溶液颜色不会变浅的是
| A.往溶液中滴入稀硫酸 | B.往溶液中加入NH4Cl晶体 |
| C.把溶液加热至沸腾 | D.往溶液中加入NaOH固体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在0.1 mol·L-1的CH3COOH溶液中,要抑制醋酸电离,且c(H+)增大,应采取的措施是
| A.加水 | B.升温 | C.加适量CH3COONa固体 | D.通适量HCl气体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】已知水中存在如下平衡:H2O+H2O H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是( )
H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是( )
 H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是( )
H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是( )| A.向水中加入NaHSO4 | B.向水中加入Cu(NO3)2 |
| C.加热水至100℃[其中c(H+)=1×10-6mol·L-1] | D.在水中加入Na2CO3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列方法中不能使0.10mol/L氨水中NH3·H2O电离程度增大的是
| A.加水稀释 | B.微热溶液 |
| C.滴加少量浓盐酸 | D.加入少量氯化铵晶体 |
您最近一年使用:0次

 不变
不变
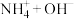 当其它条件不变时,改变下列条件,平衡逆向移动,且
当其它条件不变时,改变下列条件,平衡逆向移动,且 增大的是
增大的是
 NH3·H2O
NH3·H2O

