常温下,用0.1mol/L盐酸或NaOH溶液滴定体积均为20 mL,浓度均为0.1mol/L的MOH、HX溶液,滴定曲线如图所示。下列说法错误的是
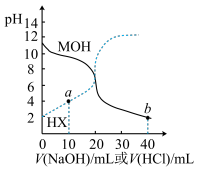

| A.两个滴定实验均可用酚酞作指示剂 |
| B.常温下0.1mol/LMX溶液的pH<7 |
| C.a点溶液中存在:c(X-)>c(HX) |
| D.b点溶液中存在:2c(MOH)+c(M+)+c(OH-)=c(H+) |
更新时间:2020-01-17 13:13:34
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关实验操作的叙述不正确 的是
| A.可用氨水除去试管内壁上的银镜 |
| B.用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏大 |
| C.蒸馏完毕后,应先停止加热,待装置冷却后,停止通水,再拆卸蒸馏装置 |
| D.用标准盐酸溶液滴定氨水来测定其浓度,选择甲基橙为指示剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验装置或操作能达到相应实验目的的是
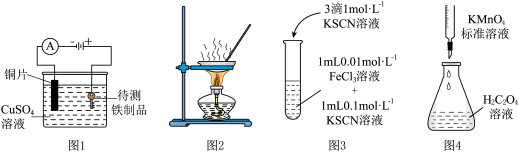

| A.图1铁上电镀铜 | B.图2蒸发 溶液制得 溶液制得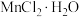 |
| C.图3增大反应物浓度,平衡正向移动 | D.图4测定 溶液的浓度 溶液的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】某学习小组用“间接碘量法”测定某 晶体试样的纯度,试样不含其他能与
晶体试样的纯度,试样不含其他能与 发生反应的氧化性杂质。已知:
发生反应的氧化性杂质。已知: ,
, 。m g试样溶于水,加入过量KI固体,充分反应,用0.1000 mol·L⁻¹的
。m g试样溶于水,加入过量KI固体,充分反应,用0.1000 mol·L⁻¹的 标准溶液滴定,部分实验仪器和读数如图所示。
标准溶液滴定,部分实验仪器和读数如图所示。

下列说法错误的是
 晶体试样的纯度,试样不含其他能与
晶体试样的纯度,试样不含其他能与 发生反应的氧化性杂质。已知:
发生反应的氧化性杂质。已知: ,
, 。m g试样溶于水,加入过量KI固体,充分反应,用0.1000 mol·L⁻¹的
。m g试样溶于水,加入过量KI固体,充分反应,用0.1000 mol·L⁻¹的 标准溶液滴定,部分实验仪器和读数如图所示。
标准溶液滴定,部分实验仪器和读数如图所示。
下列说法错误的是
| A.试样在甲中溶解,滴定管选丙 |
B.丁图中滴定前,滴定管的读数为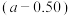 mL mL |
| C.用淀粉作指示剂,当甲中溶液由蓝色变为无色且30 s内不恢复原色时,达到滴定终点 |
| D.对装有标准液的滴定管读数时,滴定前后读数方式如丁图所示,则测得的结果偏小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】实验室现有3种酸碱指示剂,其pH的变色范围如下:甲基橙:3.1~4.4,石蕊:5.0~8.0,酚酞:8.2~10.0,用0.1000mol·L-1NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述正确的是
| A.溶液呈中性,可选用甲基橙或酚酞作指示剂 |
| B.溶液呈中性,只能选用石蕊作指示剂 |
| C.溶液呈碱性,可选用甲基橙或酚酞作指示剂 |
| D.溶液呈碱性,只能选用酚酞作指示剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃下,弱电解质的电离平衡常数Ka(CH3COOH) = Kb(NH3•H2O) = 1.75×10-5,下列说法正确的是
| A.用0.1mol/L的盐酸滴定0.1mol/L的氨水时,可用酚酞作指示剂 |
| B.0.2mol/L的醋酸与0.1mol/L的氢氧化钠溶液等体积混合,所得溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH) +c(H+) |
| C.pH相同的①CH3COONa、②NaClO的两种溶液的c(Na+):① > ② |
| D.pH=3的醋酸与pH=11的氨水等体积混合,所得溶液中由水电离出的c(H+)=1×10-7mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,下列有关稀溶液中离子浓度的说法正确的是
| A.同浓度的四种溶液:① NH4Cl② (NH4)2SO4③ NH4HSO4④ NH4Al(SO4)2溶液,c(NH4+)浓度的大小关系:②>④>③>① |
| B.一定浓度的NaHS溶液中:c(Na+)+c(OH-)=c(H+)+c(HS-)+2c(H2S) |
| C.若0.1 mol/L NH4Cl溶液pH=5,则其中离子浓度最大与最小的差值为(0.1-10-5)mol/L |
| D.现有四种溶液:① pH=4的H2SO4溶液② pH=4的NH4Cl溶液③ pH=10的氨水④ pH=10的CH3COONa溶液,其中水电离出的氢离子浓度大小关系为:②=④>③>① |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在常温下,有关下列四种溶液的叙述不正确的是
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| A.分别取1mL稀释至100mL,四种溶液的pH:②>①>④>③ |
| B.在①、②中分别加入适量的氯化铵晶体,两种溶液的pH均减小 |
| C.将②、③等体积混合,所得溶液pH=4.7:c(CH3COO−)>c(Na+)>c(H+)>c(OH−) |
| D.若将aL④与bL②混合后(忽略溶液体积变化),溶液的pH=4,则a:b=11:9 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,二元弱酸H2Y溶液中滴加KOH溶液,所得混合溶液的pH与离子浓度变化的关系如图所示,下列有关说法不正确的是
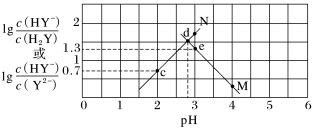
A.曲线M表示pH与lg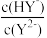 的变化关系 的变化关系 |
| B.NaHY溶液显酸性 |
| C.交点d对应的pH=2.8 |
| D.e点溶液中:c(HY-)>c(H2Y)>c(Y2-)>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】亚氯酸钠(NaClO2)用于漂白织物、纤维、纸浆,具有对纤维损伤小的特点.其在溶液中可生成ClO2、HClO2、ClO2﹣、Cl﹣等,其中HClO2和ClO2都具有漂白作用.已知pOH=﹣lgc(OH﹣),经测定25℃时各组分含量随pOH变化情况如图所示(Cl﹣没有画出),此温度下,下列分析正确的是
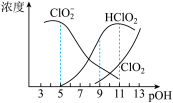
| A.HClO2的电离平衡常数的数值Ka=10﹣6 |
| B.亚氯酸钠在酸性条件下较稳定 |
| C.pH=7时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2﹣)>c(ClO2)>c(Cl﹣) |
| D.同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有c(HClO2)-2c(H+)=c(ClO2﹣)-2c(OH﹣) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,向25.00 mL 0.100 0 mol·L−1的醋酸溶液中逐滴加入0.100 0 mol·L−1 NaOH溶液,pH随NaOH溶液体积的变化曲线如图所示。下列说法不正确的是
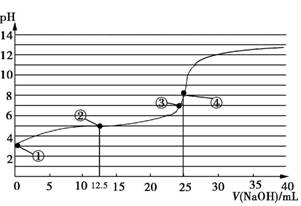

| A.当V(NaOH)=0时,c(CH3COOH)>c(H+)>c(CH3COO−)>c(OH−) |
| B.①②③④点的水溶液导电能力依次增强 |
| C.当V(NaOH)=12.5 mL时,c(CH3COO−)+c(OH−)=c(CH3COOH)+c(H+) |
| D.当V(NaOH)>25 mL时,可能出现c(Na+)>c(OH−)>c(CH3COO−)>c(H+) |
您最近一年使用:0次

 ):③>②>①
):③>②>① )+c(H2SeO4)+c(SeO
)+c(H2SeO4)+c(SeO

