在一恒容的密闭容器中,加入1 mol CO(g)、2 mol H2O(g),发生反应CO(g)+H2O(g) H2(g)+CO2(g) ΔH,CO的平衡转化率随温度的变化如图所示。
H2(g)+CO2(g) ΔH,CO的平衡转化率随温度的变化如图所示。
①该反应的ΔH____ (填“<”或“>”)0。
②在体积不变时,要增大该反应的正反应速率可采取的措施是____ (任写一条)。
③A点时该反应的平衡常数为____ (精确到0.01)。
 H2(g)+CO2(g) ΔH,CO的平衡转化率随温度的变化如图所示。
H2(g)+CO2(g) ΔH,CO的平衡转化率随温度的变化如图所示。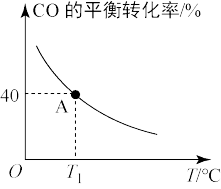
①该反应的ΔH
②在体积不变时,要增大该反应的正反应速率可采取的措施是
③A点时该反应的平衡常数为
更新时间:2020-01-18 09:55:11
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】卤素化合物在生产生活中应用广泛,回答下列问题
(1)研究表明 气体中存在单体和环状六聚体的平衡:
气体中存在单体和环状六聚体的平衡: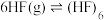 ,HF形成环状六聚体的作用力是
,HF形成环状六聚体的作用力是____________ ;在测定 相对分子质量的实验中,
相对分子质量的实验中,____________ (填“低压”或“高压”)有利于测定的准确性.
(2) 气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸
气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸 和氯酸钾
和氯酸钾 在酸性条件下制备
在酸性条件下制备 ,离子方程式为
,离子方程式为__________ ;产物中的另一种气体可以起到的作用是________________ .
(3) 与
与 以共价键形成
以共价键形成 ,其中
,其中________ 显负电性, 与水反应的方程式是
与水反应的方程式是____________ .
(4)利用 和浓磷酸制备
和浓磷酸制备 的原理是:
的原理是: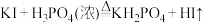 ,该反应中利用了浓磷酸的什么性质:
,该反应中利用了浓磷酸的什么性质:________ (“强酸性”“强氧化性”“高沸点”).
(1)研究表明
 气体中存在单体和环状六聚体的平衡:
气体中存在单体和环状六聚体的平衡: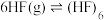 ,HF形成环状六聚体的作用力是
,HF形成环状六聚体的作用力是 相对分子质量的实验中,
相对分子质量的实验中,(2)
 气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸
气体是高效绿色消毒剂,但其性质不稳定,浓度大时会发生爆炸.可用草酸 和氯酸钾
和氯酸钾 在酸性条件下制备
在酸性条件下制备 ,离子方程式为
,离子方程式为(3)
 与
与 以共价键形成
以共价键形成 ,其中
,其中 与水反应的方程式是
与水反应的方程式是(4)利用
 和浓磷酸制备
和浓磷酸制备 的原理是:
的原理是: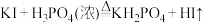 ,该反应中利用了浓磷酸的什么性质:
,该反应中利用了浓磷酸的什么性质:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氨氮( )废水造成水体富营养化,必须脱除才能排放,常用的方法有化学沉淀法、氧化法等。
)废水造成水体富营养化,必须脱除才能排放,常用的方法有化学沉淀法、氧化法等。
I.化学沉淀法:
(1)向含有氨氮的废水中添加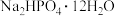 和
和 ,发生反应,生成
,发生反应,生成 沉淀,写出该反应的离子方程式
沉淀,写出该反应的离子方程式_______ 。
(2)为探究溶液酸碱性对氨氮脱除效果的影响,室温下配制氨氮废水[ ],对该废水进行
],对该废水进行 值与氨氮脱除效果影响的实验研究,研究结果如图:
值与氨氮脱除效果影响的实验研究,研究结果如图:

①氨氮脱除效果最佳的 范围是
范围是_______ 。
a.6~7b.8~10c.10~12
② 氨氮脱除率较低的原因为
氨氮脱除率较低的原因为___ , 造成氨氮脱除率随
造成氨氮脱除率随 增大而减小的可能原因是
增大而减小的可能原因是____ 。
II.氧化法:
 和
和 在有氧条件及催化剂作用下发生反应:
在有氧条件及催化剂作用下发生反应:
 ,当温度升高到550~700℃时,NO转化率明显下降,
,当温度升高到550~700℃时,NO转化率明显下降, 产率明显上升,可能原因是
产率明显上升,可能原因是___ 。
 )废水造成水体富营养化,必须脱除才能排放,常用的方法有化学沉淀法、氧化法等。
)废水造成水体富营养化,必须脱除才能排放,常用的方法有化学沉淀法、氧化法等。I.化学沉淀法:
(1)向含有氨氮的废水中添加
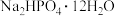 和
和 ,发生反应,生成
,发生反应,生成 沉淀,写出该反应的离子方程式
沉淀,写出该反应的离子方程式(2)为探究溶液酸碱性对氨氮脱除效果的影响,室温下配制氨氮废水[
 ],对该废水进行
],对该废水进行 值与氨氮脱除效果影响的实验研究,研究结果如图:
值与氨氮脱除效果影响的实验研究,研究结果如图:
①氨氮脱除效果最佳的
 范围是
范围是a.6~7b.8~10c.10~12
②
 氨氮脱除率较低的原因为
氨氮脱除率较低的原因为 造成氨氮脱除率随
造成氨氮脱除率随 增大而减小的可能原因是
增大而减小的可能原因是II.氧化法:
 和
和 在有氧条件及催化剂作用下发生反应:
在有氧条件及催化剂作用下发生反应:
 ,当温度升高到550~700℃时,NO转化率明显下降,
,当温度升高到550~700℃时,NO转化率明显下降, 产率明显上升,可能原因是
产率明显上升,可能原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图1所示。根据图中数据,试填写下列空白:

(1)该反应的化学方程式为___________ 。
(2)若X、Y、Z均为气体,反应恰好达到平衡时:
①用Z表示的平均反应速率为___________ ;
②若此时将容器的体积缩小为原来的 倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为
倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为___________ 反应(填“放热”或“吸热”)。
(3)在一密闭容器中发生反应 ,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图2所示。
,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图2所示。
①判断t1、t3、t4时刻分别改变的一个条件是:(填字母代号)
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.恒温恒容时充入氮气
t1时刻___________ ;t3时刻___________ ;t4时刻___________ 。
②依据上述①中的结论,下列时间段中,氨的百分含量最高的是___________ (填字母代号)。
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6。

(1)该反应的化学方程式为
(2)若X、Y、Z均为气体,反应恰好达到平衡时:
①用Z表示的平均反应速率为
②若此时将容器的体积缩小为原来的
 倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为
倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为(3)在一密闭容器中发生反应
 ,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图2所示。
,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图2所示。①判断t1、t3、t4时刻分别改变的一个条件是:(填字母代号)
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.恒温恒容时充入氮气
t1时刻
②依据上述①中的结论,下列时间段中,氨的百分含量最高的是
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6。
您最近一年使用:0次
【推荐1】在密闭容器中发生反应
 ,该反应达到平衡后,测得如下数据:
,该反应达到平衡后,测得如下数据:
(1)实验1中,10h后达到平衡,H2的平均反应速率为___________  。在此实验的平衡体系中,再加入1mol CO2和1mol H2,平衡将
。在此实验的平衡体系中,再加入1mol CO2和1mol H2,平衡将___________ (“向左”“向右”或“不”)移动。
(2)实验2中,x的值___________(填字母)。
(3)实验3中,y的值为___________ 。
(4)在100℃条件下,下列能说明该反应达到平衡状态的是 (填字母)
(5)对于上述反应,欲提高CO的平衡转化率,下列措施可行的是 。

 ,该反应达到平衡后,测得如下数据:
,该反应达到平衡后,测得如下数据:| 实验序号 | 温度 | 初始CO浓度( ) ) | 初始 浓度( 浓度( ) ) | CO的平衡转化率 |
| 1 | 110 | 1 | 1 | 50% |
| 2 | 100 | 1 | 1 | x |
| 3 | 110 | 0.8 | y | 60% |
(1)实验1中,10h后达到平衡,H2的平均反应速率为
 。在此实验的平衡体系中,再加入1mol CO2和1mol H2,平衡将
。在此实验的平衡体系中,再加入1mol CO2和1mol H2,平衡将(2)实验2中,x的值___________(填字母)。
| A.等于50% | B.小于50% | C.大于50% | D.无法确定 |
(4)在100℃条件下,下列能说明该反应达到平衡状态的是 (填字母)
| A.生成H2O的速率和消耗H2的速率相等 | B. H2的质量不再变化 |
| C.压强不再变化 | D.混合气体的密度不变 |
| A.增大初始时的H2O蒸汽的浓度 | B.增大反应容器的压强 |
| C.适当降低反应的温度 | D.使用更高效的催化剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】化学反应的快慢(速率)和化学反应的限度是化学反应原理的重要组成部分。请回答下列问题:
(1)在一定温度下的定容容器中,当C(s)+CO2(g) 2CO(g)不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的浓度之比等于化学计量数之比,⑦某种气体的百分含量。能说明C(s)+CO2(g)
2CO(g)不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的浓度之比等于化学计量数之比,⑦某种气体的百分含量。能说明C(s)+CO2(g) 2CO(g)达到平衡状态的是
2CO(g)达到平衡状态的是_____ 。
(2)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
回答下列问题:
①该反应为_____ 反应(填“吸热”或“放热”)。
②某温度下,各物质的平衡浓度符合下式:3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为_____ 。
③若830℃时,向容器中充入1molCO、5molH2O,反应达到平衡后,其化学平衡常数K_____ 1.0(填“大于”“小于”或“等于”)。
④若1200℃时在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2mol·L-1、2mol·L-1、4mol·L-1、4mol·L-1,则此时上述反应的平衡移动方向为_____ (填“正反应方向”“逆反应方向”或“不移动”)。
(1)在一定温度下的定容容器中,当C(s)+CO2(g)
 2CO(g)不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的浓度之比等于化学计量数之比,⑦某种气体的百分含量。能说明C(s)+CO2(g)
2CO(g)不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的浓度之比等于化学计量数之比,⑦某种气体的百分含量。能说明C(s)+CO2(g) 2CO(g)达到平衡状态的是
2CO(g)达到平衡状态的是(2)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
①该反应为
②某温度下,各物质的平衡浓度符合下式:3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为
③若830℃时,向容器中充入1molCO、5molH2O,反应达到平衡后,其化学平衡常数K
④若1200℃时在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2mol·L-1、2mol·L-1、4mol·L-1、4mol·L-1,则此时上述反应的平衡移动方向为
您最近一年使用:0次
【推荐3】能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料,为了减少CO的排放,某环境研究小组以CO和H2为原料合成清洁能源二甲醚(DME),反应如下:4H2(g)+2CO(g) CH3OCH3(g)+H2O(g) ΔH=-198kJ·mol-1。
CH3OCH3(g)+H2O(g) ΔH=-198kJ·mol-1。
(1)如图所示能正确反映平衡常数K随温度变化关系的曲线为___ (填曲线标记字母),其判断理由是___ 。
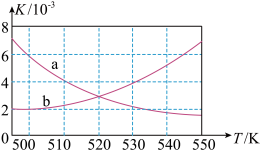
(2)在一定温度下,向2.0L固定容积的密闭容器中充入2molH2和1molCO,经过一段时间后,反应4H2(g)+2CO(g) CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见下表(部分数据未给出):
CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见下表(部分数据未给出):
①0~20min的平均反应速率v(CO)=____ mol·L−1·min−1。
②达到平衡时,H2的转化率为____ 。
③在上述温度下,该反应的平衡常数K=___ 。
④在上述温度下,向平衡后的2L容器中再充入0.4molH2和0.4molCH3OCH3(g),则化学平衡___ 移动(填“向左”“向右”或“不”)。
 CH3OCH3(g)+H2O(g) ΔH=-198kJ·mol-1。
CH3OCH3(g)+H2O(g) ΔH=-198kJ·mol-1。(1)如图所示能正确反映平衡常数K随温度变化关系的曲线为

(2)在一定温度下,向2.0L固定容积的密闭容器中充入2molH2和1molCO,经过一段时间后,反应4H2(g)+2CO(g)
 CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见下表(部分数据未给出):
CH3OCH3(g)+H2O(g)达到平衡。反应过程中测得的部分数据见下表(部分数据未给出):| 时间/min | 0 | 20 | 40 | 80 | 100 |
| n(H2)/mol | 2.0 | 1.4 | 0.85 | 0.4 | |
| n(CO)/mol | 1.0 | 0.425 | 0.2 | 0.2 | |
| n(CH3OCH3)/mol | 0 | 0.15 | 0.4 | ||
| n(H2O)/mol | 0 | 0.15 | 0.2875 | 0.4 | 0.4 |
①0~20min的平均反应速率v(CO)=
②达到平衡时,H2的转化率为
③在上述温度下,该反应的平衡常数K=
④在上述温度下,向平衡后的2L容器中再充入0.4molH2和0.4molCH3OCH3(g),则化学平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)一定条件下的密闭容器中,反应3H2(g)+3CO(g) CH3OCH3(二甲醚)(g)+CO2(g) ΔH<0达到平衡,要提高CO的转化率,可以采取的措施是
CH3OCH3(二甲醚)(g)+CO2(g) ΔH<0达到平衡,要提高CO的转化率,可以采取的措施是____ (填字母代号)。
a.升高温度 b.加入催化剂 c.减小CO2的浓度 d.增加CO的浓度 e.分离出二甲醚
(2)已知反应②2CH3OH(g) CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
①比较此时正、逆反应速率的大小:v(正)____ v(逆)(填“>”“<”或“=”)。
②若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH)=____ ;该时间内反应速率v(CH3OH)=____ 。
 CH3OCH3(二甲醚)(g)+CO2(g) ΔH<0达到平衡,要提高CO的转化率,可以采取的措施是
CH3OCH3(二甲醚)(g)+CO2(g) ΔH<0达到平衡,要提高CO的转化率,可以采取的措施是a.升高温度 b.加入催化剂 c.减小CO2的浓度 d.增加CO的浓度 e.分离出二甲醚
(2)已知反应②2CH3OH(g)
 CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)在某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
②若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.完成下列问题
(1)已知在448 ℃时,反应H2(g)+I2(g) 2HI(g) ΔH<0的平衡常数K1为25,则该温度下反应2HI(g)
2HI(g) ΔH<0的平衡常数K1为25,则该温度下反应2HI(g)  H2(g)+I2(g)的平衡常数K2为
H2(g)+I2(g)的平衡常数K2为_______ ;反应 H2(g)+
H2(g)+ I2(g)
I2(g)  HI(g)的平衡常数K3为
HI(g)的平衡常数K3为_______ 。
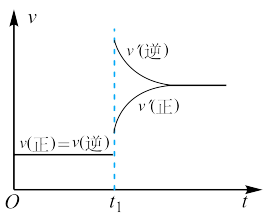
(2)在一密闭容器中发生上述反应,压缩容器体积,造成容器内压强增大,则下列说法中正确的是_______。
Ⅱ.在一定容积的密闭容器中,发生如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
回答下列问题:
(3)该反应的化学平衡常数表达式为K=_______ 。
(4)该反应为_______ 反应(填“吸热”或“放热”)。
(5)能判断该反应达到化学平衡状态的依据是_______。
(6)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),判断此时温度为_______ ℃。
(7)在800 ℃时,发生上述反应,某时刻测得容器内各物质的浓度分别为c(CO2)=2 mol/L、(H2)=1.5 mol/L、c(CO)=1 mol/L、c(H2O)=3 mol/L,则下一时刻,反应向_______ (填“正反应”或“逆反应”)方向进行。
(1)已知在448 ℃时,反应H2(g)+I2(g)
 2HI(g) ΔH<0的平衡常数K1为25,则该温度下反应2HI(g)
2HI(g) ΔH<0的平衡常数K1为25,则该温度下反应2HI(g)  H2(g)+I2(g)的平衡常数K2为
H2(g)+I2(g)的平衡常数K2为 H2(g)+
H2(g)+ I2(g)
I2(g)  HI(g)的平衡常数K3为
HI(g)的平衡常数K3为(2)在一密闭容器中发生上述反应,压缩容器体积,造成容器内压强增大,则下列说法中正确的是_______。

| A.容器内气体的颜色变深,混合气体的密度增大 |
| B.平衡不发生移动 |
| C.I2(g)的转化率不变,H2的平衡浓度不变 |
| D.改变条件前后,速率图像如图所示 |
Ⅱ.在一定容积的密闭容器中,发生如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(3)该反应的化学平衡常数表达式为K=
(4)该反应为
(5)能判断该反应达到化学平衡状态的依据是_______。
| A.容器中压强不变 | B.混合气体中c(CO)不变 |
| C.v(H2)正=v(H2O)逆 | D.c(CO2)=c(CO) |
(7)在800 ℃时,发生上述反应,某时刻测得容器内各物质的浓度分别为c(CO2)=2 mol/L、(H2)=1.5 mol/L、c(CO)=1 mol/L、c(H2O)=3 mol/L,则下一时刻,反应向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示:
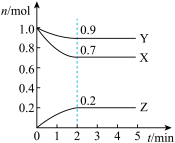
(1)由图中所给数据进行分析,该反应的化学方程式为__________ 。
(2)若上述反应中X、Y、Z分别为H2、N2、NH3,某温度下,在容积恒定为2.0L的密闭容器中充入2.0mol N2和2.0mol H2,一段时间后反应达平衡状态,实验数据如表所示:
0~50s内的平均反应速率v(N2)=__________ 。
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成1mol NH3过程中放出46kJ的热量。则N≡N的键能为_________ kJ/mol。

(1)由图中所给数据进行分析,该反应的化学方程式为
(2)若上述反应中X、Y、Z分别为H2、N2、NH3,某温度下,在容积恒定为2.0L的密闭容器中充入2.0mol N2和2.0mol H2,一段时间后反应达平衡状态,实验数据如表所示:
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(NH3) | 0 | 0.36 | 0.48 | 0.50 | 0.50 |
0~50s内的平均反应速率v(N2)=
(3)已知:键能指在标准状况下,将1mol气态分子AB(g)解离为气态原子A(g)、B(g)所需的能量,用符号E表示,单位为kJ/mol。H-H的键能为436kJ/mol,N-H的键能为391kJ/mol,生成1mol NH3过程中放出46kJ的热量。则N≡N的键能为
您最近一年使用:0次



