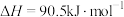在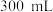 的密闭容器中,放入镍粉并充入
的密闭容器中,放入镍粉并充入 定量的CO气体,一定条件下发生反应:
定量的CO气体,一定条件下发生反应: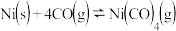 ,已知该反应平衡常数与温度的关系如表所示:下列说法正确的是
,已知该反应平衡常数与温度的关系如表所示:下列说法正确的是

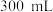 的密闭容器中,放入镍粉并充入
的密闭容器中,放入镍粉并充入 定量的CO气体,一定条件下发生反应:
定量的CO气体,一定条件下发生反应: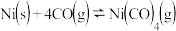 ,已知该反应平衡常数与温度的关系如表所示:下列说法正确的是
,已知该反应平衡常数与温度的关系如表所示:下列说法正确的是

温度 | 25 | 80 | 230 |
| 平衡常数 | 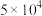 | 2 |  |
A.上述生成Ni 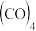 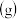 的反应为吸热反应 的反应为吸热反应 |
B. 时反应Ni 时反应Ni 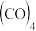 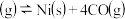 的平衡常数为 的平衡常数为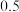 |
C.在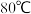 时,测得某时刻, 时,测得某时刻,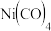 、CO浓度均 、CO浓度均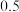  ,则此时 ,则此时 |
D.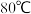 达到平衡时,测得 达到平衡时,测得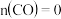 3 mol,则 3 mol,则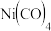 的平衡浓度为2 的平衡浓度为2  |
12-13高三上·浙江杭州·期中 查看更多[19]
(已下线)第七章 化学反应速率与化学平衡 第41练 化学平衡状态 化学平衡常数黑龙江省哈尔滨市第四中学校2022-2023学年高二上学期第一次月考化学试题天津市耀华中学2021-2022学年高二上学期期中考试化学试题江西省鄱阳县第一中学2019-2020学年高二上学期第二次检测化学试题河北省衡水市第十四中学2020-2021学年高二上学期三调考试(校内)化学试题福建师范大学第二附属中学2019-2020学年高二上学期期中考试化学(选考)试题鲁科版(2019)高二选择性必修第一册第2章 化学反应的方向、限度与速率 易错疑难集训(一)河北省沧州市盐山中学2019-2020学年高二上学期期末考试(B)化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理—— 化学平衡常数与浓度商的应用(提升练)福建省永安市第三中学2019-2020学年高二上学期第二次月考化学试题福建省漳平市第一中学2019-2020学年高二上学期第二次月考化学试题河北省张家口市第一中学2019-2020学年高二12月月考化学试题江西省南昌市新建县第一中学2019-2020学年高二上学期期中考试化学试题河北省张家口市第一中学2019-2020学年高二上学期期中考试(实验班)化学试题江西省上高县第二中学2017-2018学年高二上学期期末考试化学试题湖北省荆州中学2017-2018学年高二12月阶段性质量检测化学试题2016-2017学年河北冀州中学高二上第一次月考化学试卷(已下线)2014高考名师推荐化学化学平衡常数(已下线)2013届浙江省杭州市高三上学期期中七校联考化学试卷
更新时间:2020-02-07 14:15:31
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】小组同学探究盐溶液对反应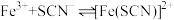 (血红色)的影响。将2mL0.01mol/LFeCl3的溶液与2mL0.02mol/L的KSCN溶液混合,分别加入等体积的试剂①~④,测得平衡后体系的透光率如下图所示。
(血红色)的影响。将2mL0.01mol/LFeCl3的溶液与2mL0.02mol/L的KSCN溶液混合,分别加入等体积的试剂①~④,测得平衡后体系的透光率如下图所示。
已知:ⅰ.溶液血红色越深,透光率越小,其它颜色对透光率的影响可忽略。
ⅱ. (黄色)
(黄色)
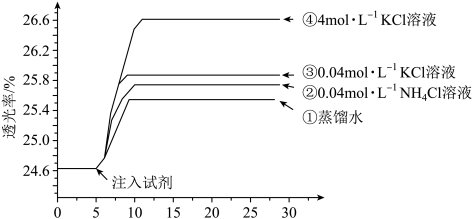
下列说法不正确的是
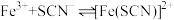 (血红色)的影响。将2mL0.01mol/LFeCl3的溶液与2mL0.02mol/L的KSCN溶液混合,分别加入等体积的试剂①~④,测得平衡后体系的透光率如下图所示。
(血红色)的影响。将2mL0.01mol/LFeCl3的溶液与2mL0.02mol/L的KSCN溶液混合,分别加入等体积的试剂①~④,测得平衡后体系的透光率如下图所示。已知:ⅰ.溶液血红色越深,透光率越小,其它颜色对透光率的影响可忽略。
ⅱ.
 (黄色)
(黄色)
下列说法不正确的是
A.注入试剂①后溶液透光率增大,一定是由于 平衡逆向移动引起的 平衡逆向移动引起的 |
| B.透光率③比②高,可能是阳离子种类或溶液pH导致的 |
C.透光率④比③高,可能发生了反应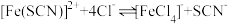 |
D.若要证明试剂③中Cl—对平衡体系有影响,还应使用与试剂③等体积的0.04mol/L的KNO3溶液进行对比实验(已知NO 对实验无影响) 对实验无影响) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】可逆反应2SO2(g)+O2(g)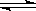 2SO3(g)从正方向开始,并达到了平衡,此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是
2SO3(g)从正方向开始,并达到了平衡,此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是
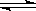 2SO3(g)从正方向开始,并达到了平衡,此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是
2SO3(g)从正方向开始,并达到了平衡,此时SO2和O2的物质的量之比为2∶1;若采取某种措施,导致SO2和O2又消耗了一些,并再次达到平衡,下列说法正确的是| A.新平衡体系中,SO2和O2物质的量之比仍为2∶1 |
| B.平衡向正反应方向移动,原因是正反应速率增大,逆反应速率减小 |
| C.新平衡体系与旧平衡体系比较,SO3的浓度肯定增大 |
| D.若采取的措施是缩小容器的容积,则新旧平衡中SO2和O2的转化率之比都是1∶1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】Al3+与F-具有很强的亲和性,当F-的浓度过大时,还会形成AlF 。AlF3在一定溶剂中存在分步电离,常温下向某浓度的AlF3溶液中加入NaF,实验测定Al3+、AlF2+、AlF
。AlF3在一定溶剂中存在分步电离,常温下向某浓度的AlF3溶液中加入NaF,实验测定Al3+、AlF2+、AlF 、AlF3在所有含铝元素微粒中的百分含量随pF[
、AlF3在所有含铝元素微粒中的百分含量随pF[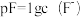 ]的变化如图所示,下列说法错误的是
]的变化如图所示,下列说法错误的是
 。AlF3在一定溶剂中存在分步电离,常温下向某浓度的AlF3溶液中加入NaF,实验测定Al3+、AlF2+、AlF
。AlF3在一定溶剂中存在分步电离,常温下向某浓度的AlF3溶液中加入NaF,实验测定Al3+、AlF2+、AlF 、AlF3在所有含铝元素微粒中的百分含量随pF[
、AlF3在所有含铝元素微粒中的百分含量随pF[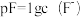 ]的变化如图所示,下列说法错误的是
]的变化如图所示,下列说法错误的是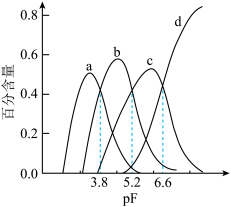
A.曲线b表示AlF |
B.pF=4时, |
C.Pf= 6.6时, 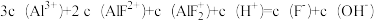 |
D.常温下, 的化学平衡常数为1015.6 的化学平衡常数为1015.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】甲胺(CH3NH2)是合成太阳能敏化剂的原料。一定温度下,在三个体积均为2.0 L的恒容密闭容器中按不同方式投入反应物,发生反应:CH3OH(g)+NH3(g) CH3NH2(g)+H2O(g),其中容器I中的反应在5min时达到平衡状态,下列说法正确的是
CH3NH2(g)+H2O(g),其中容器I中的反应在5min时达到平衡状态,下列说法正确的是
 CH3NH2(g)+H2O(g),其中容器I中的反应在5min时达到平衡状态,下列说法正确的是
CH3NH2(g)+H2O(g),其中容器I中的反应在5min时达到平衡状态,下列说法正确的是| 容器编号 | 温度/K | 起始物质的量(mol) | 平衡时物质的量(mol) | 平衡常数 | |||
| CH3OH(g) | NH3(g) | CH3NH2(g) | H2O(g) | CH3NH2(g) | |||
| Ⅰ | 530 | 0.40 | 0.40 | 0 | 0 | 0.30 | K1 |
| Ⅱ | 530 | 0.80 | 0.80 | 0 | 0 | K2 | |
| Ⅲ | 500 | 0 | 0 | 0.20 | 0.20 | 0.16 | K3 |
| A.容器I中前5min的平均反应速率v(CH3OH)=0.06 mol·L-1·min-1 |
| B.容器II达到平衡时,再通入0.1 mol NH3,达到平衡时CH3NH2的体积分数变大 |
| C.达到平衡时,转化率:αI(CH3OH)+αIII(CH3NH2)>1 |
| D.530K时,若起始向容器I中充入0.10 mol CH3OH、0.15 mol NH3、0.10 mol CH3NH2、0.10 mol H2O,则v正>v逆 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知 反应的平衡常数和温度的关系如下:
反应的平衡常数和温度的关系如下:
830℃时,向一个2L的密闭容器中充入0.2molA和0.8molB,反应初始4s内A的平均反应速率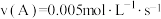 。下列说法正确的是
。下列说法正确的是
 反应的平衡常数和温度的关系如下:
反应的平衡常数和温度的关系如下:| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
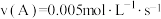 。下列说法正确的是
。下列说法正确的是A. 时 时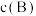 为 为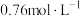 |
B.830℃时,若向另一个2L的密闭容器中充入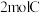 和 和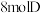 ,达平衡后该平衡混合物中C的体积分数与题干所述的830℃平衡混合物中A的体积分数相同 ,达平衡后该平衡混合物中C的体积分数与题干所述的830℃平衡混合物中A的体积分数相同 |
| C.反应达平衡后,升高温度,平衡正向移动 |
D.1200℃时反应达到平衡后再向密闭容器中充入 和 和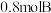 ,可提高反应物的转化率 ,可提高反应物的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某温度时,在体积为 2L 的恒容容器中发生反应, 2A(g) 2B(g) C(g) ΔH <0 ,起始时加入2 mol A 气体,测得 C 的物质的量随时间变化如表所示:
下列说法正确的是
t / min | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
C 物质的量/mol | 0 | 0.50 | 0.70 | 0.80 | 0.85 | 0.86 | 0.86 |
| A.当时间达到 60 min 时,反应恰好达到平衡状态 |
| B.在 20—30 min 内以 C 表示的反应速率为 0.005mol·L-1·min-1 |
| C.平衡时容器内压强为起始时容器内压强的 2.86 倍 |
| D.平衡时 A 的转化率为 43% |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在一定条件下,容积为2L的密闭容器中,将2molM气体和3molN气体混合,发生下列反应:2M(g)+3N(g) Q(g)+xR(g),该反应达到平衡时生成0.8molQ,并测得R浓度为1.6mol·L-1,下列叙述正确的是
Q(g)+xR(g),该反应达到平衡时生成0.8molQ,并测得R浓度为1.6mol·L-1,下列叙述正确的是
 Q(g)+xR(g),该反应达到平衡时生成0.8molQ,并测得R浓度为1.6mol·L-1,下列叙述正确的是
Q(g)+xR(g),该反应达到平衡时生成0.8molQ,并测得R浓度为1.6mol·L-1,下列叙述正确的是| A.x值为3 | B.容器内压强不变 |
| C.平衡时N的浓度为0.6mol/L | D.M的转化率为65% |
您最近一年使用:0次

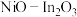 可协同催化
可协同催化 的氢化,体系中涉及以下两个反应:
的氢化,体系中涉及以下两个反应:
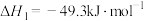


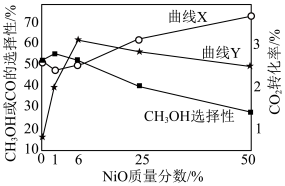
 以一定流速通过催化剂,在一定温度下反应,
以一定流速通过催化剂,在一定温度下反应, 或CO的选择性[
或CO的选择性[ ]与催化剂中NiO的质量分数的关系如图所示。下列说法正确的是
]与催化剂中NiO的质量分数的关系如图所示。下列说法正确的是