研究化学反应时,既要考虑物质变化与能量变化,也要关注反应的快慢与限度。回答下列问题:
I.现有反应:①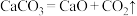 ,②
,②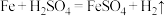 。
。
(1)两反应中属于吸热反应的是______  填序号
填序号 。
。
(2) 原电池的装置如图所示。
原电池的装置如图所示。

①溶液中 向
向______  填“铁”或“铜”
填“铁”或“铜” 电极方向移动。
电极方向移动。
②正极的现象是______ ,负极的电极反应式为______ 。
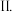 某可逆反应:
某可逆反应: 在3 种不同条件下进行,B和D的起始浓度均为0,反应物A 的浓度随反应时间的变化情况如下表:
在3 种不同条件下进行,B和D的起始浓度均为0,反应物A 的浓度随反应时间的变化情况如下表:
(3)实验1中,在 min内,以物质A表示的平均反应速率为
min内,以物质A表示的平均反应速率为______ 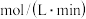 ,50min时,
,50min时,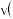 正
正
______  填“
填“ ”“
”“ ”或“
”或“ ”
”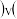 逆
逆 。
。
(4)0~20min内,实验2 比实验1的反应速率______  填“快”或“慢”
填“快”或“慢” ,其原因可能是
,其原因可能是______ 。
(5)实验3 比实验1的反应速率快,其原因是______ 。
I.现有反应:①
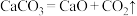 ,②
,②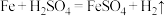 。
。(1)两反应中属于吸热反应的是
 填序号
填序号 。
。(2)
 原电池的装置如图所示。
原电池的装置如图所示。
①溶液中
 向
向 填“铁”或“铜”
填“铁”或“铜” 电极方向移动。
电极方向移动。②正极的现象是
 某可逆反应:
某可逆反应: 在3 种不同条件下进行,B和D的起始浓度均为0,反应物A 的浓度随反应时间的变化情况如下表:
在3 种不同条件下进行,B和D的起始浓度均为0,反应物A 的浓度随反应时间的变化情况如下表:| 实验序号 | 时间 浓度 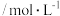 温度 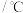 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 |  | 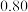 | 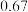 |  | 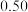 | 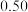 | 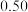 |
| 2 | 800 |  | 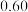 | 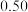 | 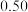 | 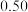 | 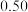 | 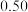 |
| 3 | 950 |  |  | 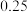 |  |  |  | 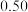 |
 min内,以物质A表示的平均反应速率为
min内,以物质A表示的平均反应速率为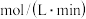 ,50min时,
,50min时,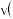 正
正
 填“
填“ ”“
”“ ”或“
”或“ ”
”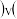 逆
逆 。
。(4)0~20min内,实验2 比实验1的反应速率
 填“快”或“慢”
填“快”或“慢” ,其原因可能是
,其原因可能是(5)实验3 比实验1的反应速率快,其原因是
更新时间:2020-02-26 10:44:32
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】甲醇(CH3OH)是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
反应I:CO2(g)+3H2(g) CH3OH(g)+H2O(g);
CH3OH(g)+H2O(g);
反应Ⅱ:CO2(g)+H2(g) CO(g)+H2O(g);
CO(g)+H2O(g);
反应Ⅲ:CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
回答下列问题:
(1)反应I进行的过程中体系内化学能减少,则反应I为______ (填“吸热”或“放热”)反应。
(2)已知反应Ⅱ为吸热反应,若反应Ⅱ在一绝热恒容密闭容器中进行,能说明反应已达到平衡状态的是______ (填字母)。
a.v(CO)=v(H2O)
b.温度不变
c.容器内CO2的体积分数保持不变
(3)250℃时,向体积为2L的恒容密闭容器中充入3molH2和1molCO2发生反应Ⅱ。经过5min达到平衡状态,平衡时测得CO2的转化率为50%。
①该温度下,反应开始至5min时,该反应的平均反应速率v(H2)=______ 。
②平衡时,H2的体积分数为_______ %,CO的物质的量浓度为______ mol•L-1。
(4)我国科学家研究Li-CO2电池,取得了重大科研成果。
①Li-CO2电池中,研究表明该电池反应产物为碳酸锂和单质碳,正极CO2电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ中CO2与CO 反应的离子方程式。
反应的离子方程式。
I.2CO2+2e-=C2O
Ⅱ.C2O =CO2+CO
=CO2+CO
Ⅲ._______
Ⅳ.CO +2Li+=Li2CO3
+2Li+=Li2CO3
②根据①中反应步骤,可以判断Li-CO2电池中,在负极参与反应的物质为_______ (填“Li”或“CO2”)。
反应I:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g);
CH3OH(g)+H2O(g);反应Ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g);
CO(g)+H2O(g);反应Ⅲ:CO(g)+2H2(g)
 CH3OH(g)。
CH3OH(g)。回答下列问题:
(1)反应I进行的过程中体系内化学能减少,则反应I为
(2)已知反应Ⅱ为吸热反应,若反应Ⅱ在一绝热恒容密闭容器中进行,能说明反应已达到平衡状态的是
a.v(CO)=v(H2O)
b.温度不变
c.容器内CO2的体积分数保持不变
(3)250℃时,向体积为2L的恒容密闭容器中充入3molH2和1molCO2发生反应Ⅱ。经过5min达到平衡状态,平衡时测得CO2的转化率为50%。
①该温度下,反应开始至5min时,该反应的平均反应速率v(H2)=
②平衡时,H2的体积分数为
(4)我国科学家研究Li-CO2电池,取得了重大科研成果。
①Li-CO2电池中,研究表明该电池反应产物为碳酸锂和单质碳,正极CO2电还原后与锂离子结合形成碳酸锂按以下4个步骤进行,写出步骤Ⅲ中CO2与CO
 反应的离子方程式。
反应的离子方程式。I.2CO2+2e-=C2O

Ⅱ.C2O
 =CO2+CO
=CO2+CO
Ⅲ.
Ⅳ.CO
 +2Li+=Li2CO3
+2Li+=Li2CO3②根据①中反应步骤,可以判断Li-CO2电池中,在负极参与反应的物质为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】化学反应中的能量变化,通常表现为热量的变化,研究化学反应中的热量变化具有重要的意义。
(1)下列变化属于吸热反应的是_____ (填序号)。
①液态水气化②胆矾加热变成白色粉末③浓硫酸稀释④氢气还原氧化铜
⑤盐酸和碳酸氢钠反应⑥氢氧化钾和稀硫酸反应⑦灼热的木炭与CO2的反应
⑧Ba(OH)2•8H2O晶体与NH4Cl晶体的反应⑨甲烷在空气中燃烧的反应
(2)已知:C(s)+O2(g)=CO2(g)ΔH1C(g)+O2(g)=CO2(g) ΔH2,则ΔH1_____ ΔH2(填“>”、“<”或“=”)。
(3)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=﹣196.6kJ•mol﹣1;在该条件下,将2molSO2(g)与1molO2(g)放入一密闭容器中充分反应,生成80gSO3(g),则放出的热量_____(填字母)。
2SO3(g) ΔH=﹣196.6kJ•mol﹣1;在该条件下,将2molSO2(g)与1molO2(g)放入一密闭容器中充分反应,生成80gSO3(g),则放出的热量_____(填字母)。
(4)在25℃、101kPa下,23g乙醇CH3CH2OH(l)完全燃烧生成CO2和液态水时放热638.4kJ。则表示乙醇燃烧的热化学方程式为_____ 。
(5)50mL0.50mol/L盐酸与50mL0.50mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。

①图中缺少的一种玻璃仪器是_____ 。
②若用相同浓度和体积的醋酸代替盐酸进行上述实验,测得的中和反应ΔH将_____ (填“偏大”、“偏小”或“无影响”)。
(1)下列变化属于吸热反应的是
①液态水气化②胆矾加热变成白色粉末③浓硫酸稀释④氢气还原氧化铜
⑤盐酸和碳酸氢钠反应⑥氢氧化钾和稀硫酸反应⑦灼热的木炭与CO2的反应
⑧Ba(OH)2•8H2O晶体与NH4Cl晶体的反应⑨甲烷在空气中燃烧的反应
(2)已知:C(s)+O2(g)=CO2(g)ΔH1C(g)+O2(g)=CO2(g) ΔH2,则ΔH1
(3)已知:2SO2(g)+O2(g)
 2SO3(g) ΔH=﹣196.6kJ•mol﹣1;在该条件下,将2molSO2(g)与1molO2(g)放入一密闭容器中充分反应,生成80gSO3(g),则放出的热量_____(填字母)。
2SO3(g) ΔH=﹣196.6kJ•mol﹣1;在该条件下,将2molSO2(g)与1molO2(g)放入一密闭容器中充分反应,生成80gSO3(g),则放出的热量_____(填字母)。| A.等于196.6kJ | B.98.3kJ~196.6kJ | C.等于98.3kJ | D.小于98.3kJ |
(5)50mL0.50mol/L盐酸与50mL0.50mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和反应的反应热。

①图中缺少的一种玻璃仪器是
②若用相同浓度和体积的醋酸代替盐酸进行上述实验,测得的中和反应ΔH将
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】在研究化学反应中的能量变化时,我们通常做下面的实验:在一个小烧杯里,加入20g已研磨成粉末的Ba(OH)2⋅8H2O,将小烧杯放在事先已滴有3∼4滴水的玻璃片上,然后向烧杯中加入约10gNH4Cl晶体,根据实验步骤,填写下表,并回答问题。

(4)写出实验过程中发生反应的化学方程式:______________________________ ;
(5)该反应在常温下就可进行,说明:____________________________________ 。

| 实验步骤 | 实验现象及结论 |
| 将晶体混合,立即快速搅拌 | 有刺激性气味能使湿润的紫色石蕊试纸变蓝的 |
| 用手摸烧杯下部 | 感觉烧杯变凉说明此反应是 |
| 用手拿起烧杯 | 烧杯下面的带有几滴水的玻璃片粘到了烧杯底部 |
| 将粘有玻璃片的烧杯放在盛有热水的烧杯上 | 玻璃片脱离上面烧杯底部 |
| 反应后移走多孔塑料片观察反应物 | 混合物成糊状,证明有 |
(5)该反应在常温下就可进行,说明:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】碘在科研与生活中有重要作用,某兴趣小组用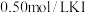 、0.2%淀粉溶液、
、0.2%淀粉溶液、 、
、 等试剂,探究反应条件对化学反应速率的影响。
等试剂,探究反应条件对化学反应速率的影响。
已知: (慢)
(慢)
 (快)
(快)
(1)向KI、 与淀粉的混合溶液中加入一定量的
与淀粉的混合溶液中加入一定量的 溶液,当溶液中的
溶液,当溶液中的___________ 耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色, 与
与 初始的体积
初始的体积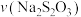 与
与 量需满足的关系为:
量需满足的关系为: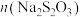
___________  (填“>”,“<”,“=”),出现蓝色之前,
(填“>”,“<”,“=”),出现蓝色之前, 在反应中起到的作用是
在反应中起到的作用是___________ 。
(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
①表中
___________ ,
___________ ,
___________ 。
②用 表示实验序号④的速率为
表示实验序号④的速率为___________ 。
(3)已知某条件下,浓度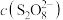 随反应时间t的变化曲线如图,若保持其它条件不变,图中分别画出降低反应温度和加入催化剂时
随反应时间t的变化曲线如图,若保持其它条件不变,图中分别画出降低反应温度和加入催化剂时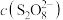 随反应时间t的变化曲线示意图(进行相应的标注)。
随反应时间t的变化曲线示意图(进行相应的标注)。_____

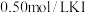 、0.2%淀粉溶液、
、0.2%淀粉溶液、 、
、 等试剂,探究反应条件对化学反应速率的影响。
等试剂,探究反应条件对化学反应速率的影响。已知:
 (慢)
(慢) (快)
(快)(1)向KI、
 与淀粉的混合溶液中加入一定量的
与淀粉的混合溶液中加入一定量的 溶液,当溶液中的
溶液,当溶液中的 与
与 初始的体积
初始的体积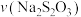 与
与 量需满足的关系为:
量需满足的关系为: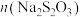
 (填“>”,“<”,“=”),出现蓝色之前,
(填“>”,“<”,“=”),出现蓝色之前, 在反应中起到的作用是
在反应中起到的作用是(2)为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验序号 | 体积V/mL | 出现蓝色的时间t/s | ||||
 溶液 溶液 | 水 | KI溶液 |  溶液 溶液 | 淀粉溶液 | ||
| ① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 | 10 |
| ② | 5.0 |  | 4.0 | 4.0 | 2.0 | 20 |
| ③ | 10.0 |  | 2.0 | 4.0 | 2.0 | 20 |
| ④ | 10.0 | 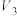 | 4.0 | 2.0 | 2.0 | 5 |



②用
 表示实验序号④的速率为
表示实验序号④的速率为(3)已知某条件下,浓度
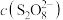 随反应时间t的变化曲线如图,若保持其它条件不变,图中分别画出降低反应温度和加入催化剂时
随反应时间t的变化曲线如图,若保持其它条件不变,图中分别画出降低反应温度和加入催化剂时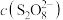 随反应时间t的变化曲线示意图(进行相应的标注)。
随反应时间t的变化曲线示意图(进行相应的标注)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】(一)某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
(1)写出草酸与高锰酸钾反应的离子方程式____________ 。
(2)通过实验A、B,可探究出________ (填外部因素)的改变对化学反应速率的影响,其中V1=_______ 、T1=______ ;通过实验______ (填实验序号)可探究出温度变化对化学反应速率的影响,其中V2=_____ 。
(3)忽略溶液体积的变化,利用实验B中数据计算,0-8s内,用KMnO4的浓度变化表示的反应速率v(KMnO4)=____ mol·L-1·min-1。
(二)为分析Fe3+和Cu2+对H2O2分解反应的催化效果,丙同学设计如下实验(三支试管中均盛有10 mL 5% H2O2):
(1)上表试管Ⅰ中应添加的试剂为5滴____________ 。
(2)结论是_________ ,实验Ⅲ的目的是__________ 。
| 实验 序号 | 实验 温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
| 酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
| V/mL | c/ mol·L-1 | V mL | c/ mol·L-1 | V/mL | |||
| A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
| C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(2)通过实验A、B,可探究出
(3)忽略溶液体积的变化,利用实验B中数据计算,0-8s内,用KMnO4的浓度变化表示的反应速率v(KMnO4)=
(二)为分析Fe3+和Cu2+对H2O2分解反应的催化效果,丙同学设计如下实验(三支试管中均盛有10 mL 5% H2O2):
| 试管 | Ⅰ | Ⅱ | Ⅲ |
| 滴加试剂 | 5滴_______ | 5滴0.1mol·L-1CuCl2 | 5滴0.3mol·L-1NaCl |
| 产生气泡情况 | 较快产生细小气泡 | 缓慢产生小气泡 | 无气泡产生 |
(2)结论是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某小组利用H2C2O4溶液和硫酸酸化的KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性KMnO4溶液褪色所需时间来判断反应的快慢。
该小组设计了如下方案。已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2 +8H2O
+8H2O
(1)表中V1=___ mL,V2=___ mL。
(2)探究温度对化学反应速率影响的实验编号是___ (填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是___ 。
(3)实验①测得KMnO4溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=___ mol·L-1·min-1。
该小组设计了如下方案。已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2
 +8H2O
+8H2O| 实验编号 | 0.1mol/L酸性 KMnO4溶液的体积/mL | 0.6mol/LH2C2O4溶液的体积 | H2O的 体积/mL | 实验温度/℃ | 溶液褪色所 需时间/min |
| ① | 10 | V1 | 35 | 25 | |
| ② | 10 | 10 | 30 | 25 | |
| ③ | 10 | 10 | V2 | 50 |
(2)探究温度对化学反应速率影响的实验编号是
(3)实验①测得KMnO4溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】结合所学内容,回答下列问题:
Ⅰ.某同学进行影响草酸与酸性高锰酸钾溶液反应速率因素的研究。草酸与酸性高锰酸钾的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。室温下,两支试管分别编号①和②,实验数据如下:
试管①中KMnO4溶液褪色的速率开始十分缓慢,一段时间后突然加快。
请回答:
(1)该实验结论是___________________________________________________________ 。
(2)实验②选用MnSO4固体而不是MnCl2固体的原因是____________________________ 。
(3)该同学为使实验更加严密,在试管③中做了如下实验,请预测褪色时间约为_____ 。
Ⅱ.滴定法是一种重要的定量分析方法,应用范围很广。某城市场上销售的一种食用精制盐包装袋上有如下部分说明:
已知:IO +5I-+6H+ = 3I2+3H2O,I2+2S2O
+5I-+6H+ = 3I2+3H2O,I2+2S2O = 2I-+S4O
= 2I-+S4O 某学生拟测定食用精制盐的碘含量,其步骤为
某学生拟测定食用精制盐的碘含量,其步骤为
a.准确称取W g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.加入指示剂,逐滴加入物质的量浓度为2.0×10-3 mol·L-1的Na2S2O3溶液10.0 mL,恰好反应完全
(4)c中加入的指示剂可选用_________ ,恰好完全反应时的现象是_______________ 。
(5)若操作b在空气中振荡时间过长,则最终测定的测定食用精制盐中的的碘含量会__________ (填“偏高”、“偏低”或“没有影响”)。
(6)根据以上实验和包装说明,算得所测食用精制盐的碘含量是(以含W的代数式表示)________ mg·kg-1(计算结果保留整数即可)。
Ⅰ.某同学进行影响草酸与酸性高锰酸钾溶液反应速率因素的研究。草酸与酸性高锰酸钾的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。室温下,两支试管分别编号①和②,实验数据如下:
| 实验序号 | ① | ② |
| 加入试剂 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 一粒黄豆粒大的MnSO4固体 |
| 褪色时间/s | 116 | 6 |
请回答:
(1)该实验结论是
(2)实验②选用MnSO4固体而不是MnCl2固体的原因是
(3)该同学为使实验更加严密,在试管③中做了如下实验,请预测褪色时间约为
| 实验序号 | ③ |
| 加入试剂 | 4 mL 0.01mol/L酸性 KMnO4溶液 2 mL 0.1mol/L H2C2O4溶液 一粒黄豆粒大的Na2SO4固体 |
| 褪色时间/s |
| 产品等级 | 一级 |
| 配料 | 食盐、碘酸钾(KIO3)、抗结剂 |
| 碘含量(以I计) | 20~50 mg·kg-1 |
 +5I-+6H+ = 3I2+3H2O,I2+2S2O
+5I-+6H+ = 3I2+3H2O,I2+2S2O = 2I-+S4O
= 2I-+S4O 某学生拟测定食用精制盐的碘含量,其步骤为
某学生拟测定食用精制盐的碘含量,其步骤为a.准确称取W g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.加入指示剂,逐滴加入物质的量浓度为2.0×10-3 mol·L-1的Na2S2O3溶液10.0 mL,恰好反应完全
(4)c中加入的指示剂可选用
(5)若操作b在空气中振荡时间过长,则最终测定的测定食用精制盐中的的碘含量会
(6)根据以上实验和包装说明,算得所测食用精制盐的碘含量是(以含W的代数式表示)
您最近一年使用:0次
【推荐2】汽车尾气中含有CO、NO、NO2、碳氢化合物等多种污染物。回答下列问题:
(1)汽车燃料中不含氮元素,尾气中所含NO产生的原因是__ 。
(2)已知:2C8H18(1)+25O2(g)=16CO2(g)+18H2O(g) △H1=-10244kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2
2NO(g)+2CO(g)=N2(g)+2CO2(g) △H3=-746kJ·mol-1
①若H2O(1)=H2O(g) △H=+44kJ·mol-1,则表示辛烷燃烧热的热化学方程式为__ 。
②部分化学键键能数据如下:
△H2=___ kJ·mol-1
(3)1573K时,N2+O2 2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为
2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为__ mol,N2的转化率为__ 。
(4)反应NO(g)+CO(g)=N2(g)+CO2(g)的平衡常数为1.68×1060,从热力学角度看,该反应程度应该很大,实际汽车尾气中该反应的程度很小,原因是__ ,要增大汽车尾气净化装置中单位时间内该反应的程度,关键是要___ 。
(1)汽车燃料中不含氮元素,尾气中所含NO产生的原因是
(2)已知:2C8H18(1)+25O2(g)=16CO2(g)+18H2O(g) △H1=-10244kJ·mol-1
N2(g)+O2(g)=2NO(g) △H2
2NO(g)+2CO(g)=N2(g)+2CO2(g) △H3=-746kJ·mol-1
①若H2O(1)=H2O(g) △H=+44kJ·mol-1,则表示辛烷燃烧热的热化学方程式为
②部分化学键键能数据如下:
| 化学键 | O=O | C=O | C O O |
E/(kJ·mol ) ) | 494 | 799 | 1076 |
△H2=
(3)1573K时,N2+O2
 2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为
2NO平衡常数为2.0×10-6,若测得内燃机内平衡混合气中氮气、氧气的物质的量分别为0.2mol、0.001mol,则生成NO的物质的量为(4)反应NO(g)+CO(g)=N2(g)+CO2(g)的平衡常数为1.68×1060,从热力学角度看,该反应程度应该很大,实际汽车尾气中该反应的程度很小,原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】按要求完成下列方程式的书写:
(1)在实验室配制 溶液时,常滴加几滴
溶液时,常滴加几滴 溶液,试用离子方程式说明原因:
溶液,试用离子方程式说明原因:____ 。
(2)汽车发动机工作时会引发 和
和 反应,其能量变化示意图如下(常温常压下测定):
反应,其能量变化示意图如下(常温常压下测定):
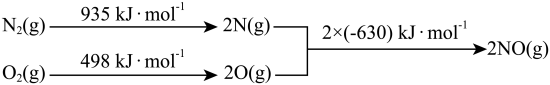
写出该反应的热化学方程式:_______________________ 。
(3)已知:常温下, 的电离常数
的电离常数 ;
; 的电离常数
的电离常数 ,
,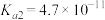 。向
。向 溶液中通入少量
溶液中通入少量 气体,则发生反应的离子方程式为
气体,则发生反应的离子方程式为_____________ 。
(4)用电解法处理含铬废水(主要成分 )时,以铁板作阴、阳极,处理过程中在电解质溶液中发生反应:
)时,以铁板作阴、阳极,处理过程中在电解质溶液中发生反应: ,最后
,最后 以
以 形式除去,则阳极的电极反应式为
形式除去,则阳极的电极反应式为_______________________ 。
(5)我国学者结合实验与计算机模拟结果,研究了丙烷在六方氮化硼催化剂表面氧化脱氢制丙烯的反应历程,部分历程如图所示,其中吸附在催化剂表面的物种用 标注。
标注。
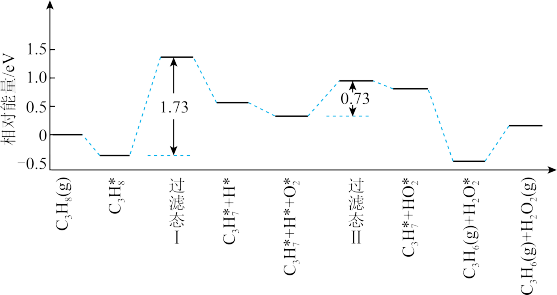
该历程中决速步骤对应的化学方程式为_______________________ 。
(1)在实验室配制
 溶液时,常滴加几滴
溶液时,常滴加几滴 溶液,试用离子方程式说明原因:
溶液,试用离子方程式说明原因:(2)汽车发动机工作时会引发
 和
和 反应,其能量变化示意图如下(常温常压下测定):
反应,其能量变化示意图如下(常温常压下测定):
写出该反应的热化学方程式:
(3)已知:常温下,
 的电离常数
的电离常数 ;
; 的电离常数
的电离常数 ,
,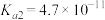 。向
。向 溶液中通入少量
溶液中通入少量 气体,则发生反应的离子方程式为
气体,则发生反应的离子方程式为(4)用电解法处理含铬废水(主要成分
 )时,以铁板作阴、阳极,处理过程中在电解质溶液中发生反应:
)时,以铁板作阴、阳极,处理过程中在电解质溶液中发生反应: ,最后
,最后 以
以 形式除去,则阳极的电极反应式为
形式除去,则阳极的电极反应式为(5)我国学者结合实验与计算机模拟结果,研究了丙烷在六方氮化硼催化剂表面氧化脱氢制丙烯的反应历程,部分历程如图所示,其中吸附在催化剂表面的物种用
 标注。
标注。
该历程中决速步骤对应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】化学反应过程既有物质变化也有能量变化。
Ⅰ.关于工业合成氨的反应,已知H-H键、N-H键、N≡N键的键能分别为436 、391
、391 、946
、946 。请根据键能的数据判断下列问题。
。请根据键能的数据判断下列问题。
(1)由 和
和 合成氨时,需要
合成氨时,需要_____________ (填“吸收”或“放出”)能量,写出该反应的热化学方程式_________________ 。
Ⅱ.原电池是化学能转化为电能的装置。
(2)肼(液态)—过氧化氢碱性燃料电池由于其较高的能量密度而备受关注,其工作原理如图。_______ (填“氧化反应”或“还原反应”),电池工作过程中, 向极移动
向极移动_________ (填“A”或“B”);
②该燃料电池的总反应方程式可表示为__________ 。在标准状况下,若A极区产生11.2L  ,则外电路中理论上通过的电子的物质的量是
,则外电路中理论上通过的电子的物质的量是__________ mol。
Ⅲ.某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:_____________ 。
(4)反应开始至2min,以气体X表示的平均反应速率为___________ 。
(5)下列措施能增大反应速率的是_________ 。
A.升高温度 B.加入高效催化剂
C.持容器压强不变,充入一定量氦气 D.保持容器容积不变,充入气体X
E.保持容器容积不变,充入一定量氦气
(6)能说明上述反应达到平衡状态的是 。(填字母)
Ⅰ.关于工业合成氨的反应,已知H-H键、N-H键、N≡N键的键能分别为436
 、391
、391 、946
、946 。请根据键能的数据判断下列问题。
。请根据键能的数据判断下列问题。(1)由
 和
和 合成氨时,需要
合成氨时,需要Ⅱ.原电池是化学能转化为电能的装置。
(2)肼(液态)—过氧化氢碱性燃料电池由于其较高的能量密度而备受关注,其工作原理如图。
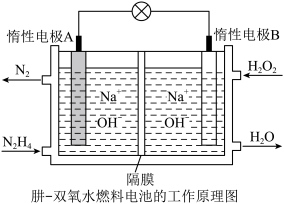
 向极移动
向极移动②该燃料电池的总反应方程式可表示为
 ,则外电路中理论上通过的电子的物质的量是
,则外电路中理论上通过的电子的物质的量是Ⅲ.某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
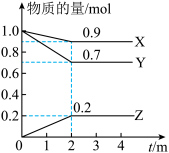
(4)反应开始至2min,以气体X表示的平均反应速率为
(5)下列措施能增大反应速率的是
A.升高温度 B.加入高效催化剂
C.持容器压强不变,充入一定量氦气 D.保持容器容积不变,充入气体X
E.保持容器容积不变,充入一定量氦气
(6)能说明上述反应达到平衡状态的是 。(填字母)
| A.混合气体的压强不随时间的变化而变化 | B. |
| C.X体积分数保持不变 | D.混合气体的密度不随时间的变化而变化 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
(1)工业合成氨是人类科学技术的一项重大突破。迄今为止,人类仍然在追求低成本、高产率的合成氨技术。 ,
,
 ,那么常温下,合成氨反应
,那么常温下,合成氨反应_______ (填“能”或“不能”)自发进行
(2)若将1.0molN2(g)和3.0molH2(g)通入体积为2L的密闭容器中,分别在T1和T2温度下进行反应。曲线A表示T2温度下n(H2)的变化,曲线B表示T1温度下n(NH3)的变化,T2温度下反应到a点恰好达到平衡。_______ (填“>”、“<”或“=”,下同)T2.T1温度下恰好平衡时,曲线B上的点为b(m,n),则m_______ 14,n_______ 1。
②T2温度下,若某时刻容器内气体的压强为起始时的70%,则此时v(正)_______ (填“>”、“<”或“=”)v(逆)。计算T2温度下,Kc=_______ 。
(3)常温下,Hg2+与Cl-的配合物存在如下平衡: ,含Hg微粒的分布系数δ与lgc(Cl-)的关系如下图所示:
,含Hg微粒的分布系数δ与lgc(Cl-)的关系如下图所示:
图中能代表HgCl 和HgCl+曲线分别是
和HgCl+曲线分别是_______ 和_______ (填字母),曲线A和曲线C交点的横坐标为_______ 。
(4)羟基自由基(·OH)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种将苯酚氧化为CO2和H2O的原电池-电解池组合装置,以实现发电、环保二位一体。_______ 。
(1)工业合成氨是人类科学技术的一项重大突破。迄今为止,人类仍然在追求低成本、高产率的合成氨技术。
 ,
,
 ,那么常温下,合成氨反应
,那么常温下,合成氨反应(2)若将1.0molN2(g)和3.0molH2(g)通入体积为2L的密闭容器中,分别在T1和T2温度下进行反应。曲线A表示T2温度下n(H2)的变化,曲线B表示T1温度下n(NH3)的变化,T2温度下反应到a点恰好达到平衡。

②T2温度下,若某时刻容器内气体的压强为起始时的70%,则此时v(正)
(3)常温下,Hg2+与Cl-的配合物存在如下平衡:
 ,含Hg微粒的分布系数δ与lgc(Cl-)的关系如下图所示:
,含Hg微粒的分布系数δ与lgc(Cl-)的关系如下图所示:

图中能代表HgCl
 和HgCl+曲线分别是
和HgCl+曲线分别是(4)羟基自由基(·OH)是自然界中氧化性仅次于氟的氧化剂。我国科学家设计了一种将苯酚氧化为CO2和H2O的原电池-电解池组合装置,以实现发电、环保二位一体。

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】在我国南海、东海海底均存在大量的可燃冰(天然气水合物,可表示为 )。
)。
2017年5月,中国首次海域可燃冰试采成功。2017年11月3日,国务院正式批准将可燃冰列为新矿种。可燃冰的开采和利用,既有助于解决人类面临的能源危机,又能生成一系列的工业产品。
(1)对某可燃冰矿样进行定量分析,取一定量样品,释放出的甲烷气体体积折合成标准状况后为166 m3,剩余 H2O 的体积为0.8m3,则该样品的化学式中 x=_________________ 。
(2)已知下表数据,且知 H2O(l)=H2O(g) △H=+41
用甲烷燃烧热表示的热化学方程式为_____________________________________________________ 。
(3)甲烷燃料电池相较于直接燃烧甲烷有着更高的能量转化效率,某甲烷燃料电池,正极通入空气,以某种金属氧化物为离子导体(金属离子空穴中能传导 O2-),该电池负极的电极反应式为__________________________________________ 。
(4)甲烷与水蒸气重整制氢是工业上获得氢气的重要手段。若甲烷与脱盐水在一定条件下反应生成H2,同时得到体积比为1:3的CO2和CO,该反应的化学方程式为_____________________________________ 。混合气体中的CO2可用浓氨水脱除,同时获得氮肥NH4HCO3,该反应的离子方程式是_________________________________________________________ 。
 )。
)。2017年5月,中国首次海域可燃冰试采成功。2017年11月3日,国务院正式批准将可燃冰列为新矿种。可燃冰的开采和利用,既有助于解决人类面临的能源危机,又能生成一系列的工业产品。
(1)对某可燃冰矿样进行定量分析,取一定量样品,释放出的甲烷气体体积折合成标准状况后为166 m3,剩余 H2O 的体积为0.8m3,则该样品的化学式中 x=
(2)已知下表数据,且知 H2O(l)=H2O(g) △H=+41

| 化学键 | C—H | O=O | C=O | H—O |
键能/  | 413 | 498 | 803 | 463 |
用甲烷燃烧热表示的热化学方程式为
(3)甲烷燃料电池相较于直接燃烧甲烷有着更高的能量转化效率,某甲烷燃料电池,正极通入空气,以某种金属氧化物为离子导体(金属离子空穴中能传导 O2-),该电池负极的电极反应式为
(4)甲烷与水蒸气重整制氢是工业上获得氢气的重要手段。若甲烷与脱盐水在一定条件下反应生成H2,同时得到体积比为1:3的CO2和CO,该反应的化学方程式为
您最近一年使用:0次



