亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下:
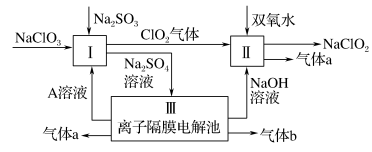
(1)Ⅰ中发生反应的还原剂是____ (填化学式)。
(2)Ⅱ中反应的离子方程式是____ 。
(3)Ⅲ中离子隔膜电解池的装置如下:
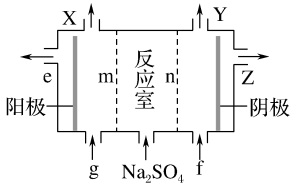
①A的化学式是________ ,A在____ 口产生。
②m为____ (填“阴”或“阳”)离子交换膜。
③结合化学用语和文字说明解释NaOH产生的原因:________
(4)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O
①该反应中氧化剂和还原剂的物质的量之比是____ 。
②研究表明:若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大,运用氧化还原反应规律分析其原因是____ 。
(5)NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量前者____ (填“>”“<”或“=”)后者。

(1)Ⅰ中发生反应的还原剂是
(2)Ⅱ中反应的离子方程式是
(3)Ⅲ中离子隔膜电解池的装置如下:

①A的化学式是
②m为
③结合化学用语和文字说明解释NaOH产生的原因:
(4)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O
①该反应中氧化剂和还原剂的物质的量之比是
②研究表明:若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大,运用氧化还原反应规律分析其原因是
(5)NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量前者
17-18高三上·北京·期中 查看更多[4]
(已下线)北京市海淀区2022届高三一模(原理综合题)(已下线)模拟卷08-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)云南省大姚实验中学2020届高三3月线上模拟理综化学试题(已下线)北京四中2018届上学期高三年级期中考试化学试卷
更新时间:2020-03-15 20:13:31
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】亚硝酸钠(NaNO2)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生Na2O、N2和O2,其水溶液呈碱性,能与AgNO3溶液反应生成难溶于水、易溶于酸的AgNO2。由于NaNO2有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____NO +_____I-+______=____NO↑+_____I2+_____H2O。
+_____I-+______=____NO↑+_____I2+_____H2O。
(1)请完成该离子方程式并配平_______ 。
(2)从物质分类角度来看,NaNO2是_______ (填字母代号)。
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是_______ 。从环保角度来讲,要将NaNO2转化为氮气,所用物质的_______ (填“氧化性”或“还原性”)应该比KI更______ (填“强”或“弱”)。
(4)下列方法不能用来区分固体NaNO2和NaCl的是______ (填序号)。
(5)误食NaNO2会导致人体血红蛋白中的Fe2+转化为Fe3+而中毒,该过程中NaNO2表现出的性质与下列_______ (填序号)反应中H2O2表现出的性质相同。
A.2H2O2 2H2O+O2↑
2H2O+O2↑
B.H2O2+Cl2=2HCl+O2↑
C.H2O2+H2SO4+2KI=2H2O+I2+K2SO4
(6)S2O 可以与Fe2+反应制备Fe2O3纳米颗粒。若S2O
可以与Fe2+反应制备Fe2O3纳米颗粒。若S2O 与Fe2+的系数之比为1:2,配平该反应的离子方程式:_______Fe2++_______S2O
与Fe2+的系数之比为1:2,配平该反应的离子方程式:_______Fe2++_______S2O +_______H2O2+_______OH-=_______Fe2O3+_______S2O
+_______H2O2+_______OH-=_______Fe2O3+_______S2O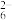 +_______H2O。
+_______H2O。_______
 +_____I-+______=____NO↑+_____I2+_____H2O。
+_____I-+______=____NO↑+_____I2+_____H2O。(1)请完成该离子方程式并配平
(2)从物质分类角度来看,NaNO2是
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是
(4)下列方法不能用来区分固体NaNO2和NaCl的是
| A.分别溶于水,滴加酚酞试液 | B.分别溶于水并滴加HNO3酸化的AgNO3溶液 |
| C.分别加强热并收集气体检验 | D.用筷子分别蘸取固体品尝味道 |
A.2H2O2
 2H2O+O2↑
2H2O+O2↑B.H2O2+Cl2=2HCl+O2↑
C.H2O2+H2SO4+2KI=2H2O+I2+K2SO4
(6)S2O
 可以与Fe2+反应制备Fe2O3纳米颗粒。若S2O
可以与Fe2+反应制备Fe2O3纳米颗粒。若S2O 与Fe2+的系数之比为1:2,配平该反应的离子方程式:_______Fe2++_______S2O
与Fe2+的系数之比为1:2,配平该反应的离子方程式:_______Fe2++_______S2O +_______H2O2+_______OH-=_______Fe2O3+_______S2O
+_______H2O2+_______OH-=_______Fe2O3+_______S2O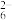 +_______H2O。
+_______H2O。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题。
(1) 物质
物质 中含有的分子数为
中含有的分子数为 ,则
,则 的摩尔质量为
的摩尔质量为___________ 。
(2)已知 具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下
具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下 和
和 反应的化学方程式:
反应的化学方程式:___________ 。
(3)某同学写出以下三个化学方程式(未配平),其中一定不可能实现的是___________ (填序号)。
①
②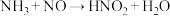
③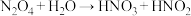
(4)写出下列物质溶于水时的电离方程式。
硝酸钾:___________ ;
硫酸氢钾:___________ ;
碳酸氢钠:___________ 。
(1)
 物质
物质 中含有的分子数为
中含有的分子数为 ,则
,则 的摩尔质量为
的摩尔质量为(2)已知
 具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下
具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下 和
和 反应的化学方程式:
反应的化学方程式:(3)某同学写出以下三个化学方程式(未配平),其中一定不可能实现的是
①

②
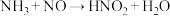
③
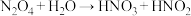
(4)写出下列物质溶于水时的电离方程式。
硝酸钾:
硫酸氢钾:
碳酸氢钠:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】海洋是一个巨大的化学资源宝库,而溴又被称为“海洋元素”。以海水为原料制备溴的工艺流程如图所示,请回答下列问题。
(1)海水晒盐所得的粗盐的主要成分为NaCl,还含有少量的 、
、 和
和 。将粗盐溶于水后,依次加入
。将粗盐溶于水后,依次加入__________ (填标号)后,过滤,往滤液中加入稍过量的稀盐酸,充分反应后加热除去HCl,获得精盐水。若过滤所得的滤液比较浑浊,原因可能是__________ 。
a.NaOH溶液、 溶液、
溶液、 溶液
溶液
b. 溶液、KOH溶液、
溶液、KOH溶液、 溶液
溶液
c. 溶液、
溶液、 溶液、NaOH溶液
溶液、NaOH溶液
d.KOH溶液、 溶液、
溶液、 溶液
溶液
(2)氯碱工业通过电解饱和食盐水制得烧碱、氢气和氯气,该反应的化学方程式为__________ ;步骤Ⅱ中反应的离子方程式为__________ 。
(3)往5mL溴水中,加入1mL四氯化碳,振荡、静置后,试管中的现象是__________ (填标号);往2mL淀粉碘化钾溶液中,滴加几滴溴水,观察到的现象为__________ 。
(4)下列有关说法正确的是__________(填标号)。
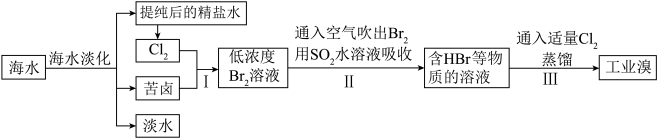
(1)海水晒盐所得的粗盐的主要成分为NaCl,还含有少量的
 、
、 和
和 。将粗盐溶于水后,依次加入
。将粗盐溶于水后,依次加入a.NaOH溶液、
 溶液、
溶液、 溶液
溶液b.
 溶液、KOH溶液、
溶液、KOH溶液、 溶液
溶液c.
 溶液、
溶液、 溶液、NaOH溶液
溶液、NaOH溶液d.KOH溶液、
 溶液、
溶液、 溶液
溶液(2)氯碱工业通过电解饱和食盐水制得烧碱、氢气和氯气,该反应的化学方程式为
(3)往5mL溴水中,加入1mL四氯化碳,振荡、静置后,试管中的现象是
A. B.
B. C.
C. D.
D.
(4)下列有关说法正确的是__________(填标号)。
| A.步骤Ⅰ、Ⅱ的目的是富集溴元素 |
| B.精盐水中分散质的粒子直径介于1~100nm |
C.非金属性: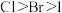 |
| D.实验室常将溴单质保存在带有橡胶塞的棕色广口瓶中,并加少量水水封 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据反应8NH3+3Cl2=6NH4Cl+N2,回答下列问题:
(1)氧化剂_____ ,还原剂_____ ;
(2)反应中转移电子数是_____ ;
(3)氧化剂与氧化产物的质量比_____ ;
(4)当生成2.8gN2时,被氧化的物质的质量是____ g。
(1)氧化剂
(2)反应中转移电子数是
(3)氧化剂与氧化产物的质量比
(4)当生成2.8gN2时,被氧化的物质的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氮元素及其化合物的转化关系如图所示,回答下列问题:

(1)Z的化学式为_______ 。
(2)若将等物质的量的X、Y通入NaOH溶液中,可获得NaNO2,写出该反应的离子方程式:_______ 。
(3)在一定条件下,氨气可与X反应.生成N2和H2O,每生成7 g N2,反应中转移的电子的物质的量为_______ mol。实验室常用NH4Cl与Ca(OH)2制取氨气,该反应的化学方程式为_______ 。欲收集纯净干燥的氨气,下列试剂可用于干燥NH3的是_______ (填标号)。
A.浓硫酸 B.碱石灰 C. NaOH固体 D. CaCl2固体
(4)工业生产中利用氨水吸收SO2和Y,原理如图所示。

“混合吸收”过程中发生反应的化学方程式为_______ ,若获得的铵盐只有一种溶质,写出此溶质的化学式_______ ,则Y被吸收过程中氧化剂和还原剂的物质的量之比为_______ 。

(1)Z的化学式为
(2)若将等物质的量的X、Y通入NaOH溶液中,可获得NaNO2,写出该反应的离子方程式:
(3)在一定条件下,氨气可与X反应.生成N2和H2O,每生成7 g N2,反应中转移的电子的物质的量为
A.浓硫酸 B.碱石灰 C. NaOH固体 D. CaCl2固体
(4)工业生产中利用氨水吸收SO2和Y,原理如图所示。

“混合吸收”过程中发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】含氯物质在日常生活中具有许多重要用途,回答下列问题:
(1)亚氯酸钠( )较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的两种产物可能为___________。
)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的两种产物可能为___________。
(2)我国用 替代氯气进行消毒,工业上常利用反应
替代氯气进行消毒,工业上常利用反应 制备
制备 ,用单线桥法表示反应中电子得失的方向和数目:
,用单线桥法表示反应中电子得失的方向和数目:___________ 。将该反应化学方程式改写为离子方程式:___________ 。
(3)工业上可利用 制备亚氯酸钠(
制备亚氯酸钠( ),反应体系中涉及下列6种物质:
),反应体系中涉及下列6种物质: 、
、 、
、 、NaOH、
、NaOH、 、
、 ,写出反应的化学方程式:
,写出反应的化学方程式:___________ 。
(4)某温度下降 通入KOH溶液里,反应后得到KCl、KClO、
通入KOH溶液里,反应后得到KCl、KClO、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为11:1,则
的个数之比为11:1,则 与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为___________ 。
(5)实验室用下列方法均可制取氯气
① ③
③
② ②
②
③ ④
④
若各反应转移的电子数相同,①②③生成的氯气质量比为___________ 。
(1)亚氯酸钠(
 )较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的两种产物可能为___________。
)较稳定,但加热或敲击亚氯酸钠固体时立即爆炸,爆炸后的两种产物可能为___________。A.NaCl、 | B.NaCl、NaClO |
C. 、 、 | D.NaCl、 |
 替代氯气进行消毒,工业上常利用反应
替代氯气进行消毒,工业上常利用反应 制备
制备 ,用单线桥法表示反应中电子得失的方向和数目:
,用单线桥法表示反应中电子得失的方向和数目:(3)工业上可利用
 制备亚氯酸钠(
制备亚氯酸钠( ),反应体系中涉及下列6种物质:
),反应体系中涉及下列6种物质: 、
、 、
、 、NaOH、
、NaOH、 、
、 ,写出反应的化学方程式:
,写出反应的化学方程式:(4)某温度下降
 通入KOH溶液里,反应后得到KCl、KClO、
通入KOH溶液里,反应后得到KCl、KClO、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为11:1,则
的个数之比为11:1,则 与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为(5)实验室用下列方法均可制取氯气
①
 ③
③②
 ②
②③
 ④
④若各反应转移的电子数相同,①②③生成的氯气质量比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知装置E为电解池,认真观察下列装置,回答下列问题:

(1)装置D为_______ (填“原电池”“电解池”或“电镀池”),装置C中Pb上发生的电极反应方程式为_______ 。
(2)装置A中Pt电极的名称为_______ (填“正极”“负极”“阴极”或“阳极”),装置A总反应的离子方程式为_______ 。
(3)若装置E中的目的是在Cu材料上镀银,则X为_______ (填化学式,下同),极板N的材料为_______ 。
(4)当装置B中PbO2电极质量改变12.8g时,装置D中阳极产生气体有_______ (填化学式),它们的总物质的量为_______ 。

(1)装置D为
(2)装置A中Pt电极的名称为
(3)若装置E中的目的是在Cu材料上镀银,则X为
(4)当装置B中PbO2电极质量改变12.8g时,装置D中阳极产生气体有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的KI溶液、足量的CuSO4溶液和K2SO4溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙中c电极质量增加32 g。据此回答问题:

(1)电源的N端为_________ 极;
(2)电极b上发生的电极反应为______________________________________ ;
(3)电极f上生成的气体在标准状况下的体积______________ ;
(4)电解开始时,在甲烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是____________________ ;
(5)电解前后溶液的pH变化情况,(填增大、减小或不变)甲溶液__________ ;乙溶液____________ 。

(1)电源的N端为
(2)电极b上发生的电极反应为
(3)电极f上生成的气体在标准状况下的体积
(4)电解开始时,在甲烧杯的中央,滴几滴淀粉溶液,你能观察到的现象是
(5)电解前后溶液的pH变化情况,(填增大、减小或不变)甲溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)以NiSO4溶液为电解质溶液进行粗镍(含Fe、Zn、Cu、Pt、Au等杂质)的电解精炼,下列说法正确的是_______(填代号)。(已知氧化性:Fe2+<Ni2+<Cu2+)
(2)如图回答问题:

①甲池A电极的电极反应式为_______ 。
②丙池总反应的化学方程式为_______ 。
③当乙池中C极质量减轻4.32 g时,甲池中B电极理论上消耗O2的体积为_______ mL(标准状况)。
④一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是_______ (填字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O=Na2FeO4+3H2↑,则电解时阳极的电极反应式是_______ 。
(4)合成甲醇工厂的酸性废水中含有甲醇(CH3OH),常用向废液中加入硫酸钴,再用微生物电池(葡萄糖C6H12O6酸性燃料电池)电解,电解时Co2+被氧化成Co3+,Co3+把水中的甲醇氧化成CO2,达到除去甲醇的目的。工作原理如下图(c为隔膜,甲醇不能通过,其它离子和水可以自由通过)。

① 电极的名称为
电极的名称为_______ 。
②写出除去甲醇的离子方程式_______ 。
(1)以NiSO4溶液为电解质溶液进行粗镍(含Fe、Zn、Cu、Pt、Au等杂质)的电解精炼,下列说法正确的是_______(填代号)。(已知氧化性:Fe2+<Ni2+<Cu2+)
| A.电解过程中,化学能转化为电能 |
| B.粗镍作阳极,发生还原反应 |
| C.利用阳极泥可回收Cu、Pt、Au等金属 |
| D.粗镍精炼时通过的电量与阴极析出镍的质量成正比 |

①甲池A电极的电极反应式为
②丙池总反应的化学方程式为
③当乙池中C极质量减轻4.32 g时,甲池中B电极理论上消耗O2的体积为
④一段时间后,断开电键K。下列物质能使乙池恢复到反应前浓度的是
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。高铁酸钠生产方法之一是电解法,其原理为Fe+2NaOH+2H2O=Na2FeO4+3H2↑,则电解时阳极的电极反应式是
(4)合成甲醇工厂的酸性废水中含有甲醇(CH3OH),常用向废液中加入硫酸钴,再用微生物电池(葡萄糖C6H12O6酸性燃料电池)电解,电解时Co2+被氧化成Co3+,Co3+把水中的甲醇氧化成CO2,达到除去甲醇的目的。工作原理如下图(c为隔膜,甲醇不能通过,其它离子和水可以自由通过)。

①
 电极的名称为
电极的名称为②写出除去甲醇的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铁、铝等金属单质及其化合物在生产和生活中有着广泛的应用。
(1)金属冶炼与处理常涉及氧化还原反应,由下列物质冶炼相应金属单质时采用电解法的是_________ 。
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述_______ (填装置序号)装置原理进行防护;装置③中总反应的离子方程式为______________________________________________ 。
(3)利用甲醇(CH3OH)、氧气组成燃料电池,电解质溶液为碱性,电池工作时负极反应式为_____________ 。
(4)氨气也可作为燃料电池的燃料源制成高效率无污染的燃料电池系统,总反应式为: (未配平),写出此碱性燃料电池的负极反应式:
(未配平),写出此碱性燃料电池的负极反应式:_______ 。
(5)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为_________________________ 。
(6)科学家制造出一种使用固体电解质的燃料电池,其效率高无污染,多用于航天航空。如图所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO3固体,它在高温下能传导阳极生成的O2-(O2+4e-=2O2-),d电极上的电极反应式为_____________________ 。

(1)金属冶炼与处理常涉及氧化还原反应,由下列物质冶炼相应金属单质时采用电解法的是
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述
(3)利用甲醇(CH3OH)、氧气组成燃料电池,电解质溶液为碱性,电池工作时负极反应式为
(4)氨气也可作为燃料电池的燃料源制成高效率无污染的燃料电池系统,总反应式为:
 (未配平),写出此碱性燃料电池的负极反应式:
(未配平),写出此碱性燃料电池的负极反应式:(5)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。与MnO2-Zn电池类似,K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为
(6)科学家制造出一种使用固体电解质的燃料电池,其效率高无污染,多用于航天航空。如图所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO3固体,它在高温下能传导阳极生成的O2-(O2+4e-=2O2-),d电极上的电极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电化学原理在金属腐蚀、能量转换、物质合成等方面应用广泛。
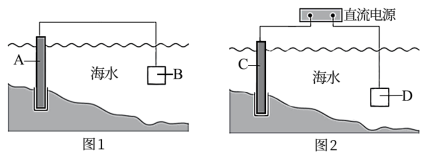
(1)通常可用图l、图2所示的两种方式减缓海水埘钢闸门A的腐蚀,则图l中材料B通常选择_________ (填字母序号),图2 中材料C最好选择_________ (填字母序号)。
a.钠块 b.铜块 c.锌块 d.石墨
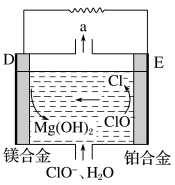
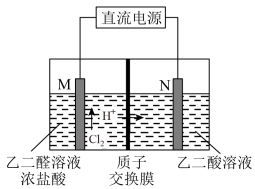
图3 图4
则图2中C上发生的主要电极反应式为___________________ 。
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①D为该燃料电池的________ 极(填“正”或“负”)。E电极上的电极反应式为_______ 。
②镁燃料电池负极容易发生自腐蚀使负极利用率降低,该过程中产生的气体a为_______ (填化学式)。
(3)乙醇酸(HOOC—CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸。
①乙二醛(OHC—CHO)与M电极的气体产物反应生成乙醛酸,则反应的化学方程式为____________ 。
②该电解装置工作中若有0.5molH+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为____________ mol。

(1)通常可用图l、图2所示的两种方式减缓海水埘钢闸门A的腐蚀,则图l中材料B通常选择
a.钠块 b.铜块 c.锌块 d.石墨


图3 图4
则图2中C上发生的主要电极反应式为
(2)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①D为该燃料电池的
②镁燃料电池负极容易发生自腐蚀使负极利用率降低,该过程中产生的气体a为
(3)乙醇酸(HOOC—CHO)是有机合成的重要中间体。工业上用“双极室成对电解法”生产乙醛酸,原理如图4所示,该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸。
①乙二醛(OHC—CHO)与M电极的气体产物反应生成乙醛酸,则反应的化学方程式为
②该电解装置工作中若有0.5molH+通过质子交换膜,并完全参与了反应,则该装置中生成的乙醛酸为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】课题式研究性学习是培养学生创造思维的良好方法,某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y 都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:
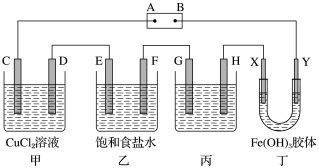
(1)电源A 极的名称是________ 。
(2)甲装置中电解反应的总化学方程式是__________________ 。
(3)如果收集乙装置中产生的气体,两种气体的体积比是________ 。
(4)欲用丙装置精炼铜,G应该是____ (填“纯铜”或“粗铜”),电解液的成分是______ 。
(5)已知氢氧化铁胶体中含有带正电荷的红褐色的粒子,那么装置丁中的现象是________________ 。
(6)在实验室电解500 mL 0.03 mol/L的NaCl溶液,通电一段时间后溶液中c(OH-)为1×10-2 mol/L(设电解时溶液的体积变化忽略不计),阴极产生___ mL(标况)气体,溶液中NaCl的浓度为_______ mol/L。

(1)电源A 极的名称是
(2)甲装置中电解反应的总化学方程式是
(3)如果收集乙装置中产生的气体,两种气体的体积比是
(4)欲用丙装置精炼铜,G应该是
(5)已知氢氧化铁胶体中含有带正电荷的红褐色的粒子,那么装置丁中的现象是
(6)在实验室电解500 mL 0.03 mol/L的NaCl溶液,通电一段时间后溶液中c(OH-)为1×10-2 mol/L(设电解时溶液的体积变化忽略不计),阴极产生
您最近一年使用:0次



