分别在等体积等pH或等物质的量浓度的盐酸和醋酸溶液中,加入足量锌粉,氢离子浓度c(H+)及氢气的体积V(H2)(同温同压下测定)的变化图示如图所示,其中正确的是
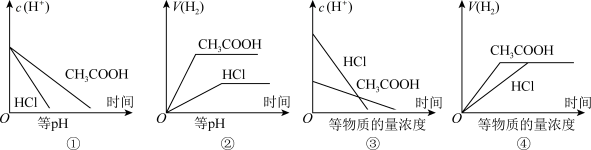

| A.①③ | B.②④ | C.①②③ | D.①②③④ |
16-17高二下·山东烟台·开学考试 查看更多[3]
更新时间:2020-03-23 09:31:59
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】某温度下,pH=11的氨水和NaOH溶液分别加水稀释100倍,溶液的pH随溶液体积变化的曲线如图所示。根据图象判断错误的是


| A.稀释后氨水中水的电离程度比NaOH溶液中水的电离程度大 |
| B.Ⅰ为NaOH溶液稀释时溶液的pH变化曲线 |
| C.完全中和稀释后的两溶液,消耗相同浓度的稀H2SO4的体积:V(NaOH)<V(氨水) |
| D.a值一定大于9 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】常温下,同时将 盐酸和
盐酸和 醋酸中溶质的浓度稀释到原浓度的
醋酸中溶质的浓度稀释到原浓度的 ,稀释过程中溶液
,稀释过程中溶液 的变化如图所示。下列说法正确的是
的变化如图所示。下列说法正确的是
 盐酸和
盐酸和 醋酸中溶质的浓度稀释到原浓度的
醋酸中溶质的浓度稀释到原浓度的 ,稀释过程中溶液
,稀释过程中溶液 的变化如图所示。下列说法正确的是
的变化如图所示。下列说法正确的是
A.曲线a表示盐酸稀释过程中的 变化 变化 |
B. 醋酸溶液中: 醋酸溶液中: |
| C.稀释后溶液中所有离子浓度均下降 |
D.稀释过程中 不变 不变 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】从植物花汁中提取的一种有机物可简化表示为HIn,因其在水溶液中存在下列电离平衡,故可用作酸碱指示剂:HIn(溶液,红色)⇌H+(溶液)+In-(溶液,黄色)。在上述溶液中加入适量下列物质,最终能使指示剂显黄色的是
| A.盐酸 | B.NaOH溶液 | C.NaHSO4溶液 | D.NaClO(固体) |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】在100mL0.1 mol∙L−1CH3COOH溶液中,欲使CH3COOH的电离程度和溶液的pH都增大,可采用的方法是
| A.微热 | B.加少量1 mol∙L−1盐酸 |
| C.加少量CH3COONa固体 | D.加少量水 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】将c(H+)=1×10-2mol/L的CH3COOH和HNO3溶液分别稀释100倍,稀释后两溶液的H+的物质的量浓度分别为a和b,则a和b的关系为
| A.a>b | B.a<b | C.a=b | D.不能确定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
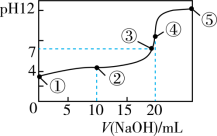
【推荐2】25℃时,在20mL HA溶液中逐滴加入
HA溶液中逐滴加入 NaOH溶液,pH的变化曲线如图所示,下列有关说法或关系不正确的是
NaOH溶液,pH的变化曲线如图所示,下列有关说法或关系不正确的是
 HA溶液中逐滴加入
HA溶液中逐滴加入 NaOH溶液,pH的变化曲线如图所示,下列有关说法或关系不正确的是
NaOH溶液,pH的变化曲线如图所示,下列有关说法或关系不正确的是
| A.甲基橙可以选为该滴定过程终点判断的指示剂 |
| B.由点①可知HA是一元弱酸 |
| C.点④溶液溶质为NaA,该点溶液呈碱性 |
D.点③溶液中有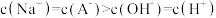 |
您最近一年使用:0次
单选题
|
较易
(0.85)
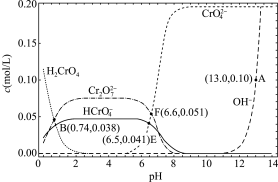
【推荐1】某温度下,改变
 溶液的
溶液的 时,各种含铬元素粒子及
时,各种含铬元素粒子及 浓度变化如图所示(已知
浓度变化如图所示(已知 是二元酸)。下列有关说法错误的是
是二元酸)。下列有关说法错误的是

 溶液的
溶液的 时,各种含铬元素粒子及
时,各种含铬元素粒子及 浓度变化如图所示(已知
浓度变化如图所示(已知 是二元酸)。下列有关说法错误的是
是二元酸)。下列有关说法错误的是
| A.该温度为25℃ |
B.溶液中存在平衡 ,该温度下此反应的 ,该温度下此反应的 |
C.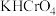 溶液中: 溶液中: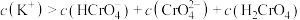 |
D.  溶液中: 溶液中: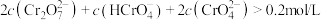 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】在测定中和热的实验中,下列说法正确的是
| A.酸、碱溶液应沿玻璃棒分三次倒入小烧杯 |
| B.用铜棒代替环形玻璃搅拌棒,会使测得的中和热的绝对值偏大 |
| C.用0.55 mol/L的NaOH溶液分别与0.5 mol/L的盐酸、醋酸溶液反应,若所取的溶液体积相等,则测得的中和热数值相同 |
| D.测量终止温度时,应当记录混合溶液的最高温度 |
您最近一年使用:0次



 2SO3,由图可知该反应的正反应是放热反应
2SO3,由图可知该反应的正反应是放热反应

