【物质结构与性质】
硅电池、锂离子电池都是现代高性能电池的代表,高性能的电极材料与物质结构密切相关。
(l) LiFePO4因具有良好的结构稳定性而成为新一代正极材料,这与 的结构密切相关,
的结构密切相关, 的立体构型为
的立体构型为____ 。P、O、S的电负性从大到小的顺序为______________ ____ (填标号)。
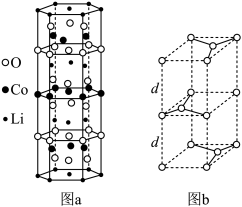
①锂钴复合氧化物中Li、Co、O分别形成了六边层状结构(图a),按照Li-O-Co-O-Li–O-Co-O- Li--顺序排列,则该化合物的化学式为____ ,Co3+的价层电子排布式为_____ 。
②石墨晶胞(图b)层间距为d pm,C—C键长为a pm,石墨晶体的密度为p g/cm3,列式表示阿伏加 德罗常数为____ mol-l。
硅电池、锂离子电池都是现代高性能电池的代表,高性能的电极材料与物质结构密切相关。
(l) LiFePO4因具有良好的结构稳定性而成为新一代正极材料,这与
 的结构密切相关,
的结构密切相关, 的立体构型为
的立体构型为(2)通常在电极材料表面进行“碳”包覆处理以增强其导电性。抗坏血酸(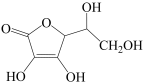 )常被用作碳包覆的碳源,其易溶于水的原因是
)常被用作碳包覆的碳源,其易溶于水的原因是
A.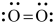 B.
B.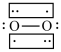 C.
C.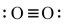 D.
D.
①锂钴复合氧化物中Li、Co、O分别形成了六边层状结构(图a),按照Li-O-Co-O-Li–O-Co-O- Li--顺序排列,则该化合物的化学式为
②石墨晶胞(图b)层间距为d pm,C—C键长为a pm,石墨晶体的密度为p g/cm3,列式表示阿伏加 德罗常数为
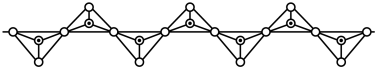
(5)硅酸盐中Si元素一般显+4价,如下图所示是一种无限长单键的多聚硅酸根离子的结构,其中“ ”表示Si原子,“
”表示Si原子,“ ”表示氧原子,则该长链硅酸根离子的通式为
”表示氧原子,则该长链硅酸根离子的通式为
更新时间:2020-04-01 11:15:33
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】2019年诺贝尔化学奖授予三位开发锂离子电池的科学家。TiS2、LiCoO2和LiMnO2等都是他们研究锂离子电池的载体。回答下列问题:
(1)基态Co原子价层电子排布式为_______________________________ 。
(2)已知第三电离能数据:I3(Mn) =3246 kJ·mol-1,I3(Fe) =2957 kJ·mol-1。 锰的第三电离能大于铁的第三电离能,其主要原因是_______________________________ 。
(3)据报道,在MnO2的催化下,甲醛可被氧化成CO2,在处理含HCHO的废水或空气方面有广泛应用。HCHO中键角_________ CO2中键角(填“大于”“小于”或“等于")。
(4)Co3+、Co2+能与NH3、H2O、SCN-等配体组成配合物。
①1 mol [ Co(NH3)6]3+含______ mol σ键。
②配位原子提供孤电子对与电负性有关,电负性越大,对孤电子对吸引力越大。SCN-的结构式为[S=C=N]- ,SCN-与金属离子形成的配离子中配位原子是______ ( 填元素符号)。
③配离子在水中颜色与分裂能有关,某些水合离子的分裂能如表所示:
由此推知,a______ b(填“>”“<”或“="),主要原因是_______________________ 。
(5)工业上,采用电解熔融氯化锂制备锂,钠还原TiCl4(g)制备钛。已知:LiCl 、TiCl4的熔点分别为605 °C、-24 °C,它们的熔点相差很大,其主要原因是_______________ 。
(6)钛的化合物有2种不同结构的晶体,其晶胞如图所示。

二氧化钛晶胞(如图1)中钛原子配位数为__________ 。 氮化钛的晶胞如图2所示,图3是氮化钛的晶胞截面图。已知:NA是阿伏加德常数的值,氮化钛晶体密度为dg·cm -3。氮化钛晶胞中N原子半径为__________ pm
(1)基态Co原子价层电子排布式为
(2)已知第三电离能数据:I3(Mn) =3246 kJ·mol-1,I3(Fe) =2957 kJ·mol-1。 锰的第三电离能大于铁的第三电离能,其主要原因是
(3)据报道,在MnO2的催化下,甲醛可被氧化成CO2,在处理含HCHO的废水或空气方面有广泛应用。HCHO中键角
(4)Co3+、Co2+能与NH3、H2O、SCN-等配体组成配合物。
①1 mol [ Co(NH3)6]3+含
②配位原子提供孤电子对与电负性有关,电负性越大,对孤电子对吸引力越大。SCN-的结构式为[S=C=N]- ,SCN-与金属离子形成的配离子中配位原子是
③配离子在水中颜色与分裂能有关,某些水合离子的分裂能如表所示:
| 配离子 | Fe(H2O)6]3+ | [Fe(H2O)6]2+ | [Co(H2O)6]2+ | [Co(H2O)6]3+ |
| 分裂能/kJ·mol-1 | 164 | 124 | a | b |
由此推知,a
(5)工业上,采用电解熔融氯化锂制备锂,钠还原TiCl4(g)制备钛。已知:LiCl 、TiCl4的熔点分别为605 °C、-24 °C,它们的熔点相差很大,其主要原因是
(6)钛的化合物有2种不同结构的晶体,其晶胞如图所示。

二氧化钛晶胞(如图1)中钛原子配位数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐2】氮化硼(BN)是一种高硬度、耐高温、耐腐蚀、高绝缘性的材料。一种获得氮化硼的方法如下:
NaBH4 B(OH)3
B(OH)3 →BN
→BN
已知:1.电负性:H2.1 B2.0 N3.0 O3.5
2.SiC与BN晶体的熔点和硬度数据如下:
(1)NaBH4被认为是有机化学上的“万能还原剂”。从化合价角度分析NaBH4具有强还原性的原因是_______ 。
(2)硼酸的化学式为B(OH)3,是一元弱酸。硼酸产生H+过程为:B(OH)3+H2O⇌H++[B(OH)4]-
①硼酸分子的空间构型为_______ 。
②硼酸具有弱酸性是由于B与水中的OH-形成配位键,描述配位键的形成过程_______ 。
(3)某一种氮化硼晶体的晶胞结构如下图:

①氮化硼(BN)属于_______ 晶体;B原子的轨道杂化类型为_______ 。
②该种氮化硼的熔点和硬度均高于SiC的原因是_______ 。
③已知该晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,则晶胞的边长为_______ cm(列计算式)。
NaBH4
 B(OH)3
B(OH)3 →BN
→BN已知:1.电负性:H2.1 B2.0 N3.0 O3.5
2.SiC与BN晶体的熔点和硬度数据如下:
| 物质 | 熔点/℃ | 硬度 |
| 碳化硅(SiC) | 2830 | 9-9.5 |
| 氮化硼(BN) | 3000 | 9.5 |
(2)硼酸的化学式为B(OH)3,是一元弱酸。硼酸产生H+过程为:B(OH)3+H2O⇌H++[B(OH)4]-
①硼酸分子的空间构型为
②硼酸具有弱酸性是由于B与水中的OH-形成配位键,描述配位键的形成过程
(3)某一种氮化硼晶体的晶胞结构如下图:

①氮化硼(BN)属于
②该种氮化硼的熔点和硬度均高于SiC的原因是
③已知该晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,则晶胞的边长为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】科幻电影《阿凡达》中外星人流的是蓝色的血液,其实血液的颜色主要是由血蛋白中含有的金属元素决定的,如含铁元素的为常见红色血液、含铜元素的为蓝色血液、含钒元素的为绿色血液等,铜、铁、钒在科学研究和工农业生产中有许多用途。回答下列问题:
(1)基态V的核外电子排布式为___________ 。
(2) 溶液常用作农业杀菌剂,溶液中存在
溶液常用作农业杀菌剂,溶液中存在 。该离子中存在的化学键有
。该离子中存在的化学键有___________ (填字母)。
A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键
(3) 与氨基吡啶形成的配合物(结构如图)是很好的磁性材料。该配合物分子中碳与氧原子间形成的
与氨基吡啶形成的配合物(结构如图)是很好的磁性材料。该配合物分子中碳与氧原子间形成的 键和π键的个数比为
键和π键的个数比为___________ ,其中C原子的杂化轨道类型为___________ 。
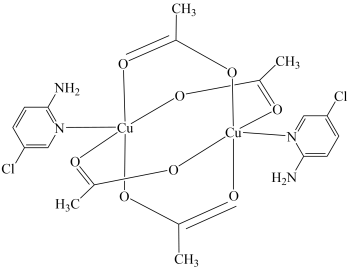
(4)铜的氧化物、氮化物都广泛应用于光信息存储和高速集成电路领域。
①Cu、O、N的电负性由大到小的顺序为___________ 。
②已知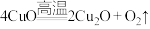 ,从铜离子的价层电子结构角度分析,高温下能转化生成
,从铜离子的价层电子结构角度分析,高温下能转化生成 的主要原因是
的主要原因是___________ 。
(1)基态V的核外电子排布式为
(2)
 溶液常用作农业杀菌剂,溶液中存在
溶液常用作农业杀菌剂,溶液中存在 。该离子中存在的化学键有
。该离子中存在的化学键有A.共价键 B.离子键 C.氢键 D.范德华力 E.配位键
(3)
 与氨基吡啶形成的配合物(结构如图)是很好的磁性材料。该配合物分子中碳与氧原子间形成的
与氨基吡啶形成的配合物(结构如图)是很好的磁性材料。该配合物分子中碳与氧原子间形成的 键和π键的个数比为
键和π键的个数比为
(4)铜的氧化物、氮化物都广泛应用于光信息存储和高速集成电路领域。
①Cu、O、N的电负性由大到小的顺序为
②已知
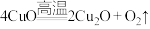 ,从铜离子的价层电子结构角度分析,高温下能转化生成
,从铜离子的价层电子结构角度分析,高温下能转化生成 的主要原因是
的主要原因是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】非金属在生产,生活和科研中应用广泛。
(1)下列说法正确的是___ 。
A.O元素的电负性大于Cl元素
B.3s电子能量高于2s,故3s电子一定在离核更远处运动
C.组成KH2PO4的四种元素形成的简单离子中,核外电子排布相同的有3种
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态的氟原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的氟原子,其价电子自旋磁量子数的代数和为___ 。
(3)CH3OH的沸点___ CH3SH,(填“高于”,“低于”或“等于”),原因是____ 。
(4)Xe是第五周期的稀有气体元素,与F形成的XeF4中心原子的价层电子对数为____ ,下列对XeF4中心原子杂化方式推断合理的是___ (填标号)。
A.sp B.sp2 C.sp3d2 D.sp3d
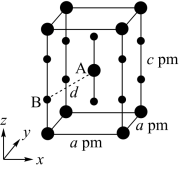
(5)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有___ 个XeF2分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为( ,
, ,
, )。已知Xe—F键长为rpm,则B点原子的分数坐标为
)。已知Xe—F键长为rpm,则B点原子的分数坐标为____ ;晶胞中A、B间距离d=___ pm。
(1)下列说法正确的是
A.O元素的电负性大于Cl元素
B.3s电子能量高于2s,故3s电子一定在离核更远处运动
C.组成KH2PO4的四种元素形成的简单离子中,核外电子排布相同的有3种
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态的氟原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的氟原子,其价电子自旋磁量子数的代数和为(3)CH3OH的沸点
(4)Xe是第五周期的稀有气体元素,与F形成的XeF4中心原子的价层电子对数为
A.sp B.sp2 C.sp3d2 D.sp3d
(5)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有
 ,
, ,
, )。已知Xe—F键长为rpm,则B点原子的分数坐标为
)。已知Xe—F键长为rpm,则B点原子的分数坐标为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】按要求回答下列问题
(1)中国古代四大发明之一-黑火药,它的爆炸反应为:2KNO3 + 3C+S A + N2↑+ 3CO2↑(已配平)
A + N2↑+ 3CO2↑(已配平)
①除S外,上列元素的电负性从大到小依次为_______ 。
②在生成物中,A的电子式_______ ,含极性共价键的分子的中心原子轨道杂化类型为_______ 。
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为_______ 。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为_______ ,Q2+的未成对电子数是_______ 。
(3)ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
①O、S、Se原子的第一电离能由大到小的顺序为_______ 。
②H2Se的酸性比H2S_______ (填“强”或“弱”)。气态SeO3分子的价层电子对互斥模型为_______ ,SeO 离子中Se的杂化方式为
离子中Se的杂化方式为_______ 。
(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是_______ 。
(5)已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体的配合物,其组成均为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种晶体的样品配成溶液;
b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤,经洗涤干燥后称量,发现绿色晶体产生沉淀的质量为紫色晶体产生沉淀质量的三分之二。则绿色晶体的配合物为_______ 。
(1)中国古代四大发明之一-黑火药,它的爆炸反应为:2KNO3 + 3C+S
 A + N2↑+ 3CO2↑(已配平)
A + N2↑+ 3CO2↑(已配平)①除S外,上列元素的电负性从大到小依次为
②在生成物中,A的电子式
③已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为
(3)ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含ⅥA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
①O、S、Se原子的第一电离能由大到小的顺序为
②H2Se的酸性比H2S
 离子中Se的杂化方式为
离子中Se的杂化方式为(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是
(5)已知Ti3+可形成配位数为6的配合物。现有紫色和绿色两种含钛晶体的配合物,其组成均为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种晶体的样品配成溶液;
b.向两种溶液中分别滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤,经洗涤干燥后称量,发现绿色晶体产生沉淀的质量为紫色晶体产生沉淀质量的三分之二。则绿色晶体的配合物为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】镍及其化合物在工农业生产中有着广泛应用,回答下列问题:
 基态镍原子的价电子排布式为
基态镍原子的价电子排布式为_________ ;元素镍的第二电离能比铜的小,其原因为_________________ 。
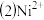 的检验可通过如下反应进行:
的检验可通过如下反应进行:

 丁二肟中碳原子的杂化轨道类型为
丁二肟中碳原子的杂化轨道类型为___________ 。
 二丁二肟合镍
二丁二肟合镍 Ⅱ
Ⅱ 中存在的作用力有
中存在的作用力有_________  填选项字母
填选项字母 。
。
A. 键
键  键
键  配位键
配位键  氢键
氢键
 四羰基镍
四羰基镍 为无色挥发性剧毒液体。熔点
为无色挥发性剧毒液体。熔点 ,沸点
,沸点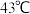 。不溶于水,易溶于乙醇等有机溶剂,呈四面体构型。四羰基镍的晶体类型是
。不溶于水,易溶于乙醇等有机溶剂,呈四面体构型。四羰基镍的晶体类型是__________ 。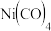 可通过如下反应合成:
可通过如下反应合成: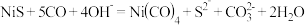 。反应中涉及所有元素的电负性由大到小的顺序为
。反应中涉及所有元素的电负性由大到小的顺序为______________ :与 互为等电子体的分子有
互为等电子体的分子有__________  任写1种
任写1种 。
。
 和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在中国已实现了产业化。该合金的晶胞结构如图所示。
和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在中国已实现了产业化。该合金的晶胞结构如图所示。
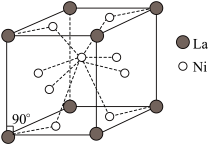
 该晶体的化学式为
该晶体的化学式为_____________ 。
 已知该晶体的摩尔质量为
已知该晶体的摩尔质量为 ,密度为
,密度为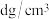 。设
。设 为阿伏加 德罗常数的值,则该晶胞的体积是
为阿伏加 德罗常数的值,则该晶胞的体积是___________  用含M、d、
用含M、d、 的代数式表示
的代数式表示 。
。
 基态镍原子的价电子排布式为
基态镍原子的价电子排布式为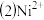 的检验可通过如下反应进行:
的检验可通过如下反应进行:
 丁二肟中碳原子的杂化轨道类型为
丁二肟中碳原子的杂化轨道类型为 二丁二肟合镍
二丁二肟合镍 Ⅱ
Ⅱ 中存在的作用力有
中存在的作用力有 填选项字母
填选项字母 。
。A.
 键
键  键
键 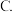 配位键
配位键  氢键
氢键 四羰基镍
四羰基镍 为无色挥发性剧毒液体。熔点
为无色挥发性剧毒液体。熔点 ,沸点
,沸点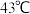 。不溶于水,易溶于乙醇等有机溶剂,呈四面体构型。四羰基镍的晶体类型是
。不溶于水,易溶于乙醇等有机溶剂,呈四面体构型。四羰基镍的晶体类型是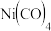 可通过如下反应合成:
可通过如下反应合成: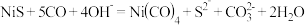 。反应中涉及所有元素的电负性由大到小的顺序为
。反应中涉及所有元素的电负性由大到小的顺序为 互为等电子体的分子有
互为等电子体的分子有 任写1种
任写1种 。
。 和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在中国已实现了产业化。该合金的晶胞结构如图所示。
和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在中国已实现了产业化。该合金的晶胞结构如图所示。
 该晶体的化学式为
该晶体的化学式为 已知该晶体的摩尔质量为
已知该晶体的摩尔质量为 ,密度为
,密度为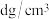 。设
。设 为阿伏加 德罗常数的值,则该晶胞的体积是
为阿伏加 德罗常数的值,则该晶胞的体积是 用含M、d、
用含M、d、 的代数式表示
的代数式表示 。
。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
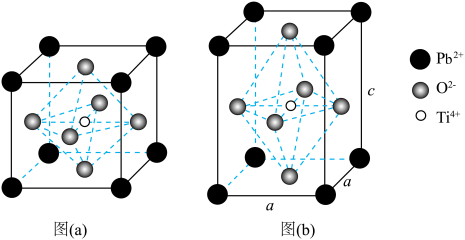
【推荐1】钛酸铅在光催化领域有很好的应用前景。以氨水、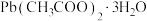 和二羟基双(乳酸铵)钛为原料可制得钛酸铅晶体。其晶体结构如下图,高于490℃时,结构以图(a)形式存在;低于490℃时,
和二羟基双(乳酸铵)钛为原料可制得钛酸铅晶体。其晶体结构如下图,高于490℃时,结构以图(a)形式存在;低于490℃时, 和
和 构成的正八面体会沿着c轴被拉伸,结构以图(b)形式存在。
构成的正八面体会沿着c轴被拉伸,结构以图(b)形式存在。
(1)Ti原子有___________ 种运动状态不同的电子,其价电子排布式为___________ 。该元素位于___________ 区。
A.s B.p C.d D.f
(2)制备钛酸铅的原料[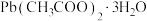 ]中,非金属元素的电负性由大到小的顺序为___________。
]中,非金属元素的电负性由大到小的顺序为___________。
(3)结合图(a)分析,立方钛酸铅的化学式为___________ 。
(4)四方钛酸铅[图(b)]中 周围最近的
周围最近的 数目为___________。
数目为___________。
(5)四方钛酸铅[图(b)]晶胞边长分别为 ,
, ,则该晶体的密度为
,则该晶体的密度为___________  。(计算结果保留2位小数,
。(计算结果保留2位小数, )
)
(6)二羟基双(乳酸铵)钛中负离子的结构为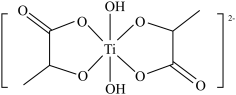 。
。
①二羟基双(乳酸铵)钛晶体中C原子杂化轨道类型为___________ 。
②二羟基双(乳酸铵)钛晶体类型为___________ 。
A.分子晶体 B.离子晶体 C.共价晶体 D.混合晶体
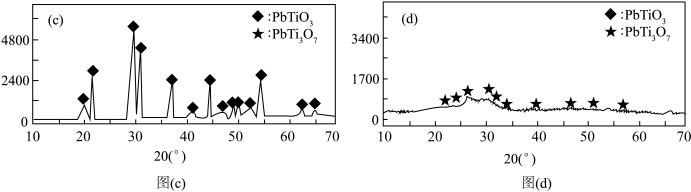
(7)晶体X射线衍射实验图谱会出现尖锐的峰。在制备钛酸铅时,分别向其中加入5 mL和20 mL二乙二醇X射线衍射实验图谱分别为图(c)和图(d),该图组说明在二乙二醇含量为20 mL时,___________ 形成晶态PbTiO3。
A.能 B.不能
 和二羟基双(乳酸铵)钛为原料可制得钛酸铅晶体。其晶体结构如下图,高于490℃时,结构以图(a)形式存在;低于490℃时,
和二羟基双(乳酸铵)钛为原料可制得钛酸铅晶体。其晶体结构如下图,高于490℃时,结构以图(a)形式存在;低于490℃时, 和
和 构成的正八面体会沿着c轴被拉伸,结构以图(b)形式存在。
构成的正八面体会沿着c轴被拉伸,结构以图(b)形式存在。
(1)Ti原子有
A.s B.p C.d D.f
(2)制备钛酸铅的原料[
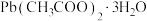 ]中,非金属元素的电负性由大到小的顺序为___________。
]中,非金属元素的电负性由大到小的顺序为___________。| A.C>H>O | B.O>H>C | C.O>C>H | D.H>O>C |
(3)结合图(a)分析,立方钛酸铅的化学式为
(4)四方钛酸铅[图(b)]中
 周围最近的
周围最近的 数目为___________。
数目为___________。| A.2 | B.4 | C.6 | D.8 |
(5)四方钛酸铅[图(b)]晶胞边长分别为
 ,
, ,则该晶体的密度为
,则该晶体的密度为 。(计算结果保留2位小数,
。(计算结果保留2位小数, )
)(6)二羟基双(乳酸铵)钛中负离子的结构为
 。
。①二羟基双(乳酸铵)钛晶体中C原子杂化轨道类型为
②二羟基双(乳酸铵)钛晶体类型为
A.分子晶体 B.离子晶体 C.共价晶体 D.混合晶体
(7)晶体X射线衍射实验图谱会出现尖锐的峰。在制备钛酸铅时,分别向其中加入5 mL和20 mL二乙二醇X射线衍射实验图谱分别为图(c)和图(d),该图组说明在二乙二醇含量为20 mL时,
A.能 B.不能

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】研究人员利用3,3-二氟环丁基胺,成功设计并合成出了首例无铅、多极轴的二维有机—无机杂化钙钛矿铁电体{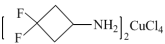 }。该材料表现出了优异的铁电性能、出色的多极轴特性和独特的热致变色性质,有望应用于新一代的多功能智能器件中。请回答下列问题:
}。该材料表现出了优异的铁电性能、出色的多极轴特性和独特的热致变色性质,有望应用于新一代的多功能智能器件中。请回答下列问题:
(1)基态 原子的电子排布式为
原子的电子排布式为_______ 。
(2)3,3-二氟环丁基胺(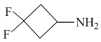 )中所含元素的电负性由强到弱的顺序为
)中所含元素的电负性由强到弱的顺序为_______ (用元素符号表示)。
(3)沸点:
_______ (填“>”或“<”) ,解释其原因:
,解释其原因:_______ 。
(4) 配合物中碳原子的杂化类型是
配合物中碳原子的杂化类型是_______ ,所含化学键的类型为_______ 。
(5)单质铁的晶体在不同温度下有两种堆积方式,分别为面心立方最密堆积和体心立方堆积。则在面心立方晶胞和体心立方晶胞中含有的铁原子的个数之比为_______ 。
(6)晶体具有自范性及各向异性等特点,造成晶体某些物理性质的各向异性最本质的原因是_______ ;铜与氯形成的晶体的晶胞如图所示,该晶体的化学式为_______ ,已知晶胞边长为 ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为_______  。
。
 }。该材料表现出了优异的铁电性能、出色的多极轴特性和独特的热致变色性质,有望应用于新一代的多功能智能器件中。请回答下列问题:
}。该材料表现出了优异的铁电性能、出色的多极轴特性和独特的热致变色性质,有望应用于新一代的多功能智能器件中。请回答下列问题:(1)基态
 原子的电子排布式为
原子的电子排布式为(2)3,3-二氟环丁基胺(
 )中所含元素的电负性由强到弱的顺序为
)中所含元素的电负性由强到弱的顺序为(3)沸点:

 ,解释其原因:
,解释其原因:(4)
 配合物中碳原子的杂化类型是
配合物中碳原子的杂化类型是(5)单质铁的晶体在不同温度下有两种堆积方式,分别为面心立方最密堆积和体心立方堆积。则在面心立方晶胞和体心立方晶胞中含有的铁原子的个数之比为
(6)晶体具有自范性及各向异性等特点,造成晶体某些物理性质的各向异性最本质的原因是
 ,
, 为阿伏加德罗常数的值,则该晶体的密度为
为阿伏加德罗常数的值,则该晶体的密度为 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】锰酸锂离子蓄电池是第二代锂离子动力电池。一种以软锰矿浆(主要成分为 ,含少量
,含少量 等杂质)为原料制备锰酸锂的流程如图所示。
等杂质)为原料制备锰酸锂的流程如图所示。
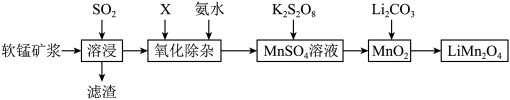
(1)溶浸生产中为提高 吸收率可采取的措施有___________(填序号)。
吸收率可采取的措施有___________(填序号)。
(2)X可选择的最佳试剂是___________ (填序号)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液
(3)由硫酸锰与 (过硫酸钾,结构为
(过硫酸钾,结构为 )溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。
)溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。 中
中 原子的化合价为
原子的化合价为___________ ,S原子的杂化方式为___________ 。
(4)将 和
和 按4:1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品
按4:1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品 并生两种气体。该反应的化学方程式为
并生两种气体。该反应的化学方程式为___________ 。
(5)锰酸锂可充电电池的总反应为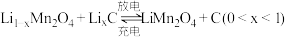
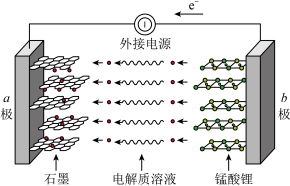
①放电时,电池正极的电极反应式为___________ 。
②充电时, 向
向___________ 极移动(填“a”或“b”)。
 ,含少量
,含少量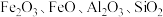 等杂质)为原料制备锰酸锂的流程如图所示。
等杂质)为原料制备锰酸锂的流程如图所示。
(1)溶浸生产中为提高
 吸收率可采取的措施有___________(填序号)。
吸收率可采取的措施有___________(填序号)。A.不断搅拌,使 和软锰矿浆充分接触 和软锰矿浆充分接触 | B.减小通入 的流速 的流速 |
| C.减少软锰矿浆的进入量 | D.增大通入 的流速 的流速 |
(2)X可选择的最佳试剂是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液(3)由硫酸锰与
 (过硫酸钾,结构为
(过硫酸钾,结构为 )溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。
)溶液常温下混合一周,慢慢得到球形二氧化锰(MnO2)。 中
中 原子的化合价为
原子的化合价为(4)将
 和
和 按4:1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品
按4:1的物质的量比配料,混合搅拌,然后升温至600~750℃,制取产品 并生两种气体。该反应的化学方程式为
并生两种气体。该反应的化学方程式为(5)锰酸锂可充电电池的总反应为
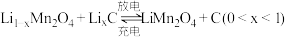

①放电时,电池正极的电极反应式为
②充电时,
 向
向
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】中国较早时期就有炼铜、炼锌技术的记录,铜、锌元素也是人体必需的微量元素之一。回答下列问题:
(1)基态Cu原子核外的最高能层符号是___ ,基态Zn价电子排布式为___ 。
(2)硫酸铜溶于氨水形成[Cu(NH3)4]SO4溶液,组成[Cu(NH3)4]SO4的元素中,除Cu外其余元素的电负性由大到小排序为___ 。
(3)向[Cu(NH3)4]SO4溶液中逐滴滴加NaOH溶液,未出现浑浊,其原因是___ 。
(4)ZnO与ZnS结构相似,ZnO的熔点为1975℃,ZnS的熔点约为1700℃。ZnO熔点比ZnS高的原因是___ 。
(5)[Zn(CN)4]2-发生反应:4HCHO+[Zn(CN)4]2-+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
①HOCH2CN分子中碳原子轨道的杂化类型是___ 。
②与H2O分子互为等电子体的阴离子为___ 。
③[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为___ 。
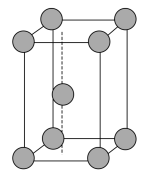
(6)金属锌晶体的晶胞如图所示,若锌原子的半径为rnm,则金属锌晶体的空间利用率是___ (用含π的代数式表示)。
(1)基态Cu原子核外的最高能层符号是
(2)硫酸铜溶于氨水形成[Cu(NH3)4]SO4溶液,组成[Cu(NH3)4]SO4的元素中,除Cu外其余元素的电负性由大到小排序为
(3)向[Cu(NH3)4]SO4溶液中逐滴滴加NaOH溶液,未出现浑浊,其原因是
(4)ZnO与ZnS结构相似,ZnO的熔点为1975℃,ZnS的熔点约为1700℃。ZnO熔点比ZnS高的原因是
(5)[Zn(CN)4]2-发生反应:4HCHO+[Zn(CN)4]2-+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
①HOCH2CN分子中碳原子轨道的杂化类型是
②与H2O分子互为等电子体的阴离子为
③[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为
(6)金属锌晶体的晶胞如图所示,若锌原子的半径为rnm,则金属锌晶体的空间利用率是

您最近一年使用:0次
【推荐2】中国是世界上最大的钨储藏国。以黑钨精矿(主要成分为FeWO4、MnWO4,含少量SiO2)为原料冶炼钨的流程如图所示:

已知:钨酸酸性很弱,难溶于水;25℃时, 和
和 开始沉淀的pH分别为10.3和7.3,完全沉淀的pH分别为8和5;碳和金属钨在高温下会反应生成碳化钨。
开始沉淀的pH分别为10.3和7.3,完全沉淀的pH分别为8和5;碳和金属钨在高温下会反应生成碳化钨。
回答下列问题:
(1)74W在周期表的位置是第_______ 周期VIB族。
(2)FeWO4参与反应的化学方程式为_______ 。
(3)“滤液I”调节pH应选择的试剂为_______ (填字母),调节pH的范围为_______ 。
A.氨水 B. WO3 C.稀硫酸 D. NaOH
(4)25℃时,Ca(OH)2和CaWO4(钨酸钙)的沉淀溶解平衡曲线如图所示。

①反应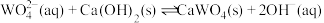 的平衡常数K=
的平衡常数K=_______ 。
②d点的CaWO4溶液中,加入CaCl2固体,d点溶液_______ (填“能”或“不能”)沿da线向c点移动(假设混合后溶液体积不变)。
(5)碳化钨(WC)是大型飞机发动机关键部位材料。碳化钨晶体的结构单元如图所示,一个W原子与周围_______ 个碳原子紧密相邻且等距;已知该结构单元边长为acmn,高为hcm,NA为阿伏加德罗常数数值,WC的摩尔质量为M ,该晶体密度为
,该晶体密度为_______  。
。


已知:钨酸酸性很弱,难溶于水;25℃时,
 和
和 开始沉淀的pH分别为10.3和7.3,完全沉淀的pH分别为8和5;碳和金属钨在高温下会反应生成碳化钨。
开始沉淀的pH分别为10.3和7.3,完全沉淀的pH分别为8和5;碳和金属钨在高温下会反应生成碳化钨。回答下列问题:
(1)74W在周期表的位置是第
(2)FeWO4参与反应的化学方程式为
(3)“滤液I”调节pH应选择的试剂为
A.氨水 B. WO3 C.稀硫酸 D. NaOH
(4)25℃时,Ca(OH)2和CaWO4(钨酸钙)的沉淀溶解平衡曲线如图所示。

①反应
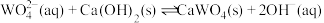 的平衡常数K=
的平衡常数K=②d点的CaWO4溶液中,加入CaCl2固体,d点溶液
(5)碳化钨(WC)是大型飞机发动机关键部位材料。碳化钨晶体的结构单元如图所示,一个W原子与周围
 ,该晶体密度为
,该晶体密度为 。
。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有B、C、N、Ni等元素。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是_______ (填标号,下同),用光谱仪可捕捉到发射光谱的是_______ 。
A.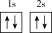 B.
B.
C. D.
D.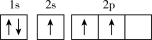
(2)基态N原子的成对电子数与未成对电子数之比为_______ , 离子的空间构型为
离子的空间构型为_______ 。
(3)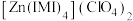 是
是 的一种配合物,IMI的结构为
的一种配合物,IMI的结构为 ,其中碳原子杂化方式为
,其中碳原子杂化方式为_______ ,所含元素电负性由大到小的顺序是_______ 。IMI中大π键可表示为_______ (已知苯中的大π键可表示为 ),该配合物的配位原子为
),该配合物的配位原子为_______ (填序号)。
(4)镍能形成多种配合物,其中 是无色挥发性液体,
是无色挥发性液体, 是红黄色单斜晶体。
是红黄色单斜晶体。 的熔点高于
的熔点高于 的原因是
的原因是_______ 。
(5)红银矿NiAs晶体结构如图所示:

①两个As原子的原子分数坐标依次为( ,
, ,
, )和
)和_______ 。
②已知NA为阿伏加德罗常数的值,X射线光谱测算出的晶胞参数为a=b=m pm、c=n pm,则该晶体的密度为_______  (用含m、n的代数式表示)。
(用含m、n的代数式表示)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是
A.
 B.
B.
C.
 D.
D.
(2)基态N原子的成对电子数与未成对电子数之比为
 离子的空间构型为
离子的空间构型为(3)
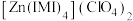 是
是 的一种配合物,IMI的结构为
的一种配合物,IMI的结构为 ,其中碳原子杂化方式为
,其中碳原子杂化方式为 ),该配合物的配位原子为
),该配合物的配位原子为(4)镍能形成多种配合物,其中
 是无色挥发性液体,
是无色挥发性液体, 是红黄色单斜晶体。
是红黄色单斜晶体。 的熔点高于
的熔点高于 的原因是
的原因是(5)红银矿NiAs晶体结构如图所示:

①两个As原子的原子分数坐标依次为(
 ,
, ,
, )和
)和②已知NA为阿伏加德罗常数的值,X射线光谱测算出的晶胞参数为a=b=m pm、c=n pm,则该晶体的密度为
 (用含m、n的代数式表示)。
(用含m、n的代数式表示)。
您最近一年使用:0次



