中国较早时期就有炼铜、炼锌技术的记录,铜、锌元素也是人体必需的微量元素之一。回答下列问题:
(1)基态Cu原子核外的最高能层符号是___ ,基态Zn价电子排布式为___ 。
(2)硫酸铜溶于氨水形成[Cu(NH3)4]SO4溶液,组成[Cu(NH3)4]SO4的元素中,除Cu外其余元素的电负性由大到小排序为___ 。
(3)向[Cu(NH3)4]SO4溶液中逐滴滴加NaOH溶液,未出现浑浊,其原因是___ 。
(4)ZnO与ZnS结构相似,ZnO的熔点为1975℃,ZnS的熔点约为1700℃。ZnO熔点比ZnS高的原因是___ 。
(5)[Zn(CN)4]2-发生反应:4HCHO+[Zn(CN)4]2-+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
①HOCH2CN分子中碳原子轨道的杂化类型是___ 。
②与H2O分子互为等电子体的阴离子为___ 。
③[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为___ 。
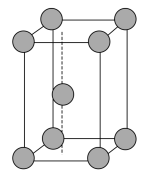
(6)金属锌晶体的晶胞如图所示,若锌原子的半径为rnm,则金属锌晶体的空间利用率是___ (用含π的代数式表示)。
(1)基态Cu原子核外的最高能层符号是
(2)硫酸铜溶于氨水形成[Cu(NH3)4]SO4溶液,组成[Cu(NH3)4]SO4的元素中,除Cu外其余元素的电负性由大到小排序为
(3)向[Cu(NH3)4]SO4溶液中逐滴滴加NaOH溶液,未出现浑浊,其原因是
(4)ZnO与ZnS结构相似,ZnO的熔点为1975℃,ZnS的熔点约为1700℃。ZnO熔点比ZnS高的原因是
(5)[Zn(CN)4]2-发生反应:4HCHO+[Zn(CN)4]2-+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
①HOCH2CN分子中碳原子轨道的杂化类型是
②与H2O分子互为等电子体的阴离子为
③[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为
(6)金属锌晶体的晶胞如图所示,若锌原子的半径为rnm,则金属锌晶体的空间利用率是

更新时间:2021-11-11 14:09:51
|
相似题推荐
【推荐1】现代工业冶炼黄金的原理是:
①
②
请回答下列问题:
(1)铜、银、金位于同族,周期数依次增大。基态金原子价层电子排布式为_______ 。
(2)上述反应中,短周期元素电负性由小到大排序为_______ (填元素符号)。
(3)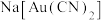 中所含化学键类型有_______(填字母)。
中所含化学键类型有_______(填字母)。
(4) 中
中 的杂化类型是
的杂化类型是_______ ;画出它的结构式_______ 。
(5)锌、钠的熔点分别为692K、371K,解释它们熔点的差异:_______ 。
(6)由金、氯和铯组成的晶体,晶胞如图所示(大灰球为铯,小黑球为氯,白球为金)。

①该晶胞含有2种不同化学环境的金,形成2种不同的配离子且均为阴离子,分别是_______ 、____ 。
②该晶体的化学式为_______ 。
(7)金和银合金构成面心立方堆积,金位于顶点、银位于面心,晶胞参数为408pm。晶胞中相邻两个面心上银原子之间距离为_______ pm。
①

②

请回答下列问题:
(1)铜、银、金位于同族,周期数依次增大。基态金原子价层电子排布式为
(2)上述反应中,短周期元素电负性由小到大排序为
(3)
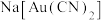 中所含化学键类型有_______(填字母)。
中所含化学键类型有_______(填字母)。| A.非极性键 | B.金属键 | C.配位键 | D.π键 |
 中
中 的杂化类型是
的杂化类型是(5)锌、钠的熔点分别为692K、371K,解释它们熔点的差异:
(6)由金、氯和铯组成的晶体,晶胞如图所示(大灰球为铯,小黑球为氯,白球为金)。

①该晶胞含有2种不同化学环境的金,形成2种不同的配离子且均为阴离子,分别是
②该晶体的化学式为
(7)金和银合金构成面心立方堆积,金位于顶点、银位于面心,晶胞参数为408pm。晶胞中相邻两个面心上银原子之间距离为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】近期我国学者研制出低成本的电解“水制氢”催化剂——镍掺杂的磷化钴三元纳米片电催化剂(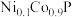 )。回答下列问题:
)。回答下列问题:
(1)P在元素周期表中的位置为___________ ,Ni原子价层电子排布式为___________ 。
(2)Co形成的一种配合物结构如下: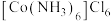
①配合物中提供孤对电子的原子是___________ ;配位数是___________ 。
②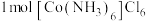 中含有
中含有 键的数目为
键的数目为___________ 。
③N、P属于同主族元素, 的沸点高于
的沸点高于 的沸点的原因是
的沸点的原因是___________ 。
④ 和
和 中氮原子的杂化方式是
中氮原子的杂化方式是___________ , 中键角
中键角___________ (填写“大于”、“小于”或“等于”) 中键角。
中键角。
(3)磷化硼是一种备受关注的耐磨涂料,其晶体中磷原子作面心立方最密堆积,硼原子填入四面体空隙中(如图)。已知磷化硼的晶胞边长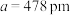 ,已知磷化硼晶体密度为
,已知磷化硼晶体密度为 ,
,
___________ (不必化简),P原子的配位数是___________ 。
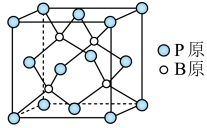
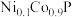 )。回答下列问题:
)。回答下列问题:(1)P在元素周期表中的位置为
(2)Co形成的一种配合物结构如下:
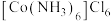
①配合物中提供孤对电子的原子是
②
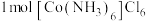 中含有
中含有 键的数目为
键的数目为③N、P属于同主族元素,
 的沸点高于
的沸点高于 的沸点的原因是
的沸点的原因是④
 和
和 中氮原子的杂化方式是
中氮原子的杂化方式是 中键角
中键角 中键角。
中键角。(3)磷化硼是一种备受关注的耐磨涂料,其晶体中磷原子作面心立方最密堆积,硼原子填入四面体空隙中(如图)。已知磷化硼的晶胞边长
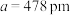 ,已知磷化硼晶体密度为
,已知磷化硼晶体密度为 ,
,

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有B、C、N、Ni、Cu等元素。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是____ (填标号,下同),用光谱仪可捕捉到发射光谱的是____ 。
A. B.
B.
C. D.
D.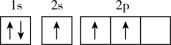
(2)已知高温下Cu2O比CuO更稳定,试从核外电子排布的角度解释:________ 。
(3)类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H−S−C≡N)的沸点低于异硫氰酸(H−N=C=S)的沸点,其主要原因为______ 。
(4)写出与 互为等电子体的一种非极性分子的化学式
互为等电子体的一种非极性分子的化学式_______ 。
(5)一种高迁移率的新型热电材料由Cd、Sn、As三种原子构成。该晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的坐标如表所示。
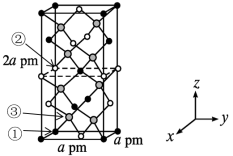
①该晶胞中粒子个数比Cd:Sn:As=________ ,找出距离Cd(0,0,0)最近的Sn原子:_______ (用坐标表示)。
②与Sn距离最近的As的数目为______ ,设该化合物的最简式量为M,该晶体的密度为_____  。(列计算式,设NA为阿伏加德罗常数的数值)
。(列计算式,设NA为阿伏加德罗常数的数值)
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是
A.
 B.
B.
C.
 D.
D.
(2)已知高温下Cu2O比CuO更稳定,试从核外电子排布的角度解释:
(3)类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H−S−C≡N)的沸点低于异硫氰酸(H−N=C=S)的沸点,其主要原因为
(4)写出与
 互为等电子体的一种非极性分子的化学式
互为等电子体的一种非极性分子的化学式(5)一种高迁移率的新型热电材料由Cd、Sn、As三种原子构成。该晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的坐标如表所示。
| 原子 | 坐标 | ||
| x | y | z | |
| ①Cd | 0 | 0 | 0 |
| ②Sn | 0 | 0 | 1 |
| ③As | 0.25 | 0.25 | 0.25 |

①该晶胞中粒子个数比Cd:Sn:As=
②与Sn距离最近的As的数目为
 。(列计算式,设NA为阿伏加德罗常数的数值)
。(列计算式,设NA为阿伏加德罗常数的数值)
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】镁、硅及其化合物用途非常广泛。回答下列问题:
(1)基态Si原子价层电子的电子排布图(轨道表达式)为__________ ,基态Mg原子电子占据最高能级的电子云轮廓图为__________ 形。
(2)Mg2C3与水反应可生成H2C=C=CH2,中间的碳原子杂化方式是__________ ,反应所涉及的元素中电负性最大的是__________ (填元素符号),Mg2C3和H2C=C=CH2中均存在(填字母)__________ 。
A.配位键 B.σ键 C.π键 D.氢键
(3)MgO晶格能可通过图1的bom- Haber循环计算得到。

Mg的第二电离能为__________ kJ·mol-1;O=O键的键能为_________ kJ·mol-1;MgO的晶格能为__________ kJ·mol-1。
(4)Mg2Si晶胞结构如图2所示,已知其密度为1.94g·cm-3,NA为阿伏伽德罗常数的值。
①则晶胞参数a=__________ nm(列出计算式)
②Mg2Si的另一种表示中,四个Mg处于上图所示立方体中的Si的位置,则Si处于____________ 。
(1)基态Si原子价层电子的电子排布图(轨道表达式)为
(2)Mg2C3与水反应可生成H2C=C=CH2,中间的碳原子杂化方式是
A.配位键 B.σ键 C.π键 D.氢键
(3)MgO晶格能可通过图1的bom- Haber循环计算得到。

Mg的第二电离能为
(4)Mg2Si晶胞结构如图2所示,已知其密度为1.94g·cm-3,NA为阿伏伽德罗常数的值。
①则晶胞参数a=
②Mg2Si的另一种表示中,四个Mg处于上图所示立方体中的Si的位置,则Si处于
您最近一年使用:0次
【推荐2】硅烷广泛应用在现代高科技领域。制备硅烷的反应为SiF4+NaAlH4=SiH4+NaAlF4。
(1)基态硅原子的价层电子轨道表示式为_____ 。
(2)SiF4中,硅的化合价为+4价。硅显正化合价的原因是_____ 。
(3)下列说法正确的是_____ (填字母)。
a.SiH4的稳定性比CH4的差
b.SiH4中4个Si-H的键长相同,H-Si-H的键角为90°
c.SiH4中硅原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个Si-Hσ键
(4)SiF4的沸点(-86℃)高于SiH4的沸点(-112℃),原因是_____ 。
(5)NaAlH4的晶胞结构如图所示,晶胞的体积为a2b×10-24cm3。
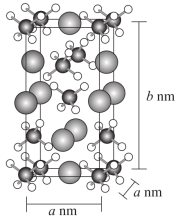
用NA表示阿伏加德罗常数的值。NaAlH4晶体密度为_____ g•cm-3(用含a、b、NA的代数式表示)。
(1)基态硅原子的价层电子轨道表示式为
(2)SiF4中,硅的化合价为+4价。硅显正化合价的原因是
(3)下列说法正确的是
a.SiH4的稳定性比CH4的差
b.SiH4中4个Si-H的键长相同,H-Si-H的键角为90°
c.SiH4中硅原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个Si-Hσ键
(4)SiF4的沸点(-86℃)高于SiH4的沸点(-112℃),原因是
(5)NaAlH4的晶胞结构如图所示,晶胞的体积为a2b×10-24cm3。

用NA表示阿伏加德罗常数的值。NaAlH4晶体密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】(1)红细胞中血红素结构如图所示,回答下列问题:
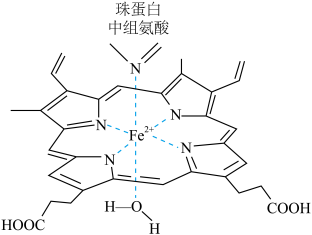
①Fe2+的轨道表示式[Ar]________ 。
②所含短周期元素电负性从大到小的顺序是___________ 。
③羧基中碳原子的杂化轨道方式是______________ 。
④在肺部,血红素中的Fe2+结合的水分子与氧分子交换,形成氧合血红蛋白,经动脉运送到组织释放出O2;然后血红素结合组织代谢所产生的CO2,经静脉送回肺中与水分子交换,最后将CO2排出体外,完成呼吸过程。血红素中Fe2+与CO2中____ 原子以____ 形式结合,这种结合是可逆的,比Fe2+与N的结合弱的原因是______________ 。
(2)磁性氧化铁Fe3O4含有Fe2+和Fe3+,其晶体属于立方晶系,氧原子呈面心立方密堆积,Fe3+和一半的Fe3+随机占据八面体空穴,电子可在Fe2+、Fe3+间迅速发生转移,另一半Fe3+作阳离占据四面体空穴。Fe3O4是一种盐,其真实结构可较好地表示为_________ [Fe2+和Fe3+分别用Fe(II)、Fe(III)表示];该晶体_____ 导电(填“能”、“不能”);该晶体的密度为5.18g·cm-3,其晶胞中最近的两个氧原子之间的核间距_________ cm(列出计算式,不必计算最终结果)。

①Fe2+的轨道表示式[Ar]
②所含短周期元素电负性从大到小的顺序是
③羧基中碳原子的杂化轨道方式是
④在肺部,血红素中的Fe2+结合的水分子与氧分子交换,形成氧合血红蛋白,经动脉运送到组织释放出O2;然后血红素结合组织代谢所产生的CO2,经静脉送回肺中与水分子交换,最后将CO2排出体外,完成呼吸过程。血红素中Fe2+与CO2中
(2)磁性氧化铁Fe3O4含有Fe2+和Fe3+,其晶体属于立方晶系,氧原子呈面心立方密堆积,Fe3+和一半的Fe3+随机占据八面体空穴,电子可在Fe2+、Fe3+间迅速发生转移,另一半Fe3+作阳离占据四面体空穴。Fe3O4是一种盐,其真实结构可较好地表示为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】铜和钛可呈现多种化合价,回答下列问题。
(1)配位化合物中心原子也存在轨道杂化现象,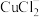 中
中 采取sp杂化,
采取sp杂化,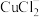 的空间结构为
的空间结构为___________ 。
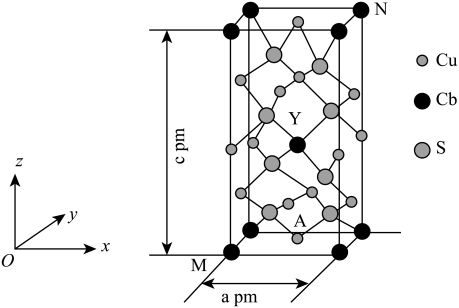
(2)某种含铜热电材料,晶胞结构如图,Cu位于棱、面上,Sb位于体心、顶点,S位于晶胞内,底部边长为 ,高为
,高为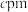 ,该晶体化学式为
,该晶体化学式为___________ ,其中部分原子坐标为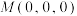 、
、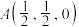 、
、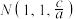 ,Y点的原子坐标为
,Y点的原子坐标为___________ 。
(3)基态Ti原子的价电子轨道表示式为___________ 。
(4)钛基配合物可用于催化环烯烃聚合,其结构如图所示:
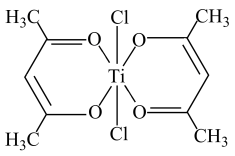
钛的配位数为___________ 。
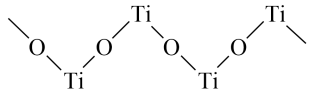
(5)已知 与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为
与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为___________ 。
(1)配位化合物中心原子也存在轨道杂化现象,
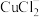 中
中 采取sp杂化,
采取sp杂化,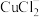 的空间结构为
的空间结构为(2)某种含铜热电材料,晶胞结构如图,Cu位于棱、面上,Sb位于体心、顶点,S位于晶胞内,底部边长为
 ,高为
,高为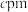 ,该晶体化学式为
,该晶体化学式为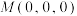 、
、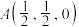 、
、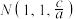 ,Y点的原子坐标为
,Y点的原子坐标为
(3)基态Ti原子的价电子轨道表示式为
(4)钛基配合物可用于催化环烯烃聚合,其结构如图所示:

钛的配位数为
(5)已知
 与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为
与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子化学式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】硒(Se)是一种有抗癌、抗氧化作用的元素,可形成多种化合物,含硒化合物在材料和药物等领域有重要应用。回答下列问题:
(1)基态硒原子价电子排布式为___________ 。
(2)某绿色农药的结构简式如图所示。C、N、O、F四种元素第一电离能由大到小的排列顺序为___________ ;该物质中,C原子的杂化轨道类型为___________ 。

(3)亚硒酸钠(Na2SeO3)能消除加速人体衰老的活性氧,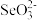 的空间构型为
的空间构型为___________ ;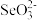 的键角
的键角___________ 气态分子SeO3(填“>”、“<”或“=”),原因是___________ 。
(4)二硫键与二硒键是重要的光响应动态共价键,其光响应原理可用下图表示。已知光的波长与其能量成反比,则图中实现光响应的波长λ1___________ λ2(填“>”、“<”或“=”)。

(5)硒氧化铋是一类全新二维半导体芯片材料,为四方晶系晶胞结构(如图所示),可以看成带正电的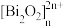 层与带负电的
层与带负电的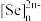 层交替堆叠。据此推断硒氧化铋的化学式为
层交替堆叠。据此推断硒氧化铋的化学式为___________ 。晶胞棱边夹角均为90°,则晶体密度的计算式为___________ g·cm-3(NA为阿伏加德罗常数的值)

(1)基态硒原子价电子排布式为
(2)某绿色农药的结构简式如图所示。C、N、O、F四种元素第一电离能由大到小的排列顺序为

(3)亚硒酸钠(Na2SeO3)能消除加速人体衰老的活性氧,
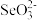 的空间构型为
的空间构型为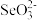 的键角
的键角(4)二硫键与二硒键是重要的光响应动态共价键,其光响应原理可用下图表示。已知光的波长与其能量成反比,则图中实现光响应的波长λ1

(5)硒氧化铋是一类全新二维半导体芯片材料,为四方晶系晶胞结构(如图所示),可以看成带正电的
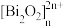 层与带负电的
层与带负电的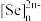 层交替堆叠。据此推断硒氧化铋的化学式为
层交替堆叠。据此推断硒氧化铋的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】钛及其化合物在生产、生活中有着广泛的用途。回答下列问题:
(1)Ti(BH4)3是一种储氢材料。BH 的空间构型为
的空间构型为_______ ;Ti 、B、H元素的电负性由大到小排列顺序为_______ 。
(2)已知Ti3+易形成多种配合物,[TiCl( H2O)5]Cl2· H2O是其中的一种。
①1 mol该配合物中含有_______ molσ键。
②中心离子杂化方式为_______ (填标号)。
a.sp2 b.sp3 c.sp3d d.sp3d2
③Ti3+具有较强还原性的原因是_______ 。
(3)研究表明,TiO2通过氮掺杂反应可生成TiO2-x Ny,能使TiO2对可见光具有活性,反应如图所示。

①上图TiO2晶胞中钛原子占据_______ 个氧原子围成的八面体空隙。
②已知所有的Ti-O键键长为rpm,B点原子的分数坐标为( ,
, ,
, ),则A点原子的分数坐标为
),则A点原子的分数坐标为_______ ;晶胞中A、B间距离为_______ pm;TiO2晶体密度为_______ g·cm-3(设NA为阿伏加德罗常数的值)。
③TiO2-x Ny晶体中x=_______ 。
(1)Ti(BH4)3是一种储氢材料。BH
 的空间构型为
的空间构型为(2)已知Ti3+易形成多种配合物,[TiCl( H2O)5]Cl2· H2O是其中的一种。
①1 mol该配合物中含有
②中心离子杂化方式为
a.sp2 b.sp3 c.sp3d d.sp3d2
③Ti3+具有较强还原性的原因是
(3)研究表明,TiO2通过氮掺杂反应可生成TiO2-x Ny,能使TiO2对可见光具有活性,反应如图所示。

①上图TiO2晶胞中钛原子占据
②已知所有的Ti-O键键长为rpm,B点原子的分数坐标为(
 ,
, ,
, ),则A点原子的分数坐标为
),则A点原子的分数坐标为③TiO2-x Ny晶体中x=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】西北工业大学曾华强课题组借用足球烯核心,成功实现了高效且选择性可精准定制的离子跨膜运输,如图所示。

已知:图甲中的有机物为“冠醚”,命名规则是“环上原子个数-冠醚-氧原子个数”。
请回答下列问题:
(1)基态Cs原子的价层电子的轨道表示式为___________ 。基态K原子的核外电子云有___________ 个伸展方向。
(2)运输Cs+的冠醚名称是___________ 。冠醚分子中氧原子的杂化类型是___________ ,冠醚与碱金属离子之间存在微弱的配位键,配位原子是___________ (填元素符号)。
(3)几种冠醚与识别的碱金属离子的有关数据如下表所示:
18-冠醚-6不能识别和运输Na+和Cs+的原因是___________ 。
(4)碱金属氯化物中NaCl 、KCl、RbCl、 CsCl熔点由高到低顺序为___________ ,理由是___________ 。
(5) 具有反萤石结构,晶胞如图所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为
具有反萤石结构,晶胞如图所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为 ,则
,则 的密度为
的密度为___________  (列出计算式)。若该立方晶胞中原子A的坐标参数为(0,1,0),则原子B的坐标参数为
(列出计算式)。若该立方晶胞中原子A的坐标参数为(0,1,0),则原子B的坐标参数为___________ 。


已知:图甲中的有机物为“冠醚”,命名规则是“环上原子个数-冠醚-氧原子个数”。
请回答下列问题:
(1)基态Cs原子的价层电子的轨道表示式为
(2)运输Cs+的冠醚名称是
(3)几种冠醚与识别的碱金属离子的有关数据如下表所示:
| 冠醚 | 冠醚空腔直径/pm | 适合的粒子直径/pm |
| 12-冠醚- 4 | 120~ 150 | Li+ (152) |
| 15 -冠醚- 5 | 170~ 220 | Na+ (204) |
| 18 -冠醚- 6 | 260~ 320 | K+ (276) |
| —— | 340~ 430 | Rb+ (304) |
| Cs+ (334) |
(4)碱金属氯化物中NaCl 、KCl、RbCl、 CsCl熔点由高到低顺序为
(5)
 具有反萤石结构,晶胞如图所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为
具有反萤石结构,晶胞如图所示。已知晶胞参数为0.4665nm,阿伏加德罗常数的值为 ,则
,则 的密度为
的密度为 (列出计算式)。若该立方晶胞中原子A的坐标参数为(0,1,0),则原子B的坐标参数为
(列出计算式)。若该立方晶胞中原子A的坐标参数为(0,1,0),则原子B的坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐2】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为___________ 。
(2) 及其周期表中相邻元素的第一电离能(I1)如表所示。
及其周期表中相邻元素的第一电离能(I1)如表所示。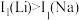 ,原因是
,原因是___________ 。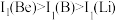 ,原因是
,原因是___________ 。
(3)磷酸根离子的空间构型为___________ ,其中P的价层电子对数为___________ 、杂化轨道类型为___________ 。
(4)金刚石与石墨都是碳的同素异形体。若碳原子半径为rnm,根据硬球接触模型,金刚石晶胞中碳原子的空间占有率为___________ (用含π的代数式表示);金刚石的密度为___________ g/cm3 (写出用r和 表示的计算式即可)
表示的计算式即可)

(1)基态
 与
与 离子中未成对的电子数之比为
离子中未成对的电子数之比为(2)
 及其周期表中相邻元素的第一电离能(I1)如表所示。
及其周期表中相邻元素的第一电离能(I1)如表所示。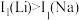 ,原因是
,原因是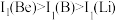 ,原因是
,原因是| I1/(kJ·mol-1) | ||
| Li 520 | Be 900 | B 801 |
| Na 496 | Mg 738 | Al 578 |
(3)磷酸根离子的空间构型为
(4)金刚石与石墨都是碳的同素异形体。若碳原子半径为rnm,根据硬球接触模型,金刚石晶胞中碳原子的空间占有率为
 表示的计算式即可)
表示的计算式即可)
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】金属冶炼过程中一种用有机化合物从水溶液中提取 的流程如下:
的流程如下:
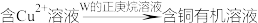
(1)有机化合物W的结构简式为:___________ 种,N、O杂化轨道类型分别为___________ 、___________ 。
(2)W可与 形成化合物Q,其结构如下所示:
形成化合物Q,其结构如下所示: 的价电子排布式为
的价电子排布式为___________ 。
②氢键对Q在水中溶解性的影响是___________ (填“增大”或“减小”)。
③W与 之间以共价键和配位键相结合,其中一定是配位键的是
之间以共价键和配位键相结合,其中一定是配位键的是___________ 键(填“Cu—O”或“Cu—N”)。
(3)有机化合物的合成通常使用催化剂,一种催化剂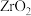 晶体的晶胞示意图如下:
晶体的晶胞示意图如下:___________ (填元素符号)。与每个Y原子距离最近且等距的X原子有___________ 个。
②该晶胞边长为a nm,阿伏加德罗常数为 ,则该晶体的密度
,则该晶体的密度
___________  (列出计算式,
(列出计算式, 的摩尔质量为123
的摩尔质量为123  )。
)。
 的流程如下:
的流程如下: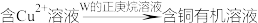
(1)有机化合物W的结构简式为:

(2)W可与
 形成化合物Q,其结构如下所示:
形成化合物Q,其结构如下所示:
 的价电子排布式为
的价电子排布式为②氢键对Q在水中溶解性的影响是
③W与
 之间以共价键和配位键相结合,其中一定是配位键的是
之间以共价键和配位键相结合,其中一定是配位键的是(3)有机化合物的合成通常使用催化剂,一种催化剂
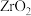 晶体的晶胞示意图如下:
晶体的晶胞示意图如下:
②该晶胞边长为a nm,阿伏加德罗常数为
 ,则该晶体的密度
,则该晶体的密度
 (列出计算式,
(列出计算式, 的摩尔质量为123
的摩尔质量为123  )。
)。
您最近一年使用:0次



