四川省眉山市仁寿县2021-2022学年高三上学期零诊考试理综化学试题
四川
高三
模拟预测
2021-11-13
998次
整体难度:
适中
考查范围:
常见无机物及其应用、认识化学科学、化学实验基础、有机化学基础、化学反应原理、物质结构与性质
四川省眉山市仁寿县2021-2022学年高三上学期零诊考试理综化学试题
四川
高三
模拟预测
2021-11-13
998次
整体难度:
适中
考查范围:
常见无机物及其应用、认识化学科学、化学实验基础、有机化学基础、化学反应原理、物质结构与性质
一、单选题 添加题型下试题
单选题
|
适中(0.65)
2. 设NA表示阿伏加德罗常数的值,下列说法正确的是
| A.1molNH3含有的电子数为NA |
| B.常温常压下,22.4LCCl4含有NA个CCl4分子 |
| C.2L0.1mol/L的FeCl3溶液中含Fe3+的数目为0.2NA |
| D.标准状况下,22.4LSO2与足量的O2反应,转移电子数目小于2NA |
【知识点】 阿伏加德罗常数的求算解读
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
您最近一年使用:0次
单选题
|
较易(0.85)
4. 下列关于有机化合物的说法,正确的是
| A.甲苯的一溴代物和2—甲基丁烷的一溴代物都有4种(不考虑立体异构) |
| B.不能用溴水鉴别己烯、苯、乙醇 |
| C.乙烷、苯分子内所有原子均可能在同一平面上 |
| D.油脂组成和结构复杂,是天然高分子化合物 |
您最近一年使用:0次
单选题
|
适中(0.65)
5. 工业上以铁为原料,经过一系列步骤可制备纳米四氧化三铁,有关流程示意图如图,下列有关叙述不正确的是
Fe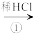 FeCl2
FeCl2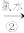 FeCl3溶液
FeCl3溶液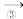 FeCl3•6H2O
FeCl3•6H2O FeOOH
FeOOH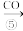 Fe3O4
Fe3O4
Fe
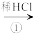 FeCl2
FeCl2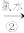 FeCl3溶液
FeCl3溶液 FeCl3•6H2O
FeCl3•6H2O FeOOH
FeOOH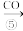 Fe3O4
Fe3O4| A.步骤⑤中CO的作用是还原FeOOH |
| B.步骤③中涉及的操作有蒸发浓缩、冷却结晶、过滤 |
| C.①中应该用足量稀HCl,步骤②中氯水可用H2O2代替 |
| D.将制得的Fe3O4粒子均匀分散在水中形成的分散系具有均一性、稳定性 |
【知识点】 有关铁及其化合物转化的流程题型解读 Fe2+的还原性解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
6. 磷酸铁锂电池是以磷酸铁锂为正极材料的一种锂离子二次电池,电池总反应为M1-xFexPO4+LiC6 LiM1-xFexPO4+6C,其原理如图所示,下列说法正确的是
LiM1-xFexPO4+6C,其原理如图所示,下列说法正确的是

 LiM1-xFexPO4+6C,其原理如图所示,下列说法正确的是
LiM1-xFexPO4+6C,其原理如图所示,下列说法正确的是
| A.放电时,石墨电极的电势更高 |
| B.充电时,Li+移向磷酸铁锂电极 |
| C.充电时,磷酸铁锂电极应与电源正极相连 |
| D.放电时,正极反应式为M1-xFexPO4+e-+Li+=LiFexPO4+(1-x)M |
您最近一年使用:0次
2021-11-11更新
|
1637次组卷
|
8卷引用:四川省眉山市仁寿县2021-2022学年高三上学期零诊考试理综化学试题
四川省眉山市仁寿县2021-2022学年高三上学期零诊考试理综化学试题(已下线)专题28 新型化学电源-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)一轮巩固卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(辽宁专用)(已下线)第12讲 化学电池(word讲义)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)(已下线)第25讲 化学电源(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)河北省衡水中学2023届高三上学期三调考试化学试题四川省成都市第七中学2022-2023学年高二下学期3月月考化学试题(已下线)专题08 新型化学电源(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
单选题
|
较难(0.4)
解题方法
7. 已知某二元酸H2A的Ka1=1.1×10-3,Ka2=3.9×10-6。常温下,用0.10mol·L-1的KOH溶液滴定20.0mL0.10mol·L-1的NaHA溶液,溶液pH的变化曲线如图所示。下列叙述错误的是


| A.c点溶液pH在9~10之间 |
| B.b点的混合溶液中:c(Na+)=2c(A2-)+c(HA-) |
| C.a点的混合溶液中:c(Na+)>c(A2-)>c(K+)>c(HA-) |
| D.a、b、c三点中,c点水的电离程度最大 |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
较易(0.85)
解题方法
8. FeCl3、FeCl2在工业生产中有很多用途,其中FeCl2是一种常用的还原剂、媒染剂,某实验小组用如下两种方法来制备无水FeCl2。有关物质的性质如下:
(1)用H2还原无水FeCl3制取FeCl2。有关装置如图1所示:

①A装置中装锌粒的仪器名称是___ ;检查A装置的气密性的方法是___ 。
②H2还原无水FeCl3制取FeCl2的化学方程式为___ 。
③按气流由左到右的方向,上述仪器的连接顺序为___ (填字母,装置可多次使用)。
(2)利用反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按图2装置,在三颈烧瓶中放入32.5g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却、分离提纯得到粗产品。
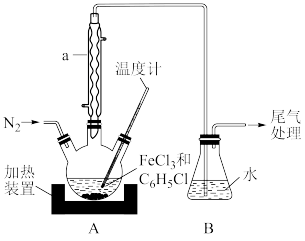
①仪器a的作用是___ 。
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品,回收滤液中C6H5Cl的操作方法是___ 。
③在反应开始之前先通一段时间N2的目的是___ ,在反应完成后继续通一段时间N2的作用是___ 。
④反应后将锥形瓶中溶液配成250mL,量取25.00mL所配溶液,用0.40mol•L-1NaOH溶液滴定,重复上述操作3次,达到滴定终点时消耗NaOH溶液的体积分别为19.50mL、20.50mL、19.70mL,则氯化铁的转化率为___ 。
| C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 | |
| 溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H2Cl2、苯,易溶于乙醇,易吸水 | ||
| 熔点/℃ | -45 | 53 | 易升华 | |
| 沸点/℃ | 132 | 173 | ||

①A装置中装锌粒的仪器名称是
②H2还原无水FeCl3制取FeCl2的化学方程式为
③按气流由左到右的方向,上述仪器的连接顺序为
(2)利用反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按图2装置,在三颈烧瓶中放入32.5g无水氯化铁和过量的氯苯,控制反应温度在一定范围加热3h,冷却、分离提纯得到粗产品。

①仪器a的作用是
②反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品,回收滤液中C6H5Cl的操作方法是
③在反应开始之前先通一段时间N2的目的是
④反应后将锥形瓶中溶液配成250mL,量取25.00mL所配溶液,用0.40mol•L-1NaOH溶液滴定,重复上述操作3次,达到滴定终点时消耗NaOH溶液的体积分别为19.50mL、20.50mL、19.70mL,则氯化铁的转化率为
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
9. 工业上使用催化剂时常需要载体,纳米氧化锌可作为一些催化剂的载体。工业上由软锰矿(主要成分为MnO2)与锌精矿(主要成分为ZnS)酸性共融法制备MnO2及纳米ZnO的工艺流程如图。回答下列问题:
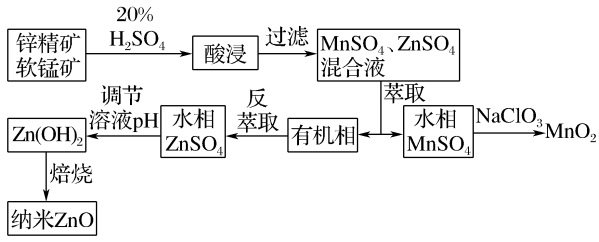
(1)为了提高矿石的“酸浸”率,可采取的措施___ (写两种)。
(2)实验室焙烧少量Zn(OH)2用到的硅酸盐仪器除玻璃棒、酒精灯外还需要的仪器有___ 。
(3)写出酸浸时ZnS与MnO2发生的主要反应的化学方程式___ (无单质硫生成)。
(4)P5O7(酸性磷酸酯)可作萃取剂分离锌、锰离子,它是一种不溶于水的淡黄色透明油状液体,属于酸性萃取剂。试分析P5O7可萃取ZnSO4从而使ZnSO4和MnSO4分离的原因是___ 。
(5)Na2S2O8是一种强氧化剂,能与Mn2+反应生成SO 和紫色MnO
和紫色MnO 。用Na2S2O8检验水相中的Mn2+时发生反应的离子方程式为
。用Na2S2O8检验水相中的Mn2+时发生反应的离子方程式为___ 。
(6)二氧化锰广泛用于电池。一种海水中的“水”电池的电池总反应可表示为5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。电池放电时,负极的电极反应式为___ 。
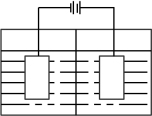
(7)MnO2也可用如图装置电解方法制备,电解池中间是质子交换膜,分隔开的两室溶液分别为足量的硫酸钠溶液和足量的硫酸锰溶液,则阴极室中的溶液为___ ;电解产生的MnO2沉积在电极上,若一段时间后该电极所在的溶液质量减轻了4.45克,则电路中转移的电子数为___ 。

(1)为了提高矿石的“酸浸”率,可采取的措施
(2)实验室焙烧少量Zn(OH)2用到的硅酸盐仪器除玻璃棒、酒精灯外还需要的仪器有
(3)写出酸浸时ZnS与MnO2发生的主要反应的化学方程式
(4)P5O7(酸性磷酸酯)可作萃取剂分离锌、锰离子,它是一种不溶于水的淡黄色透明油状液体,属于酸性萃取剂。试分析P5O7可萃取ZnSO4从而使ZnSO4和MnSO4分离的原因是
(5)Na2S2O8是一种强氧化剂,能与Mn2+反应生成SO
 和紫色MnO
和紫色MnO 。用Na2S2O8检验水相中的Mn2+时发生反应的离子方程式为
。用Na2S2O8检验水相中的Mn2+时发生反应的离子方程式为(6)二氧化锰广泛用于电池。一种海水中的“水”电池的电池总反应可表示为5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。电池放电时,负极的电极反应式为
(7)MnO2也可用如图装置电解方法制备,电解池中间是质子交换膜,分隔开的两室溶液分别为足量的硫酸钠溶液和足量的硫酸锰溶液,则阴极室中的溶液为

您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
解题方法
10. I.食醋是食物调味品之一,食醋中的乙酸也可以用于制氢,已知可以发生如下反应:
热裂解反应CH3COOH(g) 2CO(g)+2H2(g) △H=+2l3.7kJ·mol-1
2CO(g)+2H2(g) △H=+2l3.7kJ·mol-1
脱羧基反应CH3COOH(g) CH4(g)+CO2(g) △H=-33.5kJ·mol-1
CH4(g)+CO2(g) △H=-33.5kJ·mol-1
合成乙酸反应CH3OH(g)+CO(g)→CH3COOH(g) △H=-123.7kJ·mol-1
(1)请写出CO与H2甲醇化的热化学方程式___ 。
(2)在密闭容器中,利用乙酸制甲烷,若要使甲烷的产率较高,制备时选择的适宜条件为___ 。
II.工业上可用乙酸热裂解生成的CO和H2制备CH3OH,CH3OH也是重要的溶剂和替代燃料。
(3)某温度下,在一恒压容器中分别充入0.7molCO和0.5molCH3OH(g),达到平衡时容器体积为2L,且含有0.2molH2(g),则用CO和H2制备CH3OH平衡常数的值为___ ,此时向容器中再通入0.4molCO气体和0.2molCH3OH(g),则此平衡将___ 。(填“向正向移动”、“不移动”或“向逆向移动”)
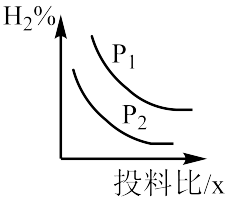
(4)对于CO和H2制备CH3OH的反应,若容器压强、CO与H2投料比x对反应的影响如图所示,则图中曲线所示的压强关系:p1___ p2(填“=”“>”或“<”),其判断理由是___ 。
(5)现有容积均为1L的a、b、c三个密闭容器,往其中分别充入1molCO和2molH2的混合气体,控制温度,进行反应,测得相关数据的关系如图所示。b中甲醇体积分数大于a中的原因是___ ;达到平衡时,a、b、c中CO的转化率大小关系为___ 。

热裂解反应CH3COOH(g)
 2CO(g)+2H2(g) △H=+2l3.7kJ·mol-1
2CO(g)+2H2(g) △H=+2l3.7kJ·mol-1脱羧基反应CH3COOH(g)
 CH4(g)+CO2(g) △H=-33.5kJ·mol-1
CH4(g)+CO2(g) △H=-33.5kJ·mol-1合成乙酸反应CH3OH(g)+CO(g)→CH3COOH(g) △H=-123.7kJ·mol-1
(1)请写出CO与H2甲醇化的热化学方程式
(2)在密闭容器中,利用乙酸制甲烷,若要使甲烷的产率较高,制备时选择的适宜条件为
| A.较低温度 | B.较大压强 | C.高温 | D.低压 |
II.工业上可用乙酸热裂解生成的CO和H2制备CH3OH,CH3OH也是重要的溶剂和替代燃料。
(3)某温度下,在一恒压容器中分别充入0.7molCO和0.5molCH3OH(g),达到平衡时容器体积为2L,且含有0.2molH2(g),则用CO和H2制备CH3OH平衡常数的值为
(4)对于CO和H2制备CH3OH的反应,若容器压强、CO与H2投料比x对反应的影响如图所示,则图中曲线所示的压强关系:p1

(5)现有容积均为1L的a、b、c三个密闭容器,往其中分别充入1molCO和2molH2的混合气体,控制温度,进行反应,测得相关数据的关系如图所示。b中甲醇体积分数大于a中的原因是

【知识点】 盖斯定律及其有关计算 化学平衡的有关计算
您最近一年使用:0次
解答题-结构与性质
|
较难(0.4)
11. 中国较早时期就有炼铜、炼锌技术的记录,铜、锌元素也是人体必需的微量元素之一。回答下列问题:
(1)基态Cu原子核外的最高能层符号是___ ,基态Zn价电子排布式为___ 。
(2)硫酸铜溶于氨水形成[Cu(NH3)4]SO4溶液,组成[Cu(NH3)4]SO4的元素中,除Cu外其余元素的电负性由大到小排序为___ 。
(3)向[Cu(NH3)4]SO4溶液中逐滴滴加NaOH溶液,未出现浑浊,其原因是___ 。
(4)ZnO与ZnS结构相似,ZnO的熔点为1975℃,ZnS的熔点约为1700℃。ZnO熔点比ZnS高的原因是___ 。
(5)[Zn(CN)4]2-发生反应:4HCHO+[Zn(CN)4]2-+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
①HOCH2CN分子中碳原子轨道的杂化类型是___ 。
②与H2O分子互为等电子体的阴离子为___ 。
③[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为___ 。
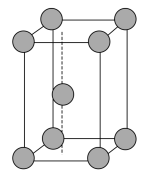
(6)金属锌晶体的晶胞如图所示,若锌原子的半径为rnm,则金属锌晶体的空间利用率是___ (用含π的代数式表示)。
(1)基态Cu原子核外的最高能层符号是
(2)硫酸铜溶于氨水形成[Cu(NH3)4]SO4溶液,组成[Cu(NH3)4]SO4的元素中,除Cu外其余元素的电负性由大到小排序为
(3)向[Cu(NH3)4]SO4溶液中逐滴滴加NaOH溶液,未出现浑浊,其原因是
(4)ZnO与ZnS结构相似,ZnO的熔点为1975℃,ZnS的熔点约为1700℃。ZnO熔点比ZnS高的原因是
(5)[Zn(CN)4]2-发生反应:4HCHO+[Zn(CN)4]2-+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
①HOCH2CN分子中碳原子轨道的杂化类型是
②与H2O分子互为等电子体的阴离子为
③[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键,不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为
(6)金属锌晶体的晶胞如图所示,若锌原子的半径为rnm,则金属锌晶体的空间利用率是

您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
12. 化工原料G的合成流程如图:

已知:①
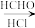

②CH3C≡CNa+ →
→
(1)B的名称___ ,条件X为___ 。
(2)E→F的反应类型为____ ,D→E的化学方程式为___ 。
(3)以乙烯为原料原子利率为100%的合成 的化学方程式为
的化学方程式为___ 。
(4)A、F的结构简式为___ ,___ 。
(5)符合下列条件的G的同分异构体有___ 种(不考虑立体异构)。
①与G具有相同官能团的芳香族类化合物;②有两个通过C—C相连的六元环;
其中核磁共振氢谱有8种吸收峰的结构简式为___ 。

已知:①

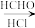

②CH3C≡CNa+
 →
→
(1)B的名称
(2)E→F的反应类型为
(3)以乙烯为原料原子利率为100%的合成
 的化学方程式为
的化学方程式为(4)A、F的结构简式为
(5)符合下列条件的G的同分异构体有
①与G具有相同官能团的芳香族类化合物;②有两个通过C—C相连的六元环;
其中核磁共振氢谱有8种吸收峰的结构简式为
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、认识化学科学、化学实验基础、有机化学基础、化学反应原理、物质结构与性质
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 次氯酸及其性质 二氧化硫的弱氧化性 | |
| 2 | 0.65 | 阿伏加德罗常数的求算 | |
| 3 | 0.65 | 化学实验基础操作 | |
| 4 | 0.85 | 同分异构体的数目的确定 有机分子中原子共面的判断 油脂的组成与结构 有机物的检验 | |
| 5 | 0.65 | 有关铁及其化合物转化的流程题型 Fe2+的还原性 | |
| 6 | 0.65 | 原电池原理 其他二次电池 | |
| 7 | 0.4 | 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 二、解答题 | |||
| 8 | 0.85 | 亚铁盐 铁盐 常见无机物的制备 | 实验探究题 |
| 9 | 0.4 | 氧化还原反应方程式的配平 电解池电极反应式及化学方程式的书写与判断 物质分离、提纯综合应用 | 工业流程题 |
| 10 | 0.65 | 盖斯定律及其有关计算 化学平衡的有关计算 | 原理综合题 |
| 11 | 0.4 | 电子排布式 元素性质与电负性的关系 利用杂化轨道理论判断分子的空间构型 晶胞的有关计算 | 结构与性质 |
| 12 | 0.65 | 有机反应类型 根据要求书写同分异构体 同分异构体的数目的确定 信息给予的有机合成 | 有机推断题 |




