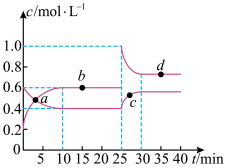
在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中发生反应:N2O4(g)  2NO2(g),反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示。
2NO2(g),反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示。
(1)该反应的平衡常数表达式为______________ ,若温度升高K值增大,则该反应的正反应为__________ 反应(填吸热或放热)。
(2)a、b、c、d四个点中,化学反应处于平衡状态的是______________ 点。从起点开始首次达到平衡时以NO2表示的平均反应速率为___________________________ 。
(3)25 min时,增加了______ mol______ (填物质的化学式)使平衡发生了移动。
(4)变化过程中a、b、c、d四个时刻体系的颜色由深到浅的顺序是______ (填字母)。
 2NO2(g),反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示。
2NO2(g),反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示。
(1)该反应的平衡常数表达式为
(2)a、b、c、d四个点中,化学反应处于平衡状态的是
(3)25 min时,增加了
(4)变化过程中a、b、c、d四个时刻体系的颜色由深到浅的顺序是
10-11高三上·上海浦东新·期末 查看更多[1]
(已下线)上海市浦东新区2010届高三上学期期末质量抽测化学试题
更新时间:2020-04-01 10:44:13
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某可逆反应: 平衡常数与温度关系如表所示:
平衡常数与温度关系如表所示:
(1)根据上述数据判断,该可逆反应的正反应是_______ (填“吸热”或“放热”)反应,理由是_______ 。
(2)为了增大X的转化率,宜采用的措施是_______(填写序号)
(3)440℃时,在2L密闭容器中,开始充入1mol X气体和3mol Y气体进行反应,在某时刻测得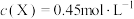 ,此时,反应是否达到平衡状态
,此时,反应是否达到平衡状态_______ (填“是”或“否”),简述理由:_______ 。
(4)在某容积固定的容器中进行上述反应,当X、Y起始物质的量一定时,仅改变一个外界条件对Z体积分数的影响如图所示(曲线Ⅰ为标准):
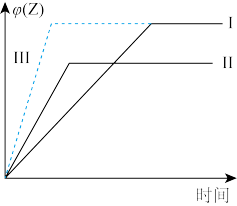
①曲线Ⅱ改变的条件是_______ 。
②曲线Ⅲ改变的条件是_______ 。
 平衡常数与温度关系如表所示:
平衡常数与温度关系如表所示:| 温度(℃) | 360 | 440 | 520 |
| K | 0.036 | 0.010 | 0.0038 |
(2)为了增大X的转化率,宜采用的措施是_______(填写序号)
| A.升高温度 | B.增大压强 | C.使用高效催化剂 | D.分离Z |
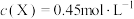 ,此时,反应是否达到平衡状态
,此时,反应是否达到平衡状态(4)在某容积固定的容器中进行上述反应,当X、Y起始物质的量一定时,仅改变一个外界条件对Z体积分数的影响如图所示(曲线Ⅰ为标准):

①曲线Ⅱ改变的条件是
②曲线Ⅲ改变的条件是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知CO和H2在催化剂作用下合成甲醇的反应如下:CO(g)+2H2(g)  CH3OH(g) ΔH1=-99 kJ/mol,反应的化学平衡常数K表达式为
CH3OH(g) ΔH1=-99 kJ/mol,反应的化学平衡常数K表达式为___________ ;下图中能正确反映平衡常数K随温度变化关系的曲线为___________ (填曲线标记字母),其判断理由是___________ 。
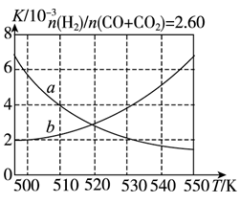
 CH3OH(g) ΔH1=-99 kJ/mol,反应的化学平衡常数K表达式为
CH3OH(g) ΔH1=-99 kJ/mol,反应的化学平衡常数K表达式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】25℃时,在1L的密闭容器中充入NO2发生如下反应:2NO2(g) N2O4(g)△H=-57 kJ·mol-1(N2O4在25℃时为无色气体)。
N2O4(g)△H=-57 kJ·mol-1(N2O4在25℃时为无色气体)。
(1)该反应的ΔS__________ 0(填“>”、“<”或“=”)。
(2)当开始充入0.03mol的NO2时,25℃时,实验测得NO2的平衡浓度为0.01 mol·L-1,则NO2的平衡转化率(α)是_____________ 。25℃时上述反应的平衡常数K =_________ 。
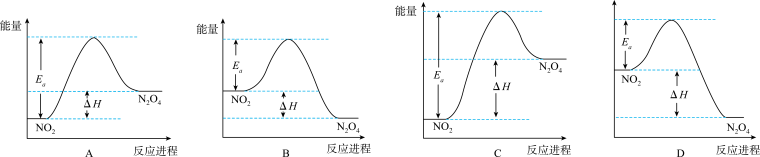
(3)25℃时,实验测得该反应的活化能Ea=92.4 kJ·mol-1。下列能量关系图合理的是_____ 。
(4)如把该密闭容器放入80℃的热水中,则气体的颜色___________ (填“不变”、“加深”或“变浅”),NO2的转化率___________ (填“增大”、“不变”或“减小”)。
 N2O4(g)△H=-57 kJ·mol-1(N2O4在25℃时为无色气体)。
N2O4(g)△H=-57 kJ·mol-1(N2O4在25℃时为无色气体)。(1)该反应的ΔS
(2)当开始充入0.03mol的NO2时,25℃时,实验测得NO2的平衡浓度为0.01 mol·L-1,则NO2的平衡转化率(α)是
(3)25℃时,实验测得该反应的活化能Ea=92.4 kJ·mol-1。下列能量关系图合理的是

(4)如把该密闭容器放入80℃的热水中,则气体的颜色
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0试回答下列问题:
CO2(g)+H2(g) ΔH<0试回答下列问题:
(1)若起始时c(CO)=2 mol/L,c(H2O)=3 mol/L,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K=____________ 。
(2)在相同温度下,若起始时c(CO)=1 mol/L,c(H2O)=2 mol/L,反应进行一段时间后,测得H2的浓度为0.5 mol/L,则此时该反应是否达到平衡状态________ (填“是”或“否”),此时v(正)________ v(逆)(填“大于”“小于”或“等于”)。
(3)若降低温度,该反应的K值将________ ,该反应的化学反应速率将________ (均填“增大”“减小”或“不变”)。
 CO2(g)+H2(g) ΔH<0试回答下列问题:
CO2(g)+H2(g) ΔH<0试回答下列问题:(1)若起始时c(CO)=2 mol/L,c(H2O)=3 mol/L,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K=
(2)在相同温度下,若起始时c(CO)=1 mol/L,c(H2O)=2 mol/L,反应进行一段时间后,测得H2的浓度为0.5 mol/L,则此时该反应是否达到平衡状态
(3)若降低温度,该反应的K值将
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g) +2H2(g) CH3OH(g) 。
CH3OH(g) 。

(1)甲图是反应时CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=________ mol•L-1•1min-1。
(2)乙图表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。反应的焓变是__________ (填“△H<0”或“△H>0”)反应,写出该反应的热化学方程式:__________ ;
(3)该反应平衡常数K的表达式为____ ,温度升高,平衡常数K________ (填“增大”、“不变”或“减小”)。
(4)下列措施能加快反应速率的是__________ 。
A 升高温度 B 增大容器的容积 C 再充入0.1molCO D 及时分离出CH3OH
(5)下列能说明反应达到平衡状态的是__________ 。
A 体系压强保持不变 B 混合气体总质量保持不变
C H2和CO的浓度相等 D 每消耗1 mol CO的同时生成1 mol CH3OH
 CH3OH(g) 。
CH3OH(g) 。
(1)甲图是反应时CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=
(2)乙图表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。反应的焓变是
(3)该反应平衡常数K的表达式为
(4)下列措施能加快反应速率的是
A 升高温度 B 增大容器的容积 C 再充入0.1molCO D 及时分离出CH3OH
(5)下列能说明反应达到平衡状态的是
A 体系压强保持不变 B 混合气体总质量保持不变
C H2和CO的浓度相等 D 每消耗1 mol CO的同时生成1 mol CH3OH
您最近一年使用:0次
【推荐3】研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+NOCl(g) K1 ΔH1<0 (Ⅰ)
NaNO3(s)+NOCl(g) K1 ΔH1<0 (Ⅰ)
2NO(g)+Cl2(g) 2NOCl(g) K2 ΔH2<0 (Ⅱ)
2NOCl(g) K2 ΔH2<0 (Ⅱ)
(1)4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=________ (用K1、K2表示)。
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得10 min内v(NOCl)=7.5×10-3 mol·L-1·min-1,则平衡后n(Cl2)=________ mol,NO的转化率α1=________ 。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2________ α1(填“>”“<”或“=”),平衡常数K2________ (填“增大”“减小”或“不变”)。若要使K2减小,可采取的措施是____________ 。
2NO2(g)+NaCl(s)
 NaNO3(s)+NOCl(g) K1 ΔH1<0 (Ⅰ)
NaNO3(s)+NOCl(g) K1 ΔH1<0 (Ⅰ)2NO(g)+Cl2(g)
 2NOCl(g) K2 ΔH2<0 (Ⅱ)
2NOCl(g) K2 ΔH2<0 (Ⅱ)(1)4NO2(g)+2NaCl(s)
 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol Cl2,10 min时反应(Ⅱ)达到平衡。测得10 min内v(NOCl)=7.5×10-3 mol·L-1·min-1,则平衡后n(Cl2)=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】利用CO和水蒸气可生产 ,反应方程式为:
,反应方程式为: 。将
。将 和
和 分别通入2L的恒容密闭容器中进行如下反应,记录部分数据如下表所示:
分别通入2L的恒容密闭容器中进行如下反应,记录部分数据如下表所示:
回答下列问题:
(1)表中x=_______ ;y=_______ 。
(2)650℃时,从开始反应到平衡,反应速率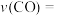
_______  。
。
(3)900℃时,用各物质的平衡浓度表示该反应的平衡常数为_______ 。
(4)由以上信息可知,该反应的正反应为_______ 反应(选填“放热”或“吸热”),原因是_______ 。
 ,反应方程式为:
,反应方程式为: 。将
。将 和
和 分别通入2L的恒容密闭容器中进行如下反应,记录部分数据如下表所示:
分别通入2L的恒容密闭容器中进行如下反应,记录部分数据如下表所示:| 温度/℃ | 起始量物质的量/mol | 达平衡 | |||
| CO |  |  的物质的量/mol 的物质的量/mol | CO转化率 | 时间/min | |
| 650 | 3 | 2 | 1.5 | x | 10 |
| 900 | 2 | 2 | y | 40% | 5 |
回答下列问题:
(1)表中x=
(2)650℃时,从开始反应到平衡,反应速率
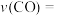
 。
。(3)900℃时,用各物质的平衡浓度表示该反应的平衡常数为
(4)由以上信息可知,该反应的正反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
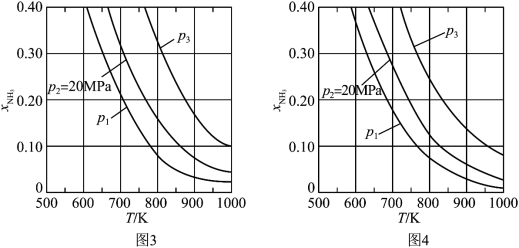
【推荐2】氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如下图所示。其中一种进料组成为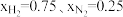 ,另一种为
,另一种为 。(物质i的摩尔分数:
。(物质i的摩尔分数: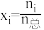 )
)_______ ,判断的依据是_______ 。
(2)进料组成中含有惰性气体 的图是
的图是_______ 。
(3)图3中,当 、
、 时,氮气的转化率
时,氮气的转化率
_______ 。该温度时,反应 N2(g)+
N2(g)+ H2(g)⇌NH3(g)的平衡常数
H2(g)⇌NH3(g)的平衡常数
_______  (化为最简式)。
(化为最简式)。
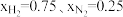 ,另一种为
,另一种为 。(物质i的摩尔分数:
。(物质i的摩尔分数: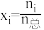 )
)
(2)进料组成中含有惰性气体
 的图是
的图是(3)图3中,当
 、
、 时,氮气的转化率
时,氮气的转化率
 N2(g)+
N2(g)+ H2(g)⇌NH3(g)的平衡常数
H2(g)⇌NH3(g)的平衡常数
 (化为最简式)。
(化为最简式)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】过氧乙酸( CH3COOOH)是一种高效消毒剂,常温下易分解,可由乙酸与H2O2在硫酸催化下反应制得,化学方程式为CH3COOH(aq)+H2O2(aq) CH3COOOH(aq)+H2O(l)。
CH3COOOH(aq)+H2O(l)。
(1)该反应的能量变化如图所示。

①该反应为____________ (填“放热” 或“吸热”)反应。
②制备38 g CH3COOOH时,热量变化为6.85 kJ,则E =________ 。
(2)取a g冰醋酸和a g 50% H2O2混合均匀,加入一定量硫酸,测得混合溶液的体积为2 L。在25 °C时,测得不同时刻,溶液中的n(CH3COOOH)变化如图所示(反应前后溶液体积变化忽略不计)。
①0 ~6 h内,v(CH3COOOH)=______ 。
②若反应前后溶液的质量没有发生变化,则反应进行到6 h时,H2O2的转化率为____ 。
③若在40 °C下进行该实验,测得不同时刻n(CH3COOOH)均有所降低,可能的原因为____________ 。
 CH3COOOH(aq)+H2O(l)。
CH3COOOH(aq)+H2O(l)。(1)该反应的能量变化如图所示。

①该反应为
②制备38 g CH3COOOH时,热量变化为6.85 kJ,则E =
(2)取a g冰醋酸和a g 50% H2O2混合均匀,加入一定量硫酸,测得混合溶液的体积为2 L。在25 °C时,测得不同时刻,溶液中的n(CH3COOOH)变化如图所示(反应前后溶液体积变化忽略不计)。
①0 ~6 h内,v(CH3COOOH)=
②若反应前后溶液的质量没有发生变化,则反应进行到6 h时,H2O2的转化率为
③若在40 °C下进行该实验,测得不同时刻n(CH3COOOH)均有所降低,可能的原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】含硫化合物是实验室和工业上的常用化学品。请回答:
(1)实验室可用铜与浓硫酸反应制备少量SO2:Cu(s)+2H2SO4(l)=CuSO4(s)+SO2(g)+2H2O(l) ΔH=−11.9kJ·mol-1。判断该反应的自发性并说明理由___________ 。
(2)已知2SO2(g)+O2 2SO3(g) ΔH=−198kJ·mol-1,850K时,在恒容密闭反应器中充入一定量的SO2和O2,10分钟反应达到平衡后测得SO2、O2和SO3的浓度分别为6.0×10-3mol·L-1、8.0×10-3mol·L-1和4.4×10-2mol·L-1。
2SO3(g) ΔH=−198kJ·mol-1,850K时,在恒容密闭反应器中充入一定量的SO2和O2,10分钟反应达到平衡后测得SO2、O2和SO3的浓度分别为6.0×10-3mol·L-1、8.0×10-3mol·L-1和4.4×10-2mol·L-1。
①反应开始到第10分钟,SO3反应速率为________ 。
②该温度下反应的平衡常数为________ 。
③平衡时SO2的转化率为________ 。
(3)工业上主要采用接触法用含硫矿石制备硫酸。其主要工艺是焙烧、炉气精制、用钒做催化剂将SO2氧化成SO3、吸收等。结合本大题的信息,完成下题。
①下列说法正确的是______ 。
a.须采用高温高压的反应条件使SO2氧化为SO3
b.通入过量的空气可以提高含硫矿石和SO2的转化率
c.进入接触室之前的气流无需净化处理
②在焙烧前要将硫铁矿粉碎,这样做的目的是______ 。
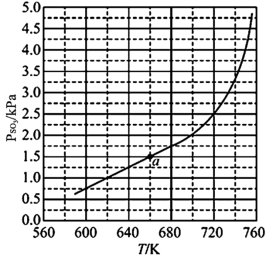
(4)将FeSO4置入抽空的刚性容器中,升高温度发生分解反应:2FeSO4(s) Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ),平衡时P(SO3)-T的关系如下图所示。660K时,该反应的平衡总压P(总)
Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ),平衡时P(SO3)-T的关系如下图所示。660K时,该反应的平衡总压P(总)_____ kPa,Kp(Ⅰ)随反应温度升高而_____ (填“增大”“减小”或“不变”)。
(1)实验室可用铜与浓硫酸反应制备少量SO2:Cu(s)+2H2SO4(l)=CuSO4(s)+SO2(g)+2H2O(l) ΔH=−11.9kJ·mol-1。判断该反应的自发性并说明理由
(2)已知2SO2(g)+O2
 2SO3(g) ΔH=−198kJ·mol-1,850K时,在恒容密闭反应器中充入一定量的SO2和O2,10分钟反应达到平衡后测得SO2、O2和SO3的浓度分别为6.0×10-3mol·L-1、8.0×10-3mol·L-1和4.4×10-2mol·L-1。
2SO3(g) ΔH=−198kJ·mol-1,850K时,在恒容密闭反应器中充入一定量的SO2和O2,10分钟反应达到平衡后测得SO2、O2和SO3的浓度分别为6.0×10-3mol·L-1、8.0×10-3mol·L-1和4.4×10-2mol·L-1。①反应开始到第10分钟,SO3反应速率为
②该温度下反应的平衡常数为
③平衡时SO2的转化率为
(3)工业上主要采用接触法用含硫矿石制备硫酸。其主要工艺是焙烧、炉气精制、用钒做催化剂将SO2氧化成SO3、吸收等。结合本大题的信息,完成下题。
①下列说法正确的是
a.须采用高温高压的反应条件使SO2氧化为SO3
b.通入过量的空气可以提高含硫矿石和SO2的转化率
c.进入接触室之前的气流无需净化处理
②在焙烧前要将硫铁矿粉碎,这样做的目的是
(4)将FeSO4置入抽空的刚性容器中,升高温度发生分解反应:2FeSO4(s)
 Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ),平衡时P(SO3)-T的关系如下图所示。660K时,该反应的平衡总压P(总)
Fe2O3(s)+SO2(g)+SO3(g) (Ⅰ),平衡时P(SO3)-T的关系如下图所示。660K时,该反应的平衡总压P(总)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】一定条件下,在体积为5 L的密闭容器中,A、B、C三种气体的物质的量n(mol)随时间t(min)的变化如图1所示。已知达平衡后,降低温度,A的体积分数将减小。
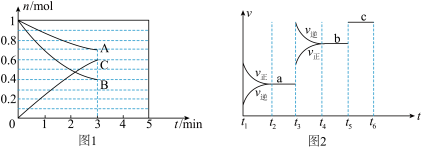
(1)该反应的化学方程式为__________________ ,此反应平衡常数的表达式为K=________ 。
(2)从开始到最初达到平衡,C的平均反应速率v(C)=________________ 。3min时,A的转化率=________ %。该反应的
________ 0。(填“ ”、“
”、“ ”或“
”或“ ”)
”)
(3)对于该反应改变某些条件,化学反应速率及化学平衡状态可能会发生变化,请回答:
①恒温恒容充入惰性气体,平衡______ 移动(填“正向”、“逆向”或“不”,下同)
②恒温恒压充入惰性气体,平衡______ 移动,化学反应速率_______ (填“加快”或“减慢”)
③升高温度,平衡______ 移动。
(4)该反应的反应速率v随时间t的关系如图2所示:
①根据图2判断,在t3时刻改变的外界条件是_______ ,t5时刻改变的外界条件是_______ 。
②a、b、c三个阶段中,C的体积分数最大的是________ ,
③a、b、c三个阶段的平衡常数分别用K1、K2、K3表示则:K1、K2、K3之间的关系为___________ (用“ ”、“
”、“ ”或“
”或“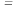 ”连接)。
”连接)。

(1)该反应的化学方程式为
(2)从开始到最初达到平衡,C的平均反应速率v(C)=

 ”、“
”、“ ”或“
”或“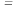 ”)
”)(3)对于该反应改变某些条件,化学反应速率及化学平衡状态可能会发生变化,请回答:
①恒温恒容充入惰性气体,平衡
②恒温恒压充入惰性气体,平衡
③升高温度,平衡
(4)该反应的反应速率v随时间t的关系如图2所示:
①根据图2判断,在t3时刻改变的外界条件是
②a、b、c三个阶段中,C的体积分数最大的是
③a、b、c三个阶段的平衡常数分别用K1、K2、K3表示则:K1、K2、K3之间的关系为
 ”、“
”、“ ”或“
”或“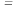 ”连接)。
”连接)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】运用化学反应原理知识研究如何利用CO、SO2等污染物有重要意义。
(1)用CO可以合成甲醇,CO(g)+2H2(g) CH3OH(g) 下列措施中能够增大上述合成甲醇反应的反应速率的是
CH3OH(g) 下列措施中能够增大上述合成甲醇反应的反应速率的是________ (填写序号).
a.使用高效催化剂 b.降低反应温度
c.增大体系压强 d.不断将CH3OH从反应混合物中分离出来
(2)在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如右图所示。
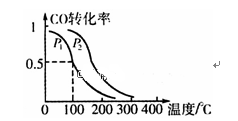
①p1________ p2(填“大于”、“小于”或“等于”);
②100 ℃时,该反应的化学平衡常数K=_______ ;
③100℃时,达到平衡后,保持压强P1不变的情况下,向容器中通入CO、H2和CH3OH各0.5amol,则平衡______ (填“向右”、“向左”或“不”移动)
④在其它条件不变的情况下,再增加a mol CO和2a molH2,达到新平衡时,CO的转化率______ (填“增大”、“减小”或“不变”)。
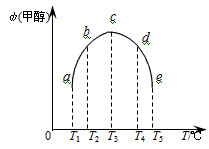
(3)在容积均为1L的密闭容器(a、b、c、d、e)中,分别充入1molCO和2molH2等量混合气体,在不同的温度下(温度分别为T1、T2、T3、T4、T5),经相同的时间,在t时刻,测得容器甲醇的体积分数如图所示。在T1-T2及T4-T5两个温度区间,容器内甲醇的体积分数的变化趋势如图所示,其原因是______ 。
(1)用CO可以合成甲醇,CO(g)+2H2(g)
 CH3OH(g) 下列措施中能够增大上述合成甲醇反应的反应速率的是
CH3OH(g) 下列措施中能够增大上述合成甲醇反应的反应速率的是a.使用高效催化剂 b.降低反应温度
c.增大体系压强 d.不断将CH3OH从反应混合物中分离出来
(2)在一定压强下,容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡转化率与温度、压强的关系如右图所示。

①p1
②100 ℃时,该反应的化学平衡常数K=
③100℃时,达到平衡后,保持压强P1不变的情况下,向容器中通入CO、H2和CH3OH各0.5amol,则平衡
④在其它条件不变的情况下,再增加a mol CO和2a molH2,达到新平衡时,CO的转化率
(3)在容积均为1L的密闭容器(a、b、c、d、e)中,分别充入1molCO和2molH2等量混合气体,在不同的温度下(温度分别为T1、T2、T3、T4、T5),经相同的时间,在t时刻,测得容器甲醇的体积分数如图所示。在T1-T2及T4-T5两个温度区间,容器内甲醇的体积分数的变化趋势如图所示,其原因是

您最近一年使用:0次



