解题方法
1 . 室温下,向10mL浓度均为0.1mol/L的CuCl2、FeCl2和ZnCl2溶液中分别滴加等浓度的Na2S溶液,滴加过程中pc[pc=-lgc(M2+),M2+为Cu2+或Fe2+或Zn2+]与Na2S溶液体积的关系如图所示。已知:Ksp(CuS)<Ksp(ZnS),Ksp(FeS)=6.25×10-18,lg25=1.4。下列说法正确的是
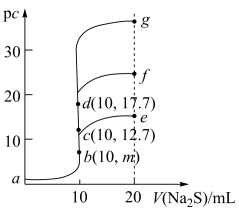

| A.m=8.6 |
| B.a点的CuCl2溶液中:2c(Cu2+)>c(Cl−)+c(OH−) |
| C.a→d→g的过程中,水的电离程度经历由大到小后又增大的过程 |
| D.将足量晶体ZnCl2加入0.1mol/L的Na2S溶液中,c(Zn2+)最大可达到10−24.4mol·L−1 |
您最近一年使用:0次
2 . 常温下,向20mL等浓度的NaCl溶液和Na2CrO4溶液中分别滴加AgNO3溶液,滴加过程中pCl=-lg c(Cl-)、pCr=-lg c(CrO )随AgNO3溶液体积变化如图。下列说法错误的是
)随AgNO3溶液体积变化如图。下列说法错误的是

 )随AgNO3溶液体积变化如图。下列说法错误的是
)随AgNO3溶液体积变化如图。下列说法错误的是
| A.AgNO3溶液的浓度为0.01mol·L-1 |
| B.L1代表pCr随AgNO3溶液体积变化的曲线 |
| C.Ksp(AgCl)的数量级为1×10-10 |
| D.若将原溶液浓度均降低一倍,图中b点将移动至c点 |
您最近一年使用:0次
3 . 某温度下,分别向10mL浓度均为0.1mol·L-1的CuCl2和ZnCl2溶液中滴加0.1mol·L-1的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)和-lgc(Zn2+)与Na2S溶液体积(V)的关系如图所示。[已知:Ksp(ZnS)>Ksp(CuS), 1g3≈0.5],下列说法正确的是
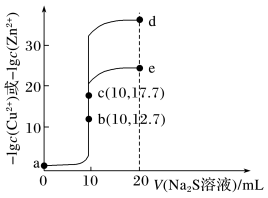

| A.a点的ZnCl2溶液中:c(Cl-)<2[c(Zn2+)+c(H+)] |
| B.由图象可以计算得出该温度下Ksp(ZnS)=10-35.4 |
| C.a—b—e为滴定CuCl2溶液的曲线 |
| D.d点纵坐标约为33.9 |
您最近一年使用:0次
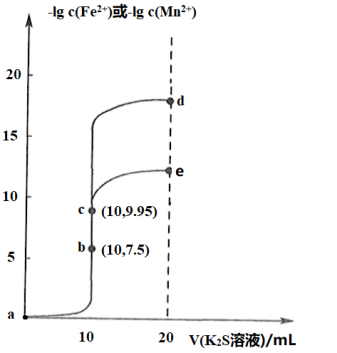
4 . 常温下,分别向体积均为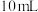 、浓度均为
、浓度均为 的
的 和
和 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中溶液
溶液,滴加过程中溶液 和
和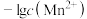 与滴入
与滴入 溶液体积(
溶液体积( )的关系如图所示。[已知:
)的关系如图所示。[已知: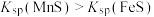 ,
, ,忽略溶液混合时温度和体积的变化],下列说法错误的是
,忽略溶液混合时温度和体积的变化],下列说法错误的是
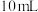 、浓度均为
、浓度均为 的
的 和
和 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中溶液
溶液,滴加过程中溶液 和
和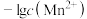 与滴入
与滴入 溶液体积(
溶液体积( )的关系如图所示。[已知:
)的关系如图所示。[已知: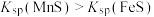 ,
, ,忽略溶液混合时温度和体积的变化],下列说法错误的是
,忽略溶液混合时温度和体积的变化],下列说法错误的是
A.加入过量难溶 可除去 可除去 溶液中混有的 溶液中混有的 |
| B.e点纵坐标约为13.5 |
C.d点钾离子的物质的量浓度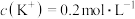 |
| D.溶液的pH:d>c>a |
您最近一年使用:0次
名校
解题方法
5 . 某温度下,分别向20mL浓度均为xmol/L的NaCl和Na2CrO4溶液中滴加0.1mol/AgNO3溶液,滴加过程中-lgc(Cl-)和-lgc(CrO )与AgNO3溶液的体积关系如图所示。下列说法不正确的是
)与AgNO3溶液的体积关系如图所示。下列说法不正确的是

 )与AgNO3溶液的体积关系如图所示。下列说法不正确的是
)与AgNO3溶液的体积关系如图所示。下列说法不正确的是
| A.x=0.1 |
| B.曲线Ⅰ代表NaCl溶液 |
| C.Ksp(Ag2CrO4)约为2×10-8 |
| D.y=9 |
您最近一年使用:0次
6 .  时,
时, 的
的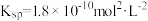 ,
, 在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
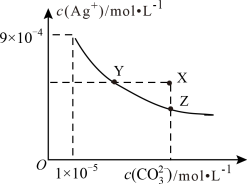
 时,
时, 的
的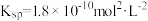 ,
, 在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是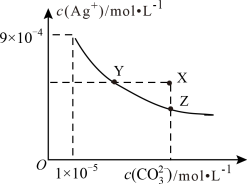
A. 的 的 为 为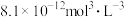 |
B.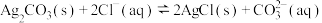 的平衡常数 的平衡常数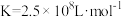 |
C.向 的饱和溶液中加入 的饱和溶液中加入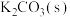 ,可使 ,可使 增大(由Y点到X点) 增大(由Y点到X点) |
D.向同浓度的 和 和 的混合溶液中滴入 的混合溶液中滴入 溶液, 溶液, 先沉淀 先沉淀 |
您最近一年使用:0次
2020-09-13更新
|
295次组卷
|
3卷引用:鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3节综合训练
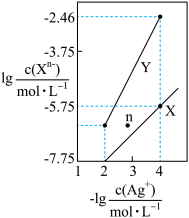
7 . 常温下,用AgNO3溶液分别滴定浓度均为0.01mol•L-1的KCl、K2C2O4溶液,所得的沉淀溶解平衡图象如图所示(不考虑C2O 的水解)。已知Ksp(AgCl)数量级为10-10。下列叙述不正确的是( )
的水解)。已知Ksp(AgCl)数量级为10-10。下列叙述不正确的是( )
 的水解)。已知Ksp(AgCl)数量级为10-10。下列叙述不正确的是( )
的水解)。已知Ksp(AgCl)数量级为10-10。下列叙述不正确的是( )
| A.Ksp(Ag2C2O4)数量级为10-11 |
| B.n点表示Ag2C2O4的过饱和溶液 |
C.向c(Cl-)=c(C2O )的混合液中滴入AgNO3溶液时,先生成AgCl沉淀 )的混合液中滴入AgNO3溶液时,先生成AgCl沉淀 |
D.Ag2C2O4(s)+2Cl-(aq) 2AgCl(s)+C2O 2AgCl(s)+C2O (aq)的平衡常数为10-0.71 (aq)的平衡常数为10-0.71 |
您最近一年使用:0次
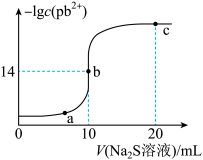
8 . 某温度下,向

 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中
溶液,滴加过程中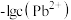 与
与 溶液体积的关系如图所示。下列有关说法正确的是
溶液体积的关系如图所示。下列有关说法正确的是


 溶液中滴加
溶液中滴加 的
的 溶液,滴加过程中
溶液,滴加过程中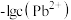 与
与 溶液体积的关系如图所示。下列有关说法正确的是
溶液体积的关系如图所示。下列有关说法正确的是
A.该温度下,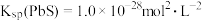 |
| B.a、b、c三点对应的溶液中,水的电离程度最小的为a点 |
C.若改用  溶液,b点应该水平左移 溶液,b点应该水平左移 |
D.若改用  溶液,b点移向右下方 溶液,b点移向右下方 |
您最近一年使用:0次
9 . 水垢中含有的 CaSO4,可先用 Na2CO3 溶液处理,使之转化为疏松、易溶于酸的 CaCO3。某化学兴趣小组用某浓度的 Na2CO3 溶液处理一定量的 CaSO4 固体,测得所加 Na2CO3 溶液体积与溶液中-lgc(CO32-)的关系如下:
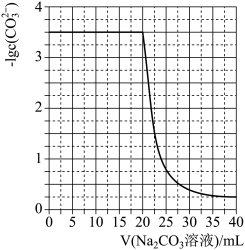
已知Ksp(CaSO4)=9×10-6,Ksp(CaCO3)=3×10-9,lg3=0.5,下列说法不正确的是

已知Ksp(CaSO4)=9×10-6,Ksp(CaCO3)=3×10-9,lg3=0.5,下列说法不正确的是
A.曲线上各点的溶液满足关系式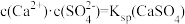 |
B.CaSO4(s)+  (aq) (aq) CaCO3(s)+ CaCO3(s)+ (aq)K=3×103 (aq)K=3×103 |
| C.该Na2CO3溶液的浓度为1.5 mol/L |
| D.相同实验条件下,若将Na2CO3溶液的浓度改为原浓度的2倍,则上图曲线整体向上平移1个单位即可 |
您最近一年使用:0次



