1 . 常温下,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的
的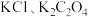 溶液,所得的沉淀溶解平衡图像如图所示(不考虑
溶液,所得的沉淀溶解平衡图像如图所示(不考虑 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是

 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的
的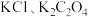 溶液,所得的沉淀溶解平衡图像如图所示(不考虑
溶液,所得的沉淀溶解平衡图像如图所示(不考虑 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是
| A.n点表示AgCl的不饱和溶液 |
B. 的数量级等于 的数量级等于 |
C.向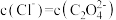 的混合液中滴入 的混合液中滴入 溶液时,先生成 溶液时,先生成 沉淀 沉淀 |
D.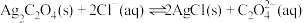 的平衡常数为 的平衡常数为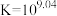 |
您最近一年使用:0次
2 . 已知p(A)=-lgc(A)。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是


| A.a点有ZnS沉淀生成 |
| B.可用MnS除去MnCl2溶液中混有的少量ZnCl2 |
| C.向CuS悬浊液中加入少量水,平衡向溶解的方向移动,c(S2-)减小 |
D.CuS和MnS共存的悬浊液中,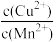 =10-20 =10-20 |
您最近一年使用:0次
3 . 已知 p(A)=-lgc平(A)。三种金属硫化物在水中的沉淀溶解平衡曲线如图 所示。下列说法不正确的是


| A.a 点有 ZnS 沉淀生成 |
| B.可用 MnS 除去 MnCl2溶液中混有的少量 ZnCl2 |
| C.向 CuS 悬浊液中加入少量水,平衡向溶解的方向移动,c平(S2-)增大 |
D.CuS 和 MnS 共存的悬浊液中,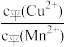 =10-20 =10-20 |
您最近一年使用:0次
2022高三·全国·专题练习
4 . 某元素M的氢氧化物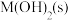 在水中的溶解反应为:
在水中的溶解反应为: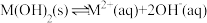 、
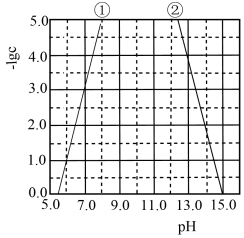
、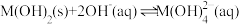 ,25℃,-lgc与pH的关系如图所示,c为
,25℃,-lgc与pH的关系如图所示,c为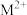 或
或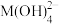 浓度的值。下列说法
浓度的值。下列说法错误 的是
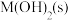 在水中的溶解反应为:
在水中的溶解反应为: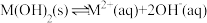 、
、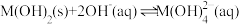 ,25℃,-lgc与pH的关系如图所示,c为
,25℃,-lgc与pH的关系如图所示,c为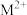 或
或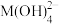 浓度的值。下列说法
浓度的值。下列说法
A.曲线①代表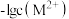 与pH的关系 与pH的关系 |
B.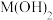 的 的 约为 约为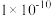 |
C.向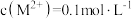 的溶液中加入NaOH溶液至pH=9.0,体系中元素M主要以 的溶液中加入NaOH溶液至pH=9.0,体系中元素M主要以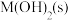 存在 存在 |
D.向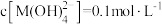 的溶液中加入等体积0.4mol/L的HCl后,体系中元素M主要以 的溶液中加入等体积0.4mol/L的HCl后,体系中元素M主要以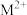 存在 存在 |
您最近一年使用:0次
2022-07-04更新
|
6862次组卷
|
14卷引用:2022年海南省高考真题化学试题
2022年海南省高考真题化学试题(已下线)专题10 水溶液中的离子平衡-2022年高考真题模拟题分项汇编(已下线)第15练 以Ksp的计算突破溶解平衡-2022年【暑假分层作业】高二化学(2023届一轮复习通用)(已下线)2022年海南省高考真题变式题1-14(已下线)第26讲 难溶电解质的溶解平衡(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题06 水溶液中的离子平衡(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)安徽省六安第一中学2022-2023学年高二上学期期末考试化学试题(已下线)题型27 沉淀溶解平衡常数及其应用图象(已下线)第15练 水溶液中的离子平衡图像分析 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点29 沉淀溶解平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题12 水溶液中的离子反应与平衡-2023年高考化学真题题源解密(全国通用)第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 第2课时 沉淀溶解平衡的应用(已下线)第6讲 沉淀溶解平衡图像分析
5 . 已知CaF2是难溶于水、可溶于酸的盐。常温下,用盐酸调节CaF2浊液的pH,测得在不同pH条件下,体系中 与-lgc(X)(X为Ca2+或F- )的关系如图所示。
与-lgc(X)(X为Ca2+或F- )的关系如图所示。
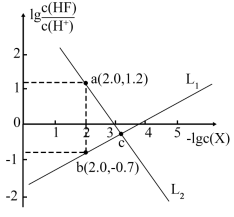
下列说法错误的是
 与-lgc(X)(X为Ca2+或F- )的关系如图所示。
与-lgc(X)(X为Ca2+或F- )的关系如图所示。
下列说法错误的是
A.L1表示-lgc(F- )与 的变化曲线 的变化曲线 |
| B.K sp(CaF2 )的数量级为10-10 |
| C.c点的溶液中: c(Cl-)<c(Ca2+) |
| D.a、b、c三点的溶液中: 2c(Ca2+)=c(F- )+c(HF) |
您最近一年使用:0次
6 . 常温下,分别向体积均为10mL,浓度均为0.1mol·L-1的KSCN溶液、K2CrO4溶液滴加0.1mol·L-1AgNO3溶液,溶液中酸根离子浓度负对数(pM)与AgNO3溶液体积的关系如图[已知:pM=-lg(SCN-)或-lgc(CrO )]。下列说法正确的是
)]。下列说法正确的是
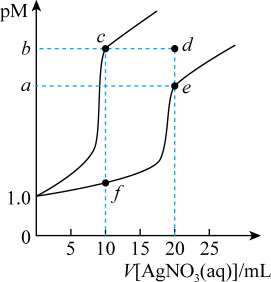
 )]。下列说法正确的是
)]。下列说法正确的是
| A.溶解度:AgSCN>Ag2CrO4 | B.Ksp(Ag2CrO4)=4×10-3a |
| C.d点Ag2CrO4溶液是不饱和溶液 | D.c(Ag+):f点溶液>e点溶液 |
您最近一年使用:0次
2022-05-20更新
|
334次组卷
|
4卷引用:湖南省多所学校2022年普通高中学业水平仿真模拟化学试题
湖南省多所学校2022年普通高中学业水平仿真模拟化学试题(已下线)专题10 水溶液中的离子平衡-2022年高考真题模拟题分项汇编湖南省株洲市第一中学2022-2023学年高二上学期期中考试化学试题(已下线)河北省石家庄市2022届高三毕业班教学质量检测二(一模)(不定项选择题)
解题方法
7 . 常温下,难溶盐 的饱和溶液中
的饱和溶液中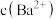 随
随 的变化关系如图所示。下列叙述正确的是(忽略
的变化关系如图所示。下列叙述正确的是(忽略 第二步水解)
第二步水解)

 的饱和溶液中
的饱和溶液中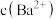 随
随 的变化关系如图所示。下列叙述正确的是(忽略
的变化关系如图所示。下列叙述正确的是(忽略 第二步水解)
第二步水解)
A. |
B.常温下 的 的 |
C.a点溶液: |
D.溶液 时, 时, |
您最近一年使用:0次
8 .  时,用
时,用 溶液分别滴定
溶液分别滴定 三种溶液,
三种溶液, [p表示负对数,M表示
[p表示负对数,M表示 ]随
]随 变化关系如图所示,已知
变化关系如图所示,已知 ,一般认为当溶液中离子浓度
,一般认为当溶液中离子浓度 时,该离子沉淀完全。下列有关分析正确的是
时,该离子沉淀完全。下列有关分析正确的是

 时,用
时,用 溶液分别滴定
溶液分别滴定 三种溶液,
三种溶液, [p表示负对数,M表示
[p表示负对数,M表示 ]随
]随 变化关系如图所示,已知
变化关系如图所示,已知 ,一般认为当溶液中离子浓度
,一般认为当溶液中离子浓度 时,该离子沉淀完全。下列有关分析正确的是
时,该离子沉淀完全。下列有关分析正确的是 
A.②代表滴定 溶液的变化关系 溶液的变化关系 |
B.滴定 溶液至a点时,溶液中 溶液至a点时,溶液中 |
C.滴定 溶液至 溶液至 时,溶液中: 时,溶液中: |
D.如果完全除去工业废水中的 ,需要调节溶液的 ,需要调节溶液的 |
您最近一年使用:0次
9 . 已知锌及其化合物的性质与铝及其化合物相似。如图横坐标为溶液的pH,纵坐标为 或
或 的物质的量浓度的对数。25℃时,下列说法中不正确的是
的物质的量浓度的对数。25℃时,下列说法中不正确的是

 或
或 的物质的量浓度的对数。25℃时,下列说法中不正确的是
的物质的量浓度的对数。25℃时,下列说法中不正确的是
A.往 溶液中加入过量氢氧化钠溶液,反应的离子方程式为 溶液中加入过量氢氧化钠溶液,反应的离子方程式为 |
| B.若要从某废液中完全沉淀Zn2+,通常可以调控该溶液的pH在8.0~10.0之间 |
| C.pH=8.0与pH=12.0的两种废液中,Zn2+浓度之比为108 |
D.该温度时, 的溶度积常数 的溶度积常数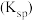 为 为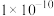 |
您最近一年使用:0次
10 . T℃ ,分别向10 mL浓度均为0.1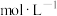 的
的 和
和 溶液中滴0.1
溶液中滴0.1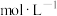 的
的 溶液,滴的过程中
溶液,滴的过程中 和
和 与
与 溶液体积(V)的关系如图所示[已知:
溶液体积(V)的关系如图所示[已知: ]。下列有关说法错误的是
]。下列有关说法错误的是

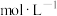 的
的 和
和 溶液中滴0.1
溶液中滴0.1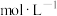 的
的 溶液,滴的过程中
溶液,滴的过程中 和
和 与
与 溶液体积(V)的关系如图所示[已知:
溶液体积(V)的关系如图所示[已知: ]。下列有关说法错误的是
]。下列有关说法错误的是
A.a~b~d为滴定 溶液的曲线 溶液的曲线 |
| B.对应溶液pH:a<b<e |
C.a点对应的 溶液中: 溶液中: |
| D.d点纵坐标约为23.9 |
您最近一年使用:0次



