1 . 秦俑彩绘中含有白色的 和黄色的
和黄色的 。常温下,
。常温下, 和
和 在不同溶液中分别达到溶解平衡时
在不同溶液中分别达到溶解平衡时 (阳离子浓度的负对数)与
(阳离子浓度的负对数)与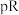 (阴离子浓度的负对数)的关系如图所示。下列说法正确的是
(阴离子浓度的负对数)的关系如图所示。下列说法正确的是
 和黄色的
和黄色的 。常温下,
。常温下, 和
和 在不同溶液中分别达到溶解平衡时
在不同溶液中分别达到溶解平衡时 (阳离子浓度的负对数)与
(阳离子浓度的负对数)与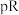 (阴离子浓度的负对数)的关系如图所示。下列说法正确的是
(阴离子浓度的负对数)的关系如图所示。下列说法正确的是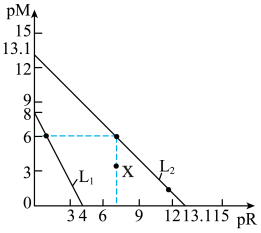
A. 表示 表示 达到沉淀溶解平衡时 达到沉淀溶解平衡时 与 与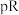 的关系 的关系 |
B.在 的 的 溶液中, 溶液中, 的溶解度为 的溶解度为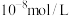 |
C.对于分散质 , , 点: 点: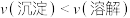 |
D.向浓度均为 的 的 的混合溶液中滴入 的混合溶液中滴入 溶液,先产生白色沉淀 溶液,先产生白色沉淀 |
您最近一年使用:0次
2 . 工业上常用H2S处理废水中的Ni2+和Cd2+,对其工艺条件进行研究。处理过程中始终保持H2S饱和,即c(H2S)=0.1 mol∙L–1,在一定pH范围内,溶液中HS–、S2–、Ni2+和Cd2+浓度的—lg(c/mol·L–1)随pH的变化关系如图,已知pH=2时溶液中仅有CdS沉淀生成,下列说法正确的是


| A.X点:c(H+)>c(Cd2+)=c(S2—) |
| B.Ka2(H2S)=10–14.6 |
| C.m=9.2 |
D.反应Cd2+(aq)+HS—(aq) CdS(s)+H+(aq)的平衡常数K=10–11.4(mol·L–1)–1 CdS(s)+H+(aq)的平衡常数K=10–11.4(mol·L–1)–1 |
您最近一年使用:0次
名校
解题方法
3 . T℃时, 和
和 的沉淀溶解平衡曲线如图所示。已知:
的沉淀溶解平衡曲线如图所示。已知: ,
, 或
或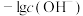 。下列说法正确的是
。下列说法正确的是

 和
和 的沉淀溶解平衡曲线如图所示。已知:
的沉淀溶解平衡曲线如图所示。已知: ,
, 或
或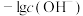 。下列说法正确的是
。下列说法正确的是
A.T℃时, |
B.Y点对应的 溶液是不饱和溶液 溶液是不饱和溶液 |
C.Z点对应的溶液中,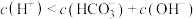 |
D.向 悬浊液中通入 悬浊液中通入 气体(忽略溶液体积的变化),溶液中 气体(忽略溶液体积的变化),溶液中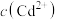 保持不变 保持不变 |
您最近一年使用:0次
4 . 常温下,将0.05mol BaSO4粉末置于盛有1L蒸馏水的烧杯中,向烧杯中加入Na2CO3固体(忽略溶液体积变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中各离子浓度变化曲线如图所示。已知:lg2=0.3;lg2.5=0.4;lg5=0.7,下列说法错误的是
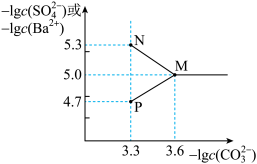

| A.图中表示c(Ba2+)的曲线是MN |
B.P点溶液中离子浓度大小为: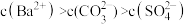 |
C.常温下 的平衡常数的数量级为10-2 的平衡常数的数量级为10-2 |
| D.若使0.05mol BaSO4全部转化为BaCO3,至少要加入1.25mol Na2CO3 |
您最近一年使用:0次
2023-07-23更新
|
353次组卷
|
2卷引用:山东省济南市2022-2023学年高三上学期1月期末考试化学试题
5 . 某温度下,向含 与
与 的混合液中滴加
的混合液中滴加 溶液实现
溶液实现 和
和 的逐级沉淀分离,测得
的逐级沉淀分离,测得 与
与 的关系如图所示。已知该温度下
的关系如图所示。已知该温度下 ,下列说法错误是
,下列说法错误是
 与
与 的混合液中滴加
的混合液中滴加 溶液实现
溶液实现 和
和 的逐级沉淀分离,测得
的逐级沉淀分离,测得 与
与 的关系如图所示。已知该温度下
的关系如图所示。已知该温度下 ,下列说法错误是
,下列说法错误是
A.曲线①表示 与 与 的关系 的关系 |
B.沉淀过程中首先析出的是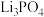 |
C.该温度下, 沉淀转化反应的平衡常数的值为 沉淀转化反应的平衡常数的值为 |
D.为提高磷酸锂的纯度,沉淀过程中需严格控制 的量和溶液的 的量和溶液的 |
您最近一年使用:0次
6 .  、
、 均是难溶物,用pM、pOH、
均是难溶物,用pM、pOH、 分别表示
分别表示 、
、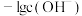 、
、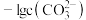 。一定温度下,
。一定温度下, 、
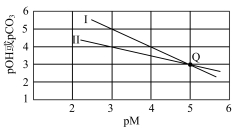
、 的沉淀溶解平衡曲线如图所示。下列说法正确的是
的沉淀溶解平衡曲线如图所示。下列说法正确的是
 、
、 均是难溶物,用pM、pOH、
均是难溶物,用pM、pOH、 分别表示
分别表示 、
、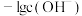 、
、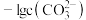 。一定温度下,
。一定温度下, 、
、 的沉淀溶解平衡曲线如图所示。下列说法正确的是
的沉淀溶解平衡曲线如图所示。下列说法正确的是
A.Ⅰ表示 的沉淀溶解平衡曲线 的沉淀溶解平衡曲线 |
B. 的 的 是 是 |
C.Q点可通过 和 和 的混合物溶于水得到 的混合物溶于水得到 |
D.同时存在 和 和 固体的溶液中 固体的溶液中 |
您最近一年使用:0次
7 . 已知p(A)=-lgc(A)。三种金属硫化物在水中的沉淀溶解平衡曲线如图所示。下列说法不正确的是
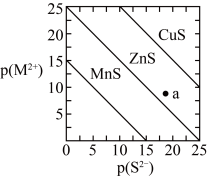

| A.可用MnS除去MnCl2溶液中混有的少量ZnCl2 |
| B.a点有ZnS沉淀生成 |
C.CuS和MnS共存的悬浊液中,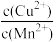 =10-20 =10-20 |
| D.向CuS悬浊液中加入少量水,平衡向溶解的方向移动,c(S2-)增大 |
您最近一年使用:0次
8 . 某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
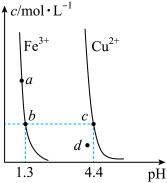

| A.Ksp[Fe(OH)3]<Ksp[Cu(OH)2] |
| B.c、d两点代表的溶液中c(H+)与c(OH-)乘积不相等 |
| C.加适量NH4Cl固体可使溶液由a点变到b点 |
| D.在b、c两点代表的溶液中Fe(OH)3、Cu(OH)2均达到饱和 |
您最近一年使用:0次
9 . 25℃时,用NaOH溶液分别滴定弱酸HA、CuSO4、FeSO4三种溶液,pM随pH变化关系如图所示[p表示负对数,M表示 、c(Cu2+)、c(Fe2+)等],已知Ksp[Cu(OH)2]<Ksp[Fe(OH)2],下列有关分析错误的是
、c(Cu2+)、c(Fe2+)等],已知Ksp[Cu(OH)2]<Ksp[Fe(OH)2],下列有关分析错误的是

 、c(Cu2+)、c(Fe2+)等],已知Ksp[Cu(OH)2]<Ksp[Fe(OH)2],下列有关分析错误的是
、c(Cu2+)、c(Fe2+)等],已知Ksp[Cu(OH)2]<Ksp[Fe(OH)2],下列有关分析错误的是
| A.①代表滴定FeSO4溶液的变化关系 |
| B.调整溶液的pH=7,可使工业废水中的Cu2+沉淀完全 |
| C.a点对应的pH=8 |
| D.Fe(OH)2固体难溶解于HA溶液 |
您最近一年使用:0次
名校
解题方法
10 . 某温度下,FeS的水溶液中存在平衡 ,其沉淀溶解平衡曲线如图所示。下列说法正确的是
,其沉淀溶解平衡曲线如图所示。下列说法正确的是

 ,其沉淀溶解平衡曲线如图所示。下列说法正确的是
,其沉淀溶解平衡曲线如图所示。下列说法正确的是
| A.可以通过升温实现由c点变到a点 |
| B.d点可能有沉淀生成 |
C.a点对应的 等于b点对应的 等于b点对应的 |
D.该温度下, |
您最近一年使用:0次



