名校
解题方法
1 . 实验室常用NaOH溶液吸收NO2尾气,探究其适宜条件原理。20℃时,将4mL不同浓度NaOH溶液一次性推入中40mLNO2,观察现象。
(1)NaOH溶液吸收NO2时生成两种钠盐,分别为NaNO2和_____ 。
(2)检验甲中剩余气体的方法:排出大注射器中的溶液,拔下导管,吸入少量空气,气体变为红棕色。用化学方程式表示检验的反应原理是_____ 。
(3)某同学推测甲中产生无色气体的原因:局部OH-浓度过低,导致部分NO2与水反应。通过实验证明其成立:用与甲相同的装置、试剂和条件,将NO2缓慢推入NaOH溶液中,_____ (补全实验现象)。
(4)进一步探究NO2与水或碱反应时还原产物价态不同的原理。
【查阅资料】
i.NO2遇水时发生反应:a.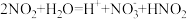
b.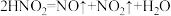 ;
;
ii.酸性条件下,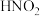 或
或 可与对氨基苯磺酸发生
可与对氨基苯磺酸发生不可逆 反应,所得产物遇萘乙二胺变红,且原溶液中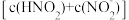 越大,红色越深。
越大,红色越深。
【实验】将2mLNO2推入5mL下列试剂中,随即取出0.1mL溶液,滴加到等量对氨基苯磺酸溶液(盐酸酸化)中,再加入等量萘乙二胺溶液,加水定容到相同体积,对比溶液颜色。
①通过实验_____ (填编号)对比,说明NO2遇水时发生了反应a和b。
②从化学反应速率的角度分析,NO2与水或碱反应时还原产物价态不同的原因是_____ 。
(5)若用0℃的NaOH溶液重复实验甲,最终剩余约3mL(20℃)无色气体。
综上,用NaOH溶液吸收NO2尾气,适宜的条件是______ (写出两点即可)。
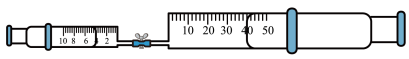
| 编号 | c(NaOH) | 现象 |
| 甲 | 2mol•L-1 | 活塞自动内移,最终剩余约7mL无色气体 |
| 乙 | 6mol•L-1 | 活塞自动内移,最终气体全部被吸收 |
(2)检验甲中剩余气体的方法:排出大注射器中的溶液,拔下导管,吸入少量空气,气体变为红棕色。用化学方程式表示检验的反应原理是
(3)某同学推测甲中产生无色气体的原因:局部OH-浓度过低,导致部分NO2与水反应。通过实验证明其成立:用与甲相同的装置、试剂和条件,将NO2缓慢推入NaOH溶液中,
(4)进一步探究NO2与水或碱反应时还原产物价态不同的原理。
【查阅资料】
i.NO2遇水时发生反应:a.
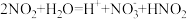
b.
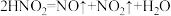 ;
;ii.酸性条件下,
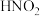 或
或 可与对氨基苯磺酸发生
可与对氨基苯磺酸发生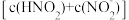 越大,红色越深。
越大,红色越深。【实验】将2mLNO2推入5mL下列试剂中,随即取出0.1mL溶液,滴加到等量对氨基苯磺酸溶液(盐酸酸化)中,再加入等量萘乙二胺溶液,加水定容到相同体积,对比溶液颜色。
| 编号 | 试剂 | 溶液颜色 |
| 丙 | 水 | 溶液均呈红色,丁与戊颜色几乎相同,丙的颜色更浅 |
| 丁 | 6mol•L-1NaOH溶液 | |
| 戊 | 酸性对氨基苯磺酸溶液 |
②从化学反应速率的角度分析,NO2与水或碱反应时还原产物价态不同的原因是
(5)若用0℃的NaOH溶液重复实验甲,最终剩余约3mL(20℃)无色气体。
综上,用NaOH溶液吸收NO2尾气,适宜的条件是
您最近半年使用:0次
2023-04-01更新
|
1256次组卷
|
7卷引用:北京市东城区2023届一模考试化学试题
名校
解题方法
2 . 硫及其化合物的“价-类”二维图体现了化学变化之美。
完成下列填空:
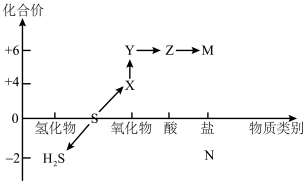
(1)不同价态的硫元素可以相互转化,请写出符合以下要求的方程式:
①反应前后存在3种价态的硫元素,写出反应的化学方程式___________ 。
②反应前后存在4种价态的硫元素,写出反应的化学方程式__________ 。
(2)结合二维图所示,在一定条件下存在以下转化:Z M,H2S
M,H2S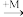 N,M是下列物质中的
N,M是下列物质中的_____________ 。
A. Na2SO4 B.CuSO4 C.FeSO4 D.K2SO4
写出H2S生成N的离子方程式为_____________ ;相应的Q可以是_____________ (写出2类物质)。
(3)小附同学利用下列装置测定空气中SO2的含量。
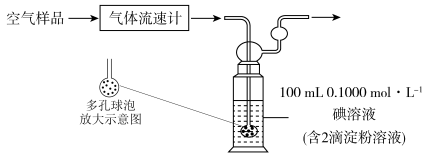
通空气样品的导管末端是带许多小孔的玻璃球泡,其主要作用是_____________ ,该装置中发生的离子方程式为:_________________________________ 。若空气流速为a m3·min-1,当观察到装置内_________ 时,结束计时,测定耗时t min。假定空气中的SO2可被溶液充分吸收,该空气样品中SO2的含量是_____ mg·m-3。
(4)小附同学发现随着SO2持续通入,装置内溶液逐渐变浑浊。查阅资料后得知,在催化剂的作用下,SO2在水中会发生歧化反应。于是又设计以下实验进行探究。
【实验装置】
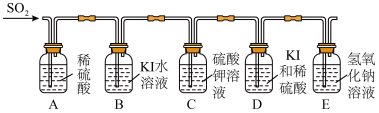
【实验现象】一段时间后, A、C中无明显现象,D中比B中的溶液先变浑浊。
【实验结论】在水中,SO2歧化的离子方程式为_____________ 。该反应中的催化剂是_____________ 。
A. H+ B. I- C. K+、H+ D. K+、I-
完成下列填空:

(1)不同价态的硫元素可以相互转化,请写出符合以下要求的方程式:
①反应前后存在3种价态的硫元素,写出反应的化学方程式
②反应前后存在4种价态的硫元素,写出反应的化学方程式
(2)结合二维图所示,在一定条件下存在以下转化:Z
 M,H2S
M,H2S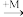 N,M是下列物质中的
N,M是下列物质中的A. Na2SO4 B.CuSO4 C.FeSO4 D.K2SO4
写出H2S生成N的离子方程式为
(3)小附同学利用下列装置测定空气中SO2的含量。

通空气样品的导管末端是带许多小孔的玻璃球泡,其主要作用是
(4)小附同学发现随着SO2持续通入,装置内溶液逐渐变浑浊。查阅资料后得知,在催化剂的作用下,SO2在水中会发生歧化反应。于是又设计以下实验进行探究。
【实验装置】

【实验现象】一段时间后, A、C中无明显现象,D中比B中的溶液先变浑浊。
【实验结论】在水中,SO2歧化的离子方程式为
A. H+ B. I- C. K+、H+ D. K+、I-
您最近半年使用:0次
2022高二上·安徽阜阳·竞赛
解题方法
3 . 2022年6月末,日本国家警察厅 (NPA) 正式宣布,将开始为富士山可能发生喷发做全面准备。也就是说,自1707年最后一次喷发后,平静了300多年的富士山,可能真的将正式进入“待机阶段”。警察厅认为,如果日本富士山喷发,火山灰不仅可能落在富士山附近地区,也有可能落在东京都市圈,也就是还可能影响东京。下列说法中正确的是
| A.硫在自然界中没有以单质存在的情况,大多数的硫元素以矿物的形式存在。 |
| B.硫化物在地表附近由于受到空气中氧气和水的长期作用,会转化为亚硫酸。 |
| C.芒硝化学式中有10个水分子,通过风化这一化学变化可以去除其中的水。 |
| D.火山灰中含硫氧化物,其自身记入PM2.5指标,进入空气一定能形成胶体。 |
您最近半年使用:0次
解题方法
4 . NH3和O2混合气100 mL通过红热的铂网,充分反应后的混合气再通过足量水最终收集到10mL残留气体,则原混合气中O2体积不可能是(气体体积在相同条件下测定)
| A.12.5 mL | B.21.5 mL | C.64.2 mL | D.70.0 mL |
您最近半年使用:0次
5 . 某固体混合物可能由SiO2、Fe2O3、Fe、Na2SO3、Na2CO3、BaCl2中的若干种物质组成,设计部分实验方案探究该固体混合物的成分,所加试剂均过量,下列说法正确的是
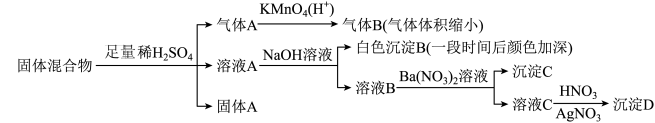

| A.气体A是SO2和CO2的混合气体 |
| B.固体A一定含有SiO2,可能含有BaSO4 |
| C.该固体混合物中Fe2O3和Fe至少有其中一种 |
| D.该固体混合物一定含有Na2CO3、Na2SO3、BaCl2 |
您最近半年使用:0次
解题方法
6 . 亚硫酸钠在印染、造纸等众多行业中有着广泛的应用。研究小组用Na2CO3溶液吸收SO2制备Na2SO3。其实验流程如下:
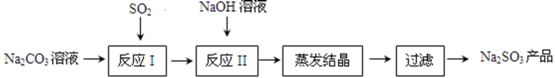
(1)SO2对环境的危害主要是形成_________ 。
(2)用Na2CO3溶液能吸收SO2的原因是____________________ 。
(3)查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中发生如下反应:
①2Na2CO3+SO2+H2O=2NaHCO3+Na2SO3
②2NaHCO3+ SO2+H2O=2CO2↑+Na2SO3
③Na2SO3+ SO2+H2O=2NaHSO3
溶液中有关组分的质量分数变化如图是所示,图中的线2表示的组分为___ (填化学式)。
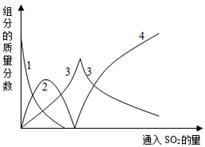
(4)实验时,“反应II”中加入NaOH溶液的目的是____________ (用化学方程式表示)。
(5)获得的Na2SO3产品久置后质量变重,主要原因是______ 。

(1)SO2对环境的危害主要是形成
(2)用Na2CO3溶液能吸收SO2的原因是
(3)查阅资料可知,向碳酸钠溶液通入二氧化硫的过程中发生如下反应:
①2Na2CO3+SO2+H2O=2NaHCO3+Na2SO3
②2NaHCO3+ SO2+H2O=2CO2↑+Na2SO3
③Na2SO3+ SO2+H2O=2NaHSO3
溶液中有关组分的质量分数变化如图是所示,图中的线2表示的组分为

(4)实验时,“反应II”中加入NaOH溶液的目的是
(5)获得的Na2SO3产品久置后质量变重,主要原因是
您最近半年使用:0次
解题方法
7 . 硫、氮、碳的氧化物都会引起环境问题,越来越引起人们的重视,如图1是氮元素的各种价态与物质类别的对应关系
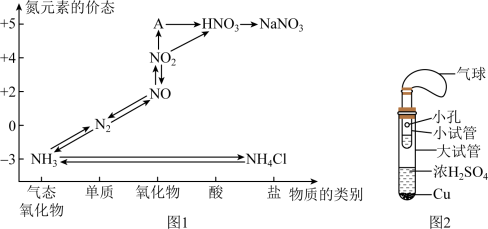
(1)根据A对应的化合价和物质类别,A为_________ (写分子式),从氦元素的化合价能否发生变化的角度判断,图1中既有氧化性又有还原性的化合物是_________ ;
(2)浓、稀硝酸的性质相似又有差别,若要除去铁制品表面的铜镀层应选择,反应的化学方程式为_________________ ;
(3)某同学设计了如图2所示的套管实验装置(部分装置未画出)来制备SO2,并利用实验现象来检验其还原性,制备SO2时选用的试剂为Cu和浓H2SO4,回答下列问题.
①写出制取SO2的化学方程式___________________ ;
②该同学利用实验现象来检验SO2的还原性,则选用的试剂为__________ ;
A 双氧水(H2O2) B品红溶液 C 酸性高锰酸钾溶液
(4)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的.吸收工艺常用的方法是用热空气吹出Br2,用SO2吸收Br2,取吸收后的溶液,向其中加入氯化钠溶液有白色沉淀析出,写出SO2吸收Br2反应的化学方程式______________ 。

(1)根据A对应的化合价和物质类别,A为
(2)浓、稀硝酸的性质相似又有差别,若要除去铁制品表面的铜镀层应选择,反应的化学方程式为
(3)某同学设计了如图2所示的套管实验装置(部分装置未画出)来制备SO2,并利用实验现象来检验其还原性,制备SO2时选用的试剂为Cu和浓H2SO4,回答下列问题.
①写出制取SO2的化学方程式
②该同学利用实验现象来检验SO2的还原性,则选用的试剂为
A 双氧水(H2O2) B品红溶液 C 酸性高锰酸钾溶液
(4)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的.吸收工艺常用的方法是用热空气吹出Br2,用SO2吸收Br2,取吸收后的溶液,向其中加入氯化钠溶液有白色沉淀析出,写出SO2吸收Br2反应的化学方程式
您最近半年使用:0次
8 . 现有铜、银合金14g与足量的某浓度的硝酸100mL发生反应,将生成的气体与1.12L(标况)氧气混合,通入足量的水中恰好全部吸收,反应后溶液体积仍为100mL。试通过计算回答下列问题:
(1)原固体混合物中铜和银的质量各是多少?
(2)若原硝酸溶液为浓硝酸,反应产生的气体是单一气体,则该反应中被还原的硝酸的物质的量是多少?
(3)合金完全溶解后,若生成的气体在标况下体积为2.24L,反应后溶液中c(H+)=7mol/L,则该混合气体中NO和NO2在标准状况下的体积分别是多少?原硝酸的浓度是多少?
(1)原固体混合物中铜和银的质量各是多少?
(2)若原硝酸溶液为浓硝酸,反应产生的气体是单一气体,则该反应中被还原的硝酸的物质的量是多少?
(3)合金完全溶解后,若生成的气体在标况下体积为2.24L,反应后溶液中c(H+)=7mol/L,则该混合气体中NO和NO2在标准状况下的体积分别是多少?原硝酸的浓度是多少?
您最近半年使用:0次
9 . 甲、乙、丙、丁四种物质中,均含有相同的某种元素。在一定条件下它们之间存在如下转化关系:下列说法中错误的是
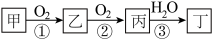

| A.甲可能是单质,也可能是化合物 | B.丁可能是酸,也可能是碱 |
| C.反应①②一定是氧化还原反应 | D.反应③一定是化合反应 |
您最近半年使用:0次
2016-12-09更新
|
1212次组卷
|
3卷引用:2015届福建省莆田市普通高中高三质量检测化学试卷
10 . A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如下图所示。其中A、B、C、D在常温下都是气体,B为红棕色。
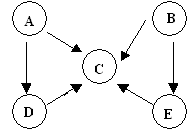
(1)用正确的化学用语描述:B的分子式:_______ , A的电子式:______ ,D的结构式:______ 。
(2)写出下列反应的化学方程式:
D→C的化学方程式为__________________________________ 。
E→B的离子方程式为____________________________ 。
A→D化学方程式为__________________________________ 。

(1)用正确的化学用语描述:B的分子式:
(2)写出下列反应的化学方程式:
D→C的化学方程式为
E→B的离子方程式为
A→D化学方程式为
您最近半年使用:0次



