名校
解题方法
1 . 硫酰氯(SO2Cl2)是化工生产的重要原料。硫酰氯与硫酸的部分性质如表:
实验室用干燥纯净的氯气和过量的二氧化硫在活性炭的催化作用下合成硫酰氯,反应方程式为SO2(g)+Cl2(g)=SO2Cl2(l),其实验装置如图所示(部分夹持仪器已省略):

(1)仪器B的名称_______ ,B中盛放的药品是_______ 。
(2)C是恒压分液漏斗,和普通分液漏斗相比,它的优点是_______ 。
(3)装置乙和丁盛装的是同一种试剂,该试剂为_______ 。若缺少装置乙和丁,对产品硫酰氯会有何影响,请用化学方程式表示_______ 。
(4)装置甲发生反应的化学方程式为_______ 。
(5)实验开始时,戊中开始加入amolKMnO4固体,假设KMnO4在过量浓盐酸的作用下完全反应,若实验结束后得到硫酰氯bmol,请计算硫酰氯的产率_______ (列出表达式)。
| 物质 | 熔点/℃ | 沸点/℃ | 其他性质 |
| SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾,生成两种强酸 ②易分解:SO2Cl2 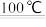 SO2↑+Cl2↑ SO2↑+Cl2↑ |
| H2SO4 | 10.4 | 338 | 强吸水性、稳定不易分解 |

(1)仪器B的名称
(2)C是恒压分液漏斗,和普通分液漏斗相比,它的优点是
(3)装置乙和丁盛装的是同一种试剂,该试剂为
(4)装置甲发生反应的化学方程式为
(5)实验开始时,戊中开始加入amolKMnO4固体,假设KMnO4在过量浓盐酸的作用下完全反应,若实验结束后得到硫酰氯bmol,请计算硫酰氯的产率
您最近一年使用:0次
名校
2 . I.前36号A、B、C、D、E、F六种元素,其中A、B、C、D、E的原子序数均小于18且其核电荷数依次递增,A是半径最小的原子,B元素基态原子电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同,D原子的价电子排布为ns2npn+2,E原子第一至第四电离能( )分别为:738、1451、7733、10540.F2+离子K、L、M层全充满。根据以上信息,回答下列问题:
)分别为:738、1451、7733、10540.F2+离子K、L、M层全充满。根据以上信息,回答下列问题:
(1)BA4D和BA2D,沸点较高的是_______ (填相关物质的结构简式)
(2)已知B与A形成的化合物在标准状况下的密度为1.16 ,则该化合物分子的空间立体构型为
,则该化合物分子的空间立体构型为_______ ,在该化合物分子中含有σ键和π键个数比_______ 。
(3)写出单质E与B的最高价氧化物反应的化学方程式_______
(4)B的单质是一种层状结构,元素B和E的形成一种合金,“ ”表示E原子的位置,该合金的化学式为
”表示E原子的位置,该合金的化学式为_______ 。

II.北京冬奥会火炬“飞扬”在研制的过程中,解决了火焰颜色与稳定性、高压储氢、氢能安全利用等多项技术难题。中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水来制备氢气,其主要过程如图所示。
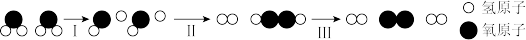
(5)过程III属于_______ 反应(填“吸热”或“放热”)。
(6)分解产生的H2(g)可以与CO2(g)反应用来合成甲醇,反应的能量变化如图所示。

①该反应需加入铜-锌基催化剂。加入催化剂后,该反应的
_______ (填“变大”“变小”或“不变”)。
②已知:


写出以CO(g)和H2(g)为原料合成甲醇的热化学方程式_______ 。
 )分别为:738、1451、7733、10540.F2+离子K、L、M层全充满。根据以上信息,回答下列问题:
)分别为:738、1451、7733、10540.F2+离子K、L、M层全充满。根据以上信息,回答下列问题:(1)BA4D和BA2D,沸点较高的是
(2)已知B与A形成的化合物在标准状况下的密度为1.16
 ,则该化合物分子的空间立体构型为
,则该化合物分子的空间立体构型为(3)写出单质E与B的最高价氧化物反应的化学方程式
(4)B的单质是一种层状结构,元素B和E的形成一种合金,“
 ”表示E原子的位置,该合金的化学式为
”表示E原子的位置,该合金的化学式为
II.北京冬奥会火炬“飞扬”在研制的过程中,解决了火焰颜色与稳定性、高压储氢、氢能安全利用等多项技术难题。中国研究人员研制出一种新型复合光催化剂,利用太阳光在催化剂表面实现高效分解水来制备氢气,其主要过程如图所示。
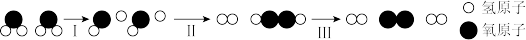
(5)过程III属于
(6)分解产生的H2(g)可以与CO2(g)反应用来合成甲醇,反应的能量变化如图所示。

①该反应需加入铜-锌基催化剂。加入催化剂后,该反应的

②已知:



写出以CO(g)和H2(g)为原料合成甲醇的热化学方程式
您最近一年使用:0次
2022-03-14更新
|
115次组卷
|
2卷引用:重庆市乌江新高考协作体2023-2024学年高一上学期期末学业质量联合调研抽测化学试题



