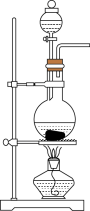
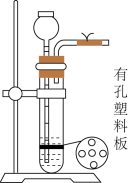
1 . 化学在“三废”治理方面发挥着重要的作用。回答下列问题:
Ⅰ.制革厂含硫废水中主要含有 ,需要对含硫废水进行处理与利用。
,需要对含硫废水进行处理与利用。
(1) 的电子式为
的电子式为___________ ;
(2)废水混合处理不但可以同时处理不同类型的废水,同时可以获得某些化工原料。某地区使用含有硫离子的废水治理含有铜离子的废水,写出该反应的离子方程式___________ 。
(3)部分地区采用空气催化氧化法脱硫。该方法以空气中的氧作为氧化剂,将废水中的 转化为
转化为 ,反应中还原剂与氧化剂的物质的量之比为
,反应中还原剂与氧化剂的物质的量之比为___________ 。
Ⅱ.工业上用烟气制酸的废料(主要含S、Se、 、CuO、ZnO、
、CuO、ZnO、 等)为原料提取硒,流程如图:
等)为原料提取硒,流程如图:
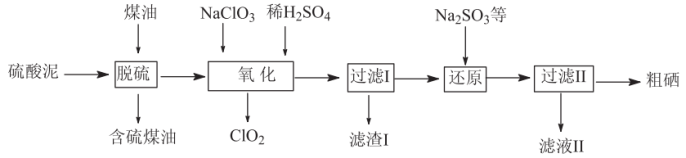
(4)硒与硫是同主族的相邻元素,其在周期表中的位置是___________ 。
(5)“脱硫”过程中,温度控制在95℃,原因是___________ 。
(6)“氧化”过程中,Se转化成弱酸 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
Ⅲ.粗硒经过下列流程可获得亚硒酸钠(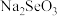 )。
)。
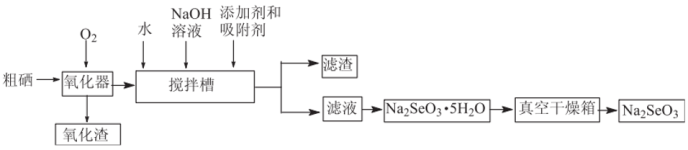
(7)已知在上述合成路线中粗硒在转化为二氧化硒时损失4%,搅拌槽中二氧化硒的利用率为95%,其他损耗忽略不计,试计算利用1t含硒79%的粗硒最终可生产___________ t(精确到0.01t)含亚硒酸钠95%的产品。
Ⅰ.制革厂含硫废水中主要含有
 ,需要对含硫废水进行处理与利用。
,需要对含硫废水进行处理与利用。(1)
 的电子式为
的电子式为(2)废水混合处理不但可以同时处理不同类型的废水,同时可以获得某些化工原料。某地区使用含有硫离子的废水治理含有铜离子的废水,写出该反应的离子方程式
(3)部分地区采用空气催化氧化法脱硫。该方法以空气中的氧作为氧化剂,将废水中的
 转化为
转化为 ,反应中还原剂与氧化剂的物质的量之比为
,反应中还原剂与氧化剂的物质的量之比为Ⅱ.工业上用烟气制酸的废料(主要含S、Se、
 、CuO、ZnO、
、CuO、ZnO、 等)为原料提取硒,流程如图:
等)为原料提取硒,流程如图:
(4)硒与硫是同主族的相邻元素,其在周期表中的位置是
(5)“脱硫”过程中,温度控制在95℃,原因是
(6)“氧化”过程中,Se转化成弱酸
 ,该反应的离子方程式为
,该反应的离子方程式为Ⅲ.粗硒经过下列流程可获得亚硒酸钠(
 )。
)。
(7)已知在上述合成路线中粗硒在转化为二氧化硒时损失4%,搅拌槽中二氧化硒的利用率为95%,其他损耗忽略不计,试计算利用1t含硒79%的粗硒最终可生产
您最近一年使用:0次
解题方法
2 . 绿色化学的核心就是利用化学原理和技术手段从源头上减少或消除工业生产对环境的污染。下列做法不符合“绿色化学”理念的是
| A.尽可能采用对人类和环境无毒无害的合成路线 |
| B.用可降解塑料生产包装盒或快餐盒 |
| C.用反应Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O制备硝酸铜 |
D.用反应2CH2=CH2+O2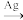 2 2 制备环氧乙烷 制备环氧乙烷 |
您最近一年使用:0次
解题方法
3 . 近期,中国科学家在实验室中首次实现从二氧化碳到淀粉的全合成,其路径如图所示。下列说法不正确的是


A.CO2分子的电子式为: |
B. 表示一种物质的分子结构 表示一种物质的分子结构 |
| C.合成路线中涉及氧化还原反应 |
| D.合成路线中涉及共价键的断裂与形成 |
您最近一年使用:0次
4 . 磺酰氯 是重要的有机合成试剂,实验室可利用
是重要的有机合成试剂,实验室可利用 与
与 在活性炭作用下反应制取少量
在活性炭作用下反应制取少量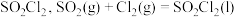 ,该反应放热,装置如图所示(部分夹持装置省略)。已知
,该反应放热,装置如图所示(部分夹持装置省略)。已知 的熔点为
的熔点为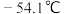 ,沸点为
,沸点为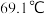 ,遇水能发生剧烈的水解反应,并产生白雾。
,遇水能发生剧烈的水解反应,并产生白雾。
回答下列问题。 ,则下列试剂组合中合适的是___________。
,则下列试剂组合中合适的是___________。
(2)导管a的作用是___________ ;仪器b中的试剂是___________ 。
(3)实验结束时,关闭分液漏斗活塞和止水夹k,此时装置戊的作用是___________ 。
(4) 遇水发生反应生成两种酸,该反应的化学方程式为
遇水发生反应生成两种酸,该反应的化学方程式为___________ 。
(5)若反应中消耗的氯气体积为 (标准状况下),最后经过分离提纯得到
(标准状况下),最后经过分离提纯得到 纯净的磺酰氯,则磺酰氯的产率为
纯净的磺酰氯,则磺酰氯的产率为___________ (产率:实际产量/理论产量 )。
)。
(6)已知酸性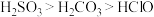 ,借助该酸性排序,使用以下装置设计实验证明
,借助该酸性排序,使用以下装置设计实验证明 的酸性强于
的酸性强于 ,其连接顺序应为
,其连接顺序应为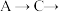
___________ 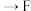 ;能证明
;能证明 的酸性强于
的酸性强于 的实验现象为
的实验现象为___________ 。
 是重要的有机合成试剂,实验室可利用
是重要的有机合成试剂,实验室可利用 与
与 在活性炭作用下反应制取少量
在活性炭作用下反应制取少量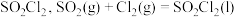 ,该反应放热,装置如图所示(部分夹持装置省略)。已知
,该反应放热,装置如图所示(部分夹持装置省略)。已知 的熔点为
的熔点为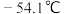 ,沸点为
,沸点为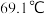 ,遇水能发生剧烈的水解反应,并产生白雾。
,遇水能发生剧烈的水解反应,并产生白雾。回答下列问题。

 ,则下列试剂组合中合适的是___________。
,则下列试剂组合中合适的是___________。A. 的硫酸和 的硫酸和 | B. 的硝酸和 的硝酸和 固体 固体 |
C. 的硫酸和 的硫酸和 固体 固体 | D. 的硫酸和 的硫酸和 固体 固体 |
(2)导管a的作用是
(3)实验结束时,关闭分液漏斗活塞和止水夹k,此时装置戊的作用是
(4)
 遇水发生反应生成两种酸,该反应的化学方程式为
遇水发生反应生成两种酸,该反应的化学方程式为(5)若反应中消耗的氯气体积为
 (标准状况下),最后经过分离提纯得到
(标准状况下),最后经过分离提纯得到 纯净的磺酰氯,则磺酰氯的产率为
纯净的磺酰氯,则磺酰氯的产率为 )。
)。(6)已知酸性
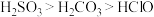 ,借助该酸性排序,使用以下装置设计实验证明
,借助该酸性排序,使用以下装置设计实验证明 的酸性强于
的酸性强于 ,其连接顺序应为
,其连接顺序应为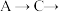
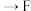 ;能证明
;能证明 的酸性强于
的酸性强于 的实验现象为
的实验现象为
您最近一年使用:0次
2024-02-23更新
|
154次组卷
|
2卷引用:广东省深圳实验学校高中部2023-2024学年高一上学期第三阶段考试化学试题
名校
解题方法
5 . 二氯化二硫(S2Cl2)在工业上用于橡胶的硫化。为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品。
②有关物质的部分性质如表:
设计实验装置图如图所示。

(1)图中装置不够完善,请你提出改进意见_____ 。
利用改进后的正确装置进行实验,请回答下列问题:
(2)仪器A的名称分别是____ ,B中反应的化学方程式:____ 。
(3)C、D中的试剂分别是____ 、____ 。
(4)长导管F的作用是____ ;如果在加热E时温度过高,在F中可能出现的现象是____ 。
(5)实验开始前应先点燃____ (选填“I”或“II”)处的酒精灯。
(6)S2Cl2粗品中可能混有的杂质是____ (填写两种),为了提高S2Cl2的纯度,关键的操作是控制好温度和____ 。
①将干燥的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品。
②有关物质的部分性质如表:
| 物质 | 熔点/℃ | 沸点/℃ | 化学性质 |
| S | 112.8 | 444.6 | 略 |
| S2Cl2 | -77 | 137 | ①遇水生成HCl、SO2、S; ②温度超300℃以上完全分解生成硫和氯气; ③S2Cl2+Cl2  2SCl2 2SCl2 |

(1)图中装置不够完善,请你提出改进意见
利用改进后的正确装置进行实验,请回答下列问题:
(2)仪器A的名称分别是
(3)C、D中的试剂分别是
(4)长导管F的作用是
(5)实验开始前应先点燃
(6)S2Cl2粗品中可能混有的杂质是
您最近一年使用:0次
名校
6 . 锂电池是目前应用广泛的新型电池,一种回收钴酸锂废旧电池(主要成分为LiCoO2,同时含有少量Fe、Al、C单质)的流程如下图所示。
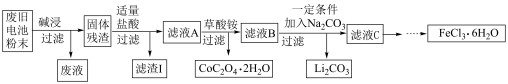
已知:Fe3+能与C2O 结合成[Fe(C2O4)3]3-,[Fe(C2O4)3]3-在强酸性环境下重新转化为Fe3+
结合成[Fe(C2O4)3]3-,[Fe(C2O4)3]3-在强酸性环境下重新转化为Fe3+
请回答下列问题:
(1)由滤液A制取CoC2O4·2H2O的过程发生的___________ (填“是”或“不是”)氧化还原反应,CoC2O4·2H2O中C的化合价为___________ ,滤渣I的主要成份为___________ 。
(2)用过量的NaOH溶液进行“碱浸”,“碱浸”的目的是___________ 。
写出该过程发生的化学反应方程式___________ 。
(3)加入适量盐酸,LiCoO2溶解后生成的Co3+能将Fe2+氧化为Fe3+,请写出该反应的离子方程式___________ 。
(4)请设计实验方案检验滤液C中的Cl-。___________
(5)高铁酸钠(Na2FeO4 ,其中铁为+6价)是一种高效多功能水处理剂。工业上用次氯酸钠和氯化铁为原料来制取高铁酸钠,该反应的离子方程式为:_________
___________ClO- +___________Fe3++___________=___________FeO +___________Cl- +___________H2O,请配平该方程式。
+___________Cl- +___________H2O,请配平该方程式。

已知:Fe3+能与C2O
 结合成[Fe(C2O4)3]3-,[Fe(C2O4)3]3-在强酸性环境下重新转化为Fe3+
结合成[Fe(C2O4)3]3-,[Fe(C2O4)3]3-在强酸性环境下重新转化为Fe3+请回答下列问题:
(1)由滤液A制取CoC2O4·2H2O的过程发生的
(2)用过量的NaOH溶液进行“碱浸”,“碱浸”的目的是
写出该过程发生的化学反应方程式
(3)加入适量盐酸,LiCoO2溶解后生成的Co3+能将Fe2+氧化为Fe3+,请写出该反应的离子方程式
(4)请设计实验方案检验滤液C中的Cl-。
(5)高铁酸钠(Na2FeO4 ,其中铁为+6价)是一种高效多功能水处理剂。工业上用次氯酸钠和氯化铁为原料来制取高铁酸钠,该反应的离子方程式为:
___________ClO- +___________Fe3++___________=___________FeO
 +___________Cl- +___________H2O,请配平该方程式。
+___________Cl- +___________H2O,请配平该方程式。
您最近一年使用:0次
2024-01-16更新
|
252次组卷
|
3卷引用:广东省茂名市七校2023-2024学年高一上学期12月联考化学试题
7 . 申泮文院士(1916-2017),广东籍化学家、教育家,长期致力于无机化学教学研究为我国无机化学教学和教材建设做出了卓越贡献。他在化学教育研究领域创下多项第一;编写出新中国第一部大学化学教材、第一个引入美国科技出版物、第一个在化学教学应用计算机技术、主持完成我国第一部多媒体教科书等。他常在课堂教学中,号召学生牢记历史,报效祖国。2005年,申先生入选“中国10位最令人感动的教师”,也是我国执教时间最长的化学教师。2011年,95岁高龄的申先生还坚持骑着行车去给本科生讲课。
申先生是我国在离子型金属氢化物、储氢合金材料和镍/金属氢化物可逆电池等研究领域的先驱者。1959年10月,他和龚毅生等在《化学通报》发表“氢化铝锂的合成”,这是我国在氢化物研究领域发表的第一篇论文。
(1)完成以氢化锂(LiH)和氯化铝为原料合成氢化铝锂(LiAlH4)的反应方程式:
4LiH+______ =LiAlH4+3______
(2)根据以上材料谈一谈你的认识和启示______ 、______ 、______ (写三点)。
申先生是我国在离子型金属氢化物、储氢合金材料和镍/金属氢化物可逆电池等研究领域的先驱者。1959年10月,他和龚毅生等在《化学通报》发表“氢化铝锂的合成”,这是我国在氢化物研究领域发表的第一篇论文。
(1)完成以氢化锂(LiH)和氯化铝为原料合成氢化铝锂(LiAlH4)的反应方程式:
4LiH+
(2)根据以上材料谈一谈你的认识和启示
您最近一年使用:0次
名校
8 . 三氯化六氨合钴(Ⅲ) 是钴化合物合成中的重要原料。实验室以
是钴化合物合成中的重要原料。实验室以 为原料制备
为原料制备 ,步骤如下:
,步骤如下:
Ⅰ. 的制备:
的制备: 可以通过钴和纯净氯气反应制得,实验室制备
可以通过钴和纯净氯气反应制得,实验室制备 可用下图实验装置实现(已知:钴单质在300℃以上易被氧气氧化,
可用下图实验装置实现(已知:钴单质在300℃以上易被氧气氧化, 易潮解)。
易潮解)。

(1)A中发生反应的离子方程式为_______ ,反应中氧化剂和氧化产物的物质的量之比为_______ 。
(2)装置的连接顺序为_______ (按气流方向,用大写字母表示),装置B中的试剂Z是_______ ,其作用是_______ 。
(3)反应开始前应先点燃A处的酒精灯,其目的是_______ 。
Ⅱ.家用泡腾消毒片由 、固体强酸及辅助剂(辅助剂不参与反应)混合制得,使用时只需将泡腾片放入水中,5~10分钟即可完全溶解,释放出
、固体强酸及辅助剂(辅助剂不参与反应)混合制得,使用时只需将泡腾片放入水中,5~10分钟即可完全溶解,释放出 气体。
气体。
(4)①泡腾片在水中发生反应的离子方程式为_______ 。
②泡腾片使用时需要加水,水作为_______ (填字母)。
A.氧化剂 B.还原剂 C.既不是氧化剂,也不是还原剂 D.既是氧化剂,又是还原剂
(5)消毒剂的消毒效率常用单位质量的消毒剂得到的电子数表示。理论上 的消毒效率是
的消毒效率是 的
的_______ 倍(结果保留两位小数)。
 是钴化合物合成中的重要原料。实验室以
是钴化合物合成中的重要原料。实验室以 为原料制备
为原料制备 ,步骤如下:
,步骤如下:Ⅰ.
 的制备:
的制备: 可以通过钴和纯净氯气反应制得,实验室制备
可以通过钴和纯净氯气反应制得,实验室制备 可用下图实验装置实现(已知:钴单质在300℃以上易被氧气氧化,
可用下图实验装置实现(已知:钴单质在300℃以上易被氧气氧化, 易潮解)。
易潮解)。
(1)A中发生反应的离子方程式为
(2)装置的连接顺序为
(3)反应开始前应先点燃A处的酒精灯,其目的是
Ⅱ.家用泡腾消毒片由
 、固体强酸及辅助剂(辅助剂不参与反应)混合制得,使用时只需将泡腾片放入水中,5~10分钟即可完全溶解,释放出
、固体强酸及辅助剂(辅助剂不参与反应)混合制得,使用时只需将泡腾片放入水中,5~10分钟即可完全溶解,释放出 气体。
气体。(4)①泡腾片在水中发生反应的离子方程式为
②泡腾片使用时需要加水,水作为
A.氧化剂 B.还原剂 C.既不是氧化剂,也不是还原剂 D.既是氧化剂,又是还原剂
(5)消毒剂的消毒效率常用单位质量的消毒剂得到的电子数表示。理论上
 的消毒效率是
的消毒效率是 的
的
您最近一年使用:0次
2022-01-22更新
|
258次组卷
|
2卷引用:广东省广州市天河区2021-2022学年高一上学期期末考试化学试题
名校
解题方法
9 . 氯化亚砜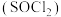 在农药、制药行业中用途广泛。某化学研究性学习小组通过查阅资料,设计了如下图所示装置来制备
在农药、制药行业中用途广泛。某化学研究性学习小组通过查阅资料,设计了如下图所示装置来制备 。
。
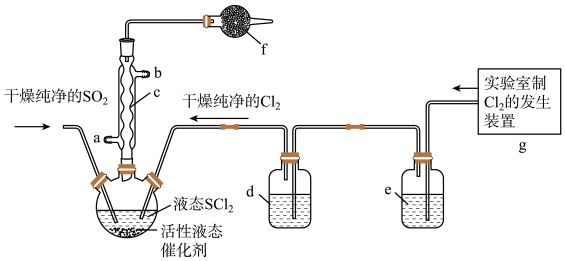
已知:① 是一种液态化合物,沸点为77℃
是一种液态化合物,沸点为77℃
② 遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生
遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生
③实验室合成 原理:
原理:
请回答以下问题:
(1)仪器c的名称是_______ ,f中的最佳试剂是_______ (填字母符号)。
A.碱石灰 B.浓硫酸 C. 溶液 D.无水氯化钙
溶液 D.无水氯化钙
(2)实验室用浓盐酸与 粉末反应制
粉末反应制 的化学方程式为
的化学方程式为________ 。
(3) 与水反应的化学方程式为
与水反应的化学方程式为_______ 。
(4)下列三种制备 的方案中最佳选择是
的方案中最佳选择是_________ .
(5)装置g中产生的 经过e、d后进入三颈烧瓶,e中的试剂为
经过e、d后进入三颈烧瓶,e中的试剂为_____ 。
(6)实验结束后,将三颈烧瓶中混合物分离开的实验操作是_____ (已知 的沸点为50℃);若反应中消耗
的沸点为50℃);若反应中消耗 的体积为
的体积为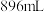 (已转化为标准状况,
(已转化为标准状况, 足量),最后得到
足量),最后得到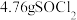 ,则
,则 的产率为
的产率为_______ (已知产率=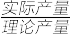 ×100%)。
×100%)。
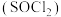 在农药、制药行业中用途广泛。某化学研究性学习小组通过查阅资料,设计了如下图所示装置来制备
在农药、制药行业中用途广泛。某化学研究性学习小组通过查阅资料,设计了如下图所示装置来制备 。
。
已知:①
 是一种液态化合物,沸点为77℃
是一种液态化合物,沸点为77℃②
 遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生
遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生③实验室合成
 原理:
原理:
请回答以下问题:
(1)仪器c的名称是
A.碱石灰 B.浓硫酸 C.
 溶液 D.无水氯化钙
溶液 D.无水氯化钙(2)实验室用浓盐酸与
 粉末反应制
粉末反应制 的化学方程式为
的化学方程式为(3)
 与水反应的化学方程式为
与水反应的化学方程式为(4)下列三种制备
 的方案中最佳选择是
的方案中最佳选择是方案 | 甲 | 乙 | 丙 |
| 发生装置 |
|
|
|
| 所选试剂 | 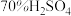 和 和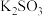 粉末 粉末 | 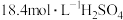 铜片 铜片 | 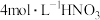 和 和 粉末 粉末 |
 经过e、d后进入三颈烧瓶,e中的试剂为
经过e、d后进入三颈烧瓶,e中的试剂为(6)实验结束后,将三颈烧瓶中混合物分离开的实验操作是
 的沸点为50℃);若反应中消耗
的沸点为50℃);若反应中消耗 的体积为
的体积为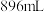 (已转化为标准状况,
(已转化为标准状况, 足量),最后得到
足量),最后得到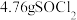 ,则
,则 的产率为
的产率为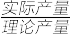 ×100%)。
×100%)。
您最近一年使用:0次
2020-08-12更新
|
251次组卷
|
2卷引用:广东省湛江市第二中学2022-2023学年高一下学期期末考试化学试题
名校
10 . 习总书记在2021年11月第26次《联合国气候变化框架公约》世界领导人大会上代表中国政府庄严承诺中国在2030年前碳达峰。下列说法正确的是
A.中科院天津化学研究所在世界上首次利用人工方法将 合成淀粉,可以实现利用空气“生产粮食” 合成淀粉,可以实现利用空气“生产粮食” |
| B.以煤为原料的火力发电厂发生的化学反应不包含还原反应 |
| C.天然气不充分燃烧的产物都是酸性氧化物 |
| D.推进煤炭消费替代和转型升级,大力发展新能源不是实现碳达峰的途径之一 |
您最近一年使用:0次
2022-01-25更新
|
350次组卷
|
4卷引用:广东省潮州市饶平县华侨中学2022-2023学年高一10月月考化学试题