名校
1 . “从二氧化碳到淀粉的人工合成”入选2021年度“中国生命科学十大进展”。实验室实现由CO2到淀粉的合成路线如图,下列说法不正确的是


| A.标况下,11.2LCO2中含有共用电子对数目为2NA |
| B.反应②属于氧化反应 |
| C.其他条件相同,温度越高,反应②的反应速率越快 |
| D.“人工合成淀粉”有助于“双碳”达标和缓解粮食危机 |
您最近一年使用:0次
解题方法
2 . I.氯气是一种重要的化工原料,氯气及其化合物在自来水的消毒、农药的生产、药物的合成等领域都有着重要的应用。
(1)NaClO具有较强的_______ (填“氧化”或“还原”)性,是常用的消毒剂和漂白剂的有效成分,其漂白原理用化学方程式表示为:_______ 。
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为SO ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
②ClO2可将废水中的Mn2+氧化为MnO2而除去,本身被还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为_______ 。
Ⅱ.某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(该反应为放热反应),回答下列问题:
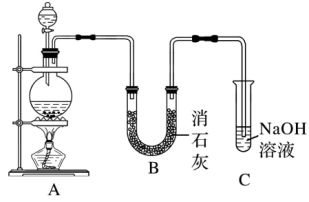
(3)实验室常用A装置制备氯气,写出该反应的化学方程式_______ 。
(4)C装置的作用是_______ 。
(5)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是_______ 。
②另一个副反应是2HCl+Ca(OH)2=CaCl2+2H2O,为避免此副反应的发生,装置的改进措施为_______ 。
(1)NaClO具有较强的
(2)黄色气体ClO2可用于污水杀菌和饮用水净化。
①KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为SO
 ,该反应的离子方程式为
,该反应的离子方程式为②ClO2可将废水中的Mn2+氧化为MnO2而除去,本身被还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为
Ⅱ.某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(该反应为放热反应),回答下列问题:

(3)实验室常用A装置制备氯气,写出该反应的化学方程式
(4)C装置的作用是
(5)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO3)2,为避免此副反应的发生,可采取的措施是
②另一个副反应是2HCl+Ca(OH)2=CaCl2+2H2O,为避免此副反应的发生,装置的改进措施为
您最近一年使用:0次
解题方法
3 . 高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(主要成分为MnS,还含Fe、Al、Mg、Zn、Ni、Si等元素的氧化物)制备,工艺流程如图所示,回答下列问题:
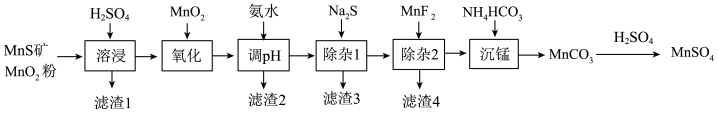
相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下表:
(1)已知“溶浸”中发生反应的化学方程式为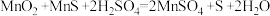 ,当生成0.5molMnSO4时,该反应中转移的电子数为
,当生成0.5molMnSO4时,该反应中转移的电子数为_____ ,该反应中n(还原剂):n(氧化剂)=_____ ,“滤渣1”的主要成分为_____ (化学式)。
(2)“氧化”中添加适量的MnO2的作用是将Fe2+氧化为Fe3+,酸性条件下MnO2氧化Fe2+反应的离子方程式为_____ 。
(3)“除杂1”的目的是去Zn2+和Ni2+,“除杂2”的目的是将Mg2+转化为MgF2沉淀从而除去Mg2+,试推测“调pH”是为了除_____ (填元素符号),溶液的pH范围应调节在_____ ~6(当某金属离子沉淀完全视作该金属离子已除净)。
(4)写出“沉锰”时发生反应的离子方程式_____ 。
(5)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为Li3NixCoyMnzO6,其中Ni、Co、Mn、O的化合价次为+2、+3、+4、-2,当x=y=1时,z=_____ ,试用氧化物的形式表示镍钴锰三元材料:_____ [某些含氧酸盐可以写成氧化物的形式(例如:NaAlO2以表示为NaO·Al2O3]。

相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下表:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
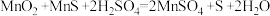 ,当生成0.5molMnSO4时,该反应中转移的电子数为
,当生成0.5molMnSO4时,该反应中转移的电子数为(2)“氧化”中添加适量的MnO2的作用是将Fe2+氧化为Fe3+,酸性条件下MnO2氧化Fe2+反应的离子方程式为
(3)“除杂1”的目的是去Zn2+和Ni2+,“除杂2”的目的是将Mg2+转化为MgF2沉淀从而除去Mg2+,试推测“调pH”是为了除
(4)写出“沉锰”时发生反应的离子方程式
(5)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为Li3NixCoyMnzO6,其中Ni、Co、Mn、O的化合价次为+2、+3、+4、-2,当x=y=1时,z=
您最近一年使用:0次
2023-07-09更新
|
162次组卷
|
2卷引用:山西省忻州市2022-2023学年高一下学期7月期末考试化学试题
解题方法
4 . 硫酰氯( )、氯化亚砜(
)、氯化亚砜(  )常作氯化剂,用于制造药品、染料和表面活性剂。它们部分性质如下:
)常作氯化剂,用于制造药品、染料和表面活性剂。它们部分性质如下:
实验室合成 的原理:
的原理:  。某小组设计实验如图所示(夹持仪器已省略):
。某小组设计实验如图所示(夹持仪器已省略):

回答下列问题:
(1)D中试剂是_______ ,活性炭的作用是 _______________________ ;
(2)实验室常用高锰酸钾固体与浓盐酸在常温下反应制氯气,写出反应的离子方程式_______________________ ;
(3)实验室用 粉末与75%的浓硫酸反应制备
粉末与75%的浓硫酸反应制备  ,发现产生
,发现产生 很少,可能的原因是
很少,可能的原因是 ________________________ ;
(4)E中碱石灰的作用是_______________________ ;
(5)氯化亚砜遇水蒸气发生反应的化学方程式是____________________ ;实验室蒸干 溶液不能得到无水
溶液不能得到无水  ,但是
,但是 和
和 混合物加热,可得到无水
混合物加热,可得到无水  ,其主要原因是
,其主要原因是 ________________________ ;
(6)为了测定 产品纯度(杂质不参与反应),称取a g
产品纯度(杂质不参与反应),称取a g 产品于锥形瓶中(如图所示),向锥形瓶中加入足量蒸馏水,充分反应后,用c
产品于锥形瓶中(如图所示),向锥形瓶中加入足量蒸馏水,充分反应后,用c  溶液滴定至终点(滴几滴
溶液滴定至终点(滴几滴 溶液作指示剂),消耗
溶液作指示剂),消耗  溶液为V mL。
溶液为V mL。
①用棕色滴定管盛装 溶液,其原因是
溶液,其原因是 ______________ ;
②该 产品的纯度为
产品的纯度为 ______________ ;
③实验中,控制分液漏斗活塞,缓慢滴加水,避免氯化氢挥发。如果操作时滴加水过快,测得结果_______ (填“偏高”“偏低”或“无影响”)。

 )、氯化亚砜(
)、氯化亚砜(  )常作氯化剂,用于制造药品、染料和表面活性剂。它们部分性质如下:
)常作氯化剂,用于制造药品、染料和表面活性剂。它们部分性质如下:| 物理性质 | 化学性质 | |
 | 熔点:-54.1℃ 沸点:69.1℃ | ①100℃分解生成 , , ②遇水蒸气产生大量白雾 |
 | 在空气中遇水蒸气发生剧烈反应,产生大量白雾 |
 的原理:
的原理:  。某小组设计实验如图所示(夹持仪器已省略):
。某小组设计实验如图所示(夹持仪器已省略):
回答下列问题:
(1)D中试剂是
(2)实验室常用高锰酸钾固体与浓盐酸在常温下反应制氯气,写出反应的离子方程式
(3)实验室用
 粉末与75%的浓硫酸反应制备
粉末与75%的浓硫酸反应制备  ,发现产生
,发现产生 很少,可能的原因是
很少,可能的原因是 (4)E中碱石灰的作用是
(5)氯化亚砜遇水蒸气发生反应的化学方程式是
 溶液不能得到无水
溶液不能得到无水  ,但是
,但是 和
和 混合物加热,可得到无水
混合物加热,可得到无水  ,其主要原因是
,其主要原因是 (6)为了测定
 产品纯度(杂质不参与反应),称取a g
产品纯度(杂质不参与反应),称取a g 产品于锥形瓶中(如图所示),向锥形瓶中加入足量蒸馏水,充分反应后,用c
产品于锥形瓶中(如图所示),向锥形瓶中加入足量蒸馏水,充分反应后,用c  溶液滴定至终点(滴几滴
溶液滴定至终点(滴几滴 溶液作指示剂),消耗
溶液作指示剂),消耗  溶液为V mL。
溶液为V mL。①用棕色滴定管盛装
 溶液,其原因是
溶液,其原因是 ②该
 产品的纯度为
产品的纯度为 ③实验中,控制分液漏斗活塞,缓慢滴加水,避免氯化氢挥发。如果操作时滴加水过快,测得结果

您最近一年使用:0次
5 . 亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:
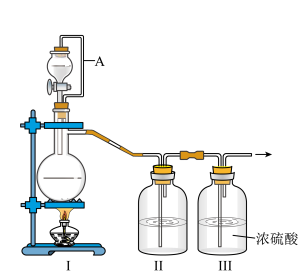
为制备纯净干燥的气体,补充下表中缺少的药品。
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:

①装置连接顺序为a→________________ (按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是____________________ 。
③装置Ⅶ的作用是________________________________________________________ 。
④装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为______________________ 。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为_______________________________________ 。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如图所示:

为制备纯净干燥的气体,补充下表中缺少的药品。
| 装置Ⅰ | 装置Ⅱ | ||
| 烧瓶中 | 分液漏斗中 | ||
| 制备纯净的Cl2 | MnO2 | ① | ② |
| 制备纯净的NO | Cu | ③ | ④ |
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:

①装置连接顺序为a→
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是
③装置Ⅶ的作用是
④装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下混酸可生成亚硝酰氯和氯气,该反应的化学方程式为
您最近一年使用:0次
2017-03-07更新
|
4682次组卷
|
18卷引用:山西省晋城市陵川县高级实验中学2020-2021学年高一下学期3月月考化学试题
山西省晋城市陵川县高级实验中学2020-2021学年高一下学期3月月考化学试题河北省定州中学2017-2018学年高一(承智班)上学期第二次月考化学试题高一必修第二册(人教2019版)第五章 素养检测黑龙江省七台河市勃利县高级中学2021-2022学年高一下学期期中考试化学试题福建省莆田第六中学2018届高三上学期期中考试化学试题湖北省荆州中学2018届高三4月月考理综化学试题2017-2018学年第一学期期末复习备考之精准复习模拟题高三化学(单科)(C卷)黑龙江省青冈县一中2017-2018学年高二下学期期末考试化学试题甘肃省甘谷县第一中学2019届高三上学期第二次检测考试化学试题陕西省渭南中学2019届高三上学期第三次质量检测化学试题【全国百强校】贵州省遵义航天高级中学2019届高三上学期第四次模拟考试理科综合化学试题吉林省吉林市第五十五中学2018-2019学年高二下学期期末考试化学试题专题3.2 非金属及其化合物(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升云南省红河州弥勒市中小学2018-2019学年高二下学期期末考试化学试题山东省枣庄市2021届高三上学期第三次质量检测化学试题云南省陆良县2019届高三毕业班第二次教学质量摸底考化学试题(已下线)01 以无机物质制备为载体的综合型实验 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)(已下线)题型47 物质制备探究型综合实验



