名校
解题方法
1 . X、Y、Z、E、T均为短周期元素,在周期表中的相对位置如图1。X是短周期中原子半径最大的元素; X、Y在同一周期,Y是常见的半导体材料; E的最高价氧化物对应水化物有强脱水性。
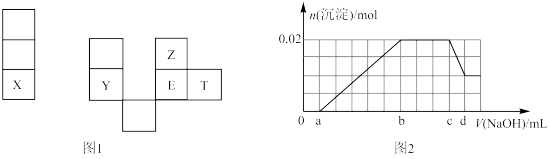
根据判断出的元素回答问题:
(1)T在元素周期表中的位置________________________ ;
(2)这几种元素的氢化物中,水溶液酸性最强的是_____________________ (填化学式);YZ2 的熔点 ______ EZ2 的熔点(填高于或低于);
(3)E2T2 的电子式______________________________ ;
(4)工业上制备单质X的化学反应方程式_______________________ ;
(5)已知1mol晶体Y在足量Z2中燃烧,恢复至室温,放出989.2 kJ热量,写出该反应的热化学方程式:_______________ ;
(6)某溶液中可能含有以下阳离子(忽略由水电离产生的H+、OH-):H+、NH 、K+、Mg2+、Al3+,现取100mL该溶液逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如上图2所示。
、K+、Mg2+、Al3+,现取100mL该溶液逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如上图2所示。
①在实验中,NaOH溶液滴至b~c段过程中发生的离子反应方程式为____________________________ ;NaOH溶液的浓度为_____ mol·L-1 (用字母c、d表示);
②原溶液中含有的Mg2+、Al3+、H+,其物质的量之比n(Mg2+):n(Al3+):n(H+)为_________ 。

根据判断出的元素回答问题:
(1)T在元素周期表中的位置
(2)这几种元素的氢化物中,水溶液酸性最强的是
(3)E2T2 的电子式
(4)工业上制备单质X的化学反应方程式
(5)已知1mol晶体Y在足量Z2中燃烧,恢复至室温,放出989.2 kJ热量,写出该反应的热化学方程式:
(6)某溶液中可能含有以下阳离子(忽略由水电离产生的H+、OH-):H+、NH
 、K+、Mg2+、Al3+,现取100mL该溶液逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如上图2所示。
、K+、Mg2+、Al3+,现取100mL该溶液逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如上图2所示。①在实验中,NaOH溶液滴至b~c段过程中发生的离子反应方程式为
②原溶液中含有的Mg2+、Al3+、H+,其物质的量之比n(Mg2+):n(Al3+):n(H+)为
您最近一年使用:0次
2016-12-09更新
|
437次组卷
|
2卷引用:2016届天津市河东区高考一模考试理科综合化学试卷
2 . 下图是无机物 A~J在一定条件下的转化关系(部分产物及反应条件未列出)。其中C为红棕色气体;H和I是两种常见的金属单质;过量I与 D溶液反应生成A。
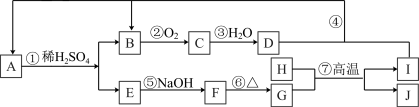
请填写下列空白:
(1)H元素在周期表中的位置是________ ;写出①的离子反应方程式:_________ ;检验E溶液中阳离子的最佳试剂为________ 。
(2)这类反应常用于冶炼高熔点的金属。用MnO2冶炼金属锰的反应中氧化剂与还原剂的物质的量之比为__________ 。
(3)SCR技术处理机动车尾气时,在催化条件下利用氨气与C反应,生成无污染的物质。发生反应的化学方程式为__________ 。
(4)F与NaClO、NaOH溶液反应,可制得一种“绿色”高效净水剂K2FeO4。每生成1molFeO42-时转移____________ mol电子。
(5)B为大气污染物,利用炭粉可以将其还原为无污染的物质X2。
已知:X2(g)+O2(g)=2XO(g) △H=+180.6kJ/mol
C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol
写出用碳粉还原B的热化学方程式__________ 。

请填写下列空白:
(1)H元素在周期表中的位置是
(2)这类反应常用于冶炼高熔点的金属。用MnO2冶炼金属锰的反应中氧化剂与还原剂的物质的量之比为
(3)SCR技术处理机动车尾气时,在催化条件下利用氨气与C反应,生成无污染的物质。发生反应的化学方程式为
(4)F与NaClO、NaOH溶液反应,可制得一种“绿色”高效净水剂K2FeO4。每生成1molFeO42-时转移
(5)B为大气污染物,利用炭粉可以将其还原为无污染的物质X2。
已知:X2(g)+O2(g)=2XO(g) △H=+180.6kJ/mol
C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol
写出用碳粉还原B的热化学方程式
您最近一年使用:0次
解题方法
3 . 各物质之间的转化关系如下图,部分生成物省略。C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10。D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷线路板。请回答下列问题:

(1)G元素在周期表中的位置______________ 。
(2)写出实验室制备G的离子反应方程式___________________ 。
(3)气体D与NaOH溶液反应可生成两种盐P和Q,在P中Na的质量分数为43%,其俗名为____________ 。
(4)实验室中检验L溶液中的阳离子常选用___________ 溶液,现象是_____________ 。
(5)A中包含X、Y、Z元素,A的化学式为____________ 。

(1)G元素在周期表中的位置
(2)写出实验室制备G的离子反应方程式
(3)气体D与NaOH溶液反应可生成两种盐P和Q,在P中Na的质量分数为43%,其俗名为
(4)实验室中检验L溶液中的阳离子常选用
(5)A中包含X、Y、Z元素,A的化学式为
您最近一年使用:0次
4 . 已知A、B、C、D、E、F、G为中学化学中常见的化合物,其中A是淡黄色固体,B是无色液体,G为红褐色沉淀。常温下甲、乙、丙为气态非金属单质,丙呈黄绿色;丁、戊为常见金属单质,其中戊是当前用量最大的金属。它们之间的转化关系如下图所示(有的反应部分产物已经略去)。请根据以上信息回答下列问题:
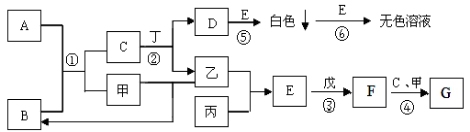
(1)写出下列物质的化学式:A____________ ,E___________ 。
(2)写出丁所含元素在周期表中的位置_______________________ 。
(3)在实验室中,欲检验F溶液中的金属阳离子,先向溶液中滴加几滴_________ 溶液,再加入几滴氯水,观察到溶液变为__________ 色,证明原溶液中的金属阳离子为___________ 。
(4)F转化为G的化学方程式:_______________________________ 。
(5)写出②中反应的离子方程式:_____________________________ 。

(1)写出下列物质的化学式:A
(2)写出丁所含元素在周期表中的位置
(3)在实验室中,欲检验F溶液中的金属阳离子,先向溶液中滴加几滴
(4)F转化为G的化学方程式:
(5)写出②中反应的离子方程式:
您最近一年使用:0次
2013·辽宁·一模
解题方法
5 . 由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有下图的转化关系,已知C为密度最小的气体,甲为非电解质。
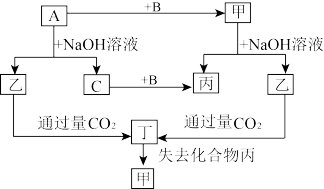
根据以上转化关系回答下列问题:
(1)写出下列物质的化学式:A______ B______ 丁______ 。
(2)元素A在周期表中的位置是______ ,写出甲的一种用途______ 。
(3)写出下列变化的方程式:
A与NaOH溶液反应的化学方程式______
乙与过量CO2反应的离子方程式______

根据以上转化关系回答下列问题:
(1)写出下列物质的化学式:A
(2)元素A在周期表中的位置是
(3)写出下列变化的方程式:
A与NaOH溶液反应的化学方程式
乙与过量CO2反应的离子方程式
您最近一年使用:0次
6 . Ⅰ.A、B、C、D、E、F是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分反应条件略去):
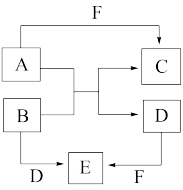
(1)若所有转化都是非氧化还原反应,B、D、E含有同种金属元素,F为强碱(部分产物略去)则B+D→E的离子方程式为________________ ,C为同周期元素构成的1:1型化合物,则C的电子式为___________________ 。
(2)若A、D、F为单质,B、C、E为化合物,B为两种非金属元素所组成的化合物,则E的化学式为___________ ,A+B→C+D的化学方程式为______________________ 。
Ⅱ.亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取来氯酸钠的工艺流程:
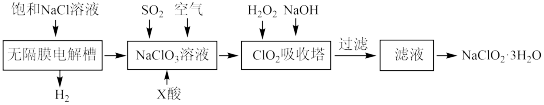
已知:①ClO2气体只能保持在浓度较低状态下以防止爆炸性分解,且需现合成现用 ②ClO2气体在中性和碱性溶液中不能稳定存在。
(3)反应生成ClO2气体需要X酸酸化,X酸可以为_______________ 。
A.盐酸 B.稀硫酸 C.硝酸 D.H2C2O4溶液
(4)吸收塔内的温度不能过高的原因为__________________________ 。
(5)ClO2被S2-还原为ClO2-、Cl-转化率与pH关系如图。
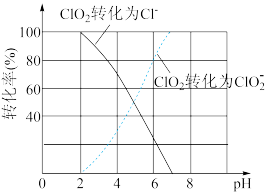
写出pH≤2时ClO2与S2-反应的离子方程式:_______________ 。

(1)若所有转化都是非氧化还原反应,B、D、E含有同种金属元素,F为强碱(部分产物略去)则B+D→E的离子方程式为
(2)若A、D、F为单质,B、C、E为化合物,B为两种非金属元素所组成的化合物,则E的化学式为
Ⅱ.亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取来氯酸钠的工艺流程:

已知:①ClO2气体只能保持在浓度较低状态下以防止爆炸性分解,且需现合成现用 ②ClO2气体在中性和碱性溶液中不能稳定存在。
(3)反应生成ClO2气体需要X酸酸化,X酸可以为
A.盐酸 B.稀硫酸 C.硝酸 D.H2C2O4溶液
(4)吸收塔内的温度不能过高的原因为
(5)ClO2被S2-还原为ClO2-、Cl-转化率与pH关系如图。

写出pH≤2时ClO2与S2-反应的离子方程式:
您最近一年使用:0次



