解题方法
1 . Na及其化合物具有独特的性质和重要的用途。
(1)钠着火时应采取的灭火措施是___________ ,不能用水灭火; 常用于呼吸面具中,有关反应的化学方程式为
常用于呼吸面具中,有关反应的化学方程式为___________ (任写一个即可)。
(2)用洁净的铂丝蘸取 溶液置于酒精灯火焰上灼烧,火焰呈
溶液置于酒精灯火焰上灼烧,火焰呈___________ 色。
(3) 常用于焙制糕点,其原理为
常用于焙制糕点,其原理为___________ 。
(4)向200mL某物质的量浓度的NaOH溶液中缓慢通入一定量的 ,充分反应后,得到含
,充分反应后,得到含 和
和 的混合溶液,向上述所得溶液中,逐滴滴加2
的混合溶液,向上述所得溶液中,逐滴滴加2 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示。
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示。

①OA段、AB段发生反应的离子方程式为___________ 、___________ 。
②B点时,反应后所得溶液中溶质的物质的量浓度是___________  。
。
③混合溶液中 和
和 的质量之比是
的质量之比是___________ 。
(1)钠着火时应采取的灭火措施是
 常用于呼吸面具中,有关反应的化学方程式为
常用于呼吸面具中,有关反应的化学方程式为(2)用洁净的铂丝蘸取
 溶液置于酒精灯火焰上灼烧,火焰呈
溶液置于酒精灯火焰上灼烧,火焰呈(3)
 常用于焙制糕点,其原理为
常用于焙制糕点,其原理为(4)向200mL某物质的量浓度的NaOH溶液中缓慢通入一定量的
 ,充分反应后,得到含
,充分反应后,得到含 和
和 的混合溶液,向上述所得溶液中,逐滴滴加2
的混合溶液,向上述所得溶液中,逐滴滴加2 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示。
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示。
①OA段、AB段发生反应的离子方程式为
②B点时,反应后所得溶液中溶质的物质的量浓度是
 。
。③混合溶液中
 和
和 的质量之比是
的质量之比是
您最近一年使用:0次
2023-11-10更新
|
373次组卷
|
3卷引用:江西省宜春市百树学校2023-2024学年高三上学期11月期中考试化学试卷
解题方法
2 . 回答下列问题:
(1)亚硝酸钠在320℃时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。该反应的化学方程式_____ 。
(2)我国规定火腿肠中亚硝酸钠添加标准为每千克食品含量不超过150毫克,以此计算,200g15%的亚硝酸钠溶液至少可用于生产火腿肠_____ 千克。
(3)在酸性条件下,NaNO2与I-按物质的量1:1恰好完全反应,且I-被氧化为I2时,产物中含氮的物质为_____ (填化学式)。
(4)工业废水中的NaNO2可用铝粉除去,已知此体系中包含AI、NaAlO2、NaNO2、NaOH、NH3、H2O六种物质。该反应的化学方程式为_____ 。
(1)亚硝酸钠在320℃时能分解产生氧化钠固体、一氧化氮和一种常见的助燃性气体。该反应的化学方程式
(2)我国规定火腿肠中亚硝酸钠添加标准为每千克食品含量不超过150毫克,以此计算,200g15%的亚硝酸钠溶液至少可用于生产火腿肠
(3)在酸性条件下,NaNO2与I-按物质的量1:1恰好完全反应,且I-被氧化为I2时,产物中含氮的物质为
(4)工业废水中的NaNO2可用铝粉除去,已知此体系中包含AI、NaAlO2、NaNO2、NaOH、NH3、H2O六种物质。该反应的化学方程式为
您最近一年使用:0次
名校
3 . 某活动小组用碳素钢进行了如下活动:
(1)常温下,可以用铁质容器盛放冷的浓硫酸,其原因是___________ ;
(2)称取碳素钢 放入
放入 浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学认为X中除 之外还可能含有
之外还可能含有 。若要确认其中的
。若要确认其中的 ,应选用
,应选用___________ (选填序号)。
A. 溶液和氯水 B、铁粉和
溶液和氯水 B、铁粉和 溶液
溶液
C.浓氨水 D.酸性 溶液
溶液
②乙同学取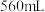 (标准状况)气体Y通入足量溴水中,溴水褪色,由此推知混合气体Y中含有
(标准状况)气体Y通入足量溴水中,溴水褪色,由此推知混合气体Y中含有___________ ,其化学方程式为:___________ ,然后加入足量 溶液,经适当操作后得干燥固体
溶液,经适当操作后得干燥固体 ,由此推知气体Y中该气体的体积分数为
,由此推知气体Y中该气体的体积分数为___________ 。
(3)将下列物质进行分类(填序号)
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦盐酸 ⑧乙醇
⑦盐酸 ⑧乙醇
属于电解质的是___________ ;
属于非电解质的是___________ ;
能导电的是___________ 。
(1)常温下,可以用铁质容器盛放冷的浓硫酸,其原因是
(2)称取碳素钢
 放入
放入 浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。①甲同学认为X中除
 之外还可能含有
之外还可能含有 。若要确认其中的
。若要确认其中的 ,应选用
,应选用A.
 溶液和氯水 B、铁粉和
溶液和氯水 B、铁粉和 溶液
溶液C.浓氨水 D.酸性
 溶液
溶液②乙同学取
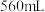 (标准状况)气体Y通入足量溴水中,溴水褪色,由此推知混合气体Y中含有
(标准状况)气体Y通入足量溴水中,溴水褪色,由此推知混合气体Y中含有 溶液,经适当操作后得干燥固体
溶液,经适当操作后得干燥固体 ,由此推知气体Y中该气体的体积分数为
,由此推知气体Y中该气体的体积分数为(3)将下列物质进行分类(填序号)
①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦盐酸 ⑧乙醇
⑦盐酸 ⑧乙醇属于电解质的是
属于非电解质的是
能导电的是
您最近一年使用:0次
2022-01-27更新
|
127次组卷
|
2卷引用:辽宁省大连市庄河市高级中学2022-2023学年高三上学期12月月考化学(B卷)试题
解题方法
4 . 白居易《暮江吟》,“一道残阳铺水中,半江瑟瑟半江红。”诗句中“瑟瑟”指像绿松石似的碧绿色,绿松石的化学式为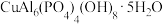 ,另含少量埃洛石(
,另含少量埃洛石(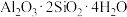 ),石英(
),石英( )、褐铁矿[
)、褐铁矿[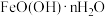 ]等杂质。回答下列问题:
]等杂质。回答下列问题:
(1) 在周期表中的位置为
在周期表中的位置为___________ ,离子半径
___________ (填“>”或“<”) 。
。
(2)检验绿松石含铜的较简单的方法是___________ ;若将绿松石写成氧化物形式(参照埃洛石),则理论上 的质量分数为
的质量分数为___________ %(结果保留三位有效数字)。
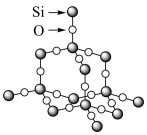
(3)已知 的结构如图所示。
的结构如图所示。 石英中含
石英中含 键的数目为
键的数目为___________ 。
(4)褐铁矿溶于稀硫酸的离子方程式为___________ 。
(5) 固态时是一种离子化合物,阳离子比阴离子少36个电子,阳离子中各原子均达到八电子稳定结构,该离子化合物的化学式为
固态时是一种离子化合物,阳离子比阴离子少36个电子,阳离子中各原子均达到八电子稳定结构,该离子化合物的化学式为___________ 。
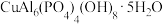 ,另含少量埃洛石(
,另含少量埃洛石(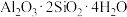 ),石英(
),石英( )、褐铁矿[
)、褐铁矿[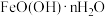 ]等杂质。回答下列问题:
]等杂质。回答下列问题:(1)
 在周期表中的位置为
在周期表中的位置为
 。
。(2)检验绿松石含铜的较简单的方法是
 的质量分数为
的质量分数为(3)已知
 的结构如图所示。
的结构如图所示。 石英中含
石英中含 键的数目为
键的数目为
(4)褐铁矿溶于稀硫酸的离子方程式为
(5)
 固态时是一种离子化合物,阳离子比阴离子少36个电子,阳离子中各原子均达到八电子稳定结构,该离子化合物的化学式为
固态时是一种离子化合物,阳离子比阴离子少36个电子,阳离子中各原子均达到八电子稳定结构,该离子化合物的化学式为
您最近一年使用:0次
5 . 向100 mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2 mol·L-1的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示:

(1)原NaOH溶液的浓度为_______
(2)通入CO2在标准状况下的体积为_______ mL
(3)所得溶液的溶质成分及物质的量之比为_______
(4)在配制盐酸溶液时,将标况下VLHCl气体溶于100mL水中,所得溶液密度为d g·cm-3,则此溶液的物质的量浓度为_______ mol·L-1

(1)原NaOH溶液的浓度为
(2)通入CO2在标准状况下的体积为
(3)所得溶液的溶质成分及物质的量之比为
(4)在配制盐酸溶液时,将标况下VLHCl气体溶于100mL水中,所得溶液密度为d g·cm-3,则此溶液的物质的量浓度为
您最近一年使用:0次
2021-10-26更新
|
255次组卷
|
2卷引用:天津市静海区第一中学2021-2022学年高三上学期(9月)学生学业能力调研化学试题
6 . 铬及其化合物在工业上有重要的用途。铬元素的化合价可以是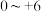 的整数价态。请根据如下转化关系图回答问题:
的整数价态。请根据如下转化关系图回答问题:
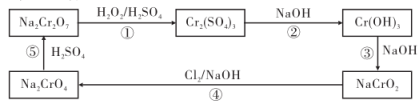
(1)框图中的含铬化合物中,铬元素为 价的盐有
价的盐有___________ 。
(2)反应①中氧化剂与还原剂的物质的量之比为___________ 。
(3)根据反应②、③,知 类似
类似 具有两性,请写出
具有两性,请写出 的酸式电离方程式:
的酸式电离方程式:___________ 。
(4)反应④的离子方程式为___________ 。
(5)目前处理酸性 废水多采用铁氧磁体法。该法是向废水中加入
废水多采用铁氧磁体法。该法是向废水中加入 将
将 还原成
还原成 ,调节
,调节 ,
, 、
、 全部转化成相当于
全部转化成相当于 (铁氧磁体,罗马数字表示元素价态)的沉淀。处理
(铁氧磁体,罗马数字表示元素价态)的沉淀。处理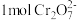 ,需加入
,需加入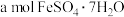 ,下列有关结论正确的是___________。
,下列有关结论正确的是___________。
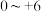 的整数价态。请根据如下转化关系图回答问题:
的整数价态。请根据如下转化关系图回答问题:
(1)框图中的含铬化合物中,铬元素为
 价的盐有
价的盐有(2)反应①中氧化剂与还原剂的物质的量之比为
(3)根据反应②、③,知
 类似
类似 具有两性,请写出
具有两性,请写出 的酸式电离方程式:
的酸式电离方程式:(4)反应④的离子方程式为
(5)目前处理酸性
 废水多采用铁氧磁体法。该法是向废水中加入
废水多采用铁氧磁体法。该法是向废水中加入 将
将 还原成
还原成 ,调节
,调节 ,
, 、
、 全部转化成相当于
全部转化成相当于 (铁氧磁体,罗马数字表示元素价态)的沉淀。处理
(铁氧磁体,罗马数字表示元素价态)的沉淀。处理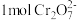 ,需加入
,需加入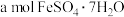 ,下列有关结论正确的是___________。
,下列有关结论正确的是___________。A.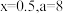 | B.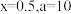 |
C.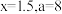 | D. |
您最近一年使用:0次
7 . 四氧化三锰主要用于电子工业,是生产软磁铁氧体的原料之一。
(1)四氧化三锰的制法有焙烧法和还原法两类。在还原法中,先将水锰矿(主要成分MnOOH)焙烧成三氧化二锰,再于250~500℃用甲烷还原生成四氧化三锰。请写出上述二步反应的化学方程式_______ 。
(2)通常所说的四氧化三锰中,锰的价态实际上既有二价,也有三价和四价。在某研究工作中,要求得知四氧化三锰中不同价态锰的比值,采用的测定方法步骤如下:
i.称取3份质量相同的试样。第一份以硫酸铵-硫酸溶液选择性溶解试样中的二价锰,过滤洗涤后,滤液用氨水中和并。用氨一氯化铵缓冲溶液调至pH10,加入必要的试剂和指示剂,用EDTA标准溶液(a1mol·L-1)滴定至终点,耗去b1mL。
ii.第二份试样中,准确加入过量的草酸钠标准溶液(a2mol·L-1,b2mL)和适量硫酸,加热使试样全部溶解,立即用高锰酸钾标准溶液(a3mol·L-1)滴定剩余的还原剂至终点,耗去b3mL。
iii.第三份试样中,同样加入过量的草酸钠标准溶液和适量硫酸,加热使全部溶解。冷却后用氨水中和并用氨-氯化铵缓冲溶液调至pH10,加入必要的试剂和指示剂,用EDTA标准溶液滴定至终点,耗去b4mL。
①写出步骤ii溶解试样时,不同价态锰的氧化物同草酸之间反应的化学方程式_______ ;写出用高锰酸钾滴定剩余还原剂的化学方程式_______ 。
②用a1、a2、a3、b1、b2、b3和b4写出试样中二价、三价和四价锰含量(分别用X、Y、Z表示)的计算式_______ ,单位用mmol表示。
(1)四氧化三锰的制法有焙烧法和还原法两类。在还原法中,先将水锰矿(主要成分MnOOH)焙烧成三氧化二锰,再于250~500℃用甲烷还原生成四氧化三锰。请写出上述二步反应的化学方程式
(2)通常所说的四氧化三锰中,锰的价态实际上既有二价,也有三价和四价。在某研究工作中,要求得知四氧化三锰中不同价态锰的比值,采用的测定方法步骤如下:
i.称取3份质量相同的试样。第一份以硫酸铵-硫酸溶液选择性溶解试样中的二价锰,过滤洗涤后,滤液用氨水中和并。用氨一氯化铵缓冲溶液调至pH10,加入必要的试剂和指示剂,用EDTA标准溶液(a1mol·L-1)滴定至终点,耗去b1mL。
ii.第二份试样中,准确加入过量的草酸钠标准溶液(a2mol·L-1,b2mL)和适量硫酸,加热使试样全部溶解,立即用高锰酸钾标准溶液(a3mol·L-1)滴定剩余的还原剂至终点,耗去b3mL。
iii.第三份试样中,同样加入过量的草酸钠标准溶液和适量硫酸,加热使全部溶解。冷却后用氨水中和并用氨-氯化铵缓冲溶液调至pH10,加入必要的试剂和指示剂,用EDTA标准溶液滴定至终点,耗去b4mL。
①写出步骤ii溶解试样时,不同价态锰的氧化物同草酸之间反应的化学方程式
②用a1、a2、a3、b1、b2、b3和b4写出试样中二价、三价和四价锰含量(分别用X、Y、Z表示)的计算式
您最近一年使用:0次
8 . 银及其化合物在制造钱币、电子工业、医药等方面具有广泛用途。
Ⅰ.银的冶炼及性质
(1)热分解法是金属冶炼方法之一。以Ag2O为原料冶炼银的化学方程式为__ 。
(2)电解精炼银的工作原理如图所示,___ (填“a”或“b”)极为含有杂质的粗银,若b极有少量红棕色气体生成,则生成该气体的电极反应式为___ 。
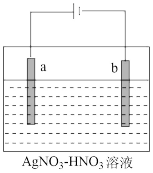
Ⅱ.银的化合物的性质
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式__ 。
(4)在光照条件下,AgNO3可分解为Ag、O2和某种氮的氧化物。称取34g AgNO3固体,充分光照使其完全分解,测得反应后生成O2的体积(折合成标准状况)为2.24L,反应过程中转移电子的物质的量为__ 。
(5)纳米硫化(Ag2S)应用广泛。Ag2S溶于浓HNO3后,产生淡黄色固体及无色气体,该气体遇空气迅速变为红棕色。写出反应的化学方程式__ 。
Ⅰ.银的冶炼及性质
(1)热分解法是金属冶炼方法之一。以Ag2O为原料冶炼银的化学方程式为
(2)电解精炼银的工作原理如图所示,

Ⅱ.银的化合物的性质
(3)在AgCl沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式
(4)在光照条件下,AgNO3可分解为Ag、O2和某种氮的氧化物。称取34g AgNO3固体,充分光照使其完全分解,测得反应后生成O2的体积(折合成标准状况)为2.24L,反应过程中转移电子的物质的量为
(5)纳米硫化(Ag2S)应用广泛。Ag2S溶于浓HNO3后,产生淡黄色固体及无色气体,该气体遇空气迅速变为红棕色。写出反应的化学方程式
您最近一年使用:0次
2021-05-03更新
|
598次组卷
|
4卷引用:北京市丰台区2021届高三第二次模拟考试化学试题
北京市丰台区2021届高三第二次模拟考试化学试题(已下线)第二章能力提升检测卷-2022年高考化学一轮复习讲练测(已下线)第二章 化学物质及其变化(测)-2023年高考化学一轮复习讲练测(全国通用)北京市第三中学2021-2022学年高三上学期期中考试化学试题
解题方法
9 . 硒是人体必需的微量元素,有无机硒和有机硒之分。
(1)硒与硫在元素周期表中的相对位置如图所示,硒在元素周期表中的位置是_______ ;硒化氢的电子式为_______ 。
(2)二硫化硒(SeS2)具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。SeS2中硫化素的化合价为负价,请从原子结构角度解释原因:_______ 。
(3)硒与硫相似,可形成多种盐。写出含不同价态硒元素的钠盐的化学式_______ (至少两种)。
(4)一种有机硒化合物的结构简式为: ,其分子式为
,其分子式为_______ ,其分子间脱水时形成的官能团的名称是_______ 。
(5)工业上提取硒的过程如下:
第一步(未配平):X+Se+H2SO4→Na2SO4+H2SeO3+ClO2↑+H2O
已知该反应中氧化产物与还原产物的物质的量之比为1:4,则X的化学式为_______ 。
第二步:向H2SeO3溶液中通入SO2,可析出固体Se,则反应化学方程式为_______ 。
| S |
| Se |
(1)硒与硫在元素周期表中的相对位置如图所示,硒在元素周期表中的位置是
(2)二硫化硒(SeS2)具有抗真菌、抗皮脂溢出作用,常用作洗发香波中的去屑剂。SeS2中硫化素的化合价为负价,请从原子结构角度解释原因:
(3)硒与硫相似,可形成多种盐。写出含不同价态硒元素的钠盐的化学式
(4)一种有机硒化合物的结构简式为:
 ,其分子式为
,其分子式为(5)工业上提取硒的过程如下:
第一步(未配平):X+Se+H2SO4→Na2SO4+H2SeO3+ClO2↑+H2O
已知该反应中氧化产物与还原产物的物质的量之比为1:4,则X的化学式为
第二步:向H2SeO3溶液中通入SO2,可析出固体Se,则反应化学方程式为
您最近一年使用:0次
解题方法
10 . 玻璃仪器内壁残留的硫单质可用热KOH溶液洗涤除去,发生如下反应:
3S + 6KOH 2K2S+ K2SO3+3H2O
2K2S+ K2SO3+3H2O
(x-1)S+K2S K2Sx(x=2~6)
K2Sx(x=2~6)
S+ K2SO3 K2S2O3
K2S2O3
请计算:
(1)0.480 g硫单质与V mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2S和K2SO3,则V=_______ mL。
(2)3.840 g硫单质与60.0 mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2Sx和K2S2O3,则x=_______ 。
3S + 6KOH
 2K2S+ K2SO3+3H2O
2K2S+ K2SO3+3H2O(x-1)S+K2S
 K2Sx(x=2~6)
K2Sx(x=2~6)S+ K2SO3
 K2S2O3
K2S2O3请计算:
(1)0.480 g硫单质与V mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2S和K2SO3,则V=
(2)3.840 g硫单质与60.0 mL 1.00 mol·L-1热KOH溶液恰好完全反应,只生成K2Sx和K2S2O3,则x=
您最近一年使用:0次



