名校
解题方法
1 . 将8.0g镁铁合金加入500mL稀盐酸中恰好完全反应,得到标准状况下氢气4.48L。下列有关说法不正确的是
| A.该合金中镁、铁的物质的量之比为1:1 |
| B.反应中转移电子0.6mol |
| C.该盐酸的物质的量浓度为0.8mol/L |
| D.将标准状况下8.96LHCl气体溶于500mL水中即可配制成该盐酸 |
您最近一年使用:0次
名校
解题方法
2 . 向200mLFe2(SO4)3和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中固体剩余物的质量与加入铁粉的质量如图所示。忽略溶液体积的变化,下列说法不正确的是
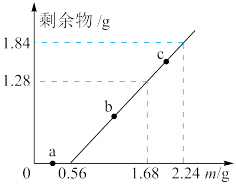

| A.a点时溶液中发生的反应为:Fe+Cu2+=Cu+Fe2+ |
| B.b点时溶液中的阳离子有:Cu2+、Fe2+ |
| C.c点时溶液中溶质的物质的量浓度为0.25mol/L |
| D.原溶液中Fe2(SO4)3和CuSO4的物质的量浓度之比为1∶1 |
您最近一年使用:0次
2022-12-10更新
|
350次组卷
|
2卷引用:江西省吉安市泰和黄冈学校2021-2022学年高一上学期期末考试化学试题
解题方法
3 . 向200mL1.5mol•L-1FeBr2溶液中逐渐通入Cl2,其中n(Fe2+):n(Br-)随通入Cl2的物质的量n(Cl2)变化如图所示。下列说法错误的是


| A.①代表Br-,②代表Fe2+ |
| B.还原性强弱:Fe2+>Br- |
| C.n(Cl2)=0.35mol时,溶液中c(Fe3+)=c(Br-) |
| D.n(Cl2)=0.45mol时,总的离子方程式为2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
您最近一年使用:0次
4 . 1.52g铜镁合金完全溶解于50mL密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法正确的是
| A.该浓硝酸中HNO3的物质的量浓度为14mol/L |
| B.该合金中铜与镁的物质的量之比为1:2 |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.得到2.54 g沉淀时,加入NaOH溶液的体积是600mL |
您最近一年使用:0次
2022-08-21更新
|
943次组卷
|
3卷引用:江西省景德镇一中2021-2022学年高一下学期期中质量检测(17)班化学试题
名校
5 . 物质W常用作漂白剂和氧化剂,其构成元素均为短周期主族元素,各元素原子半径与原子序数的关系如图所示,实验室中常用CS2洗涤残留在试管壁上的N单质。下列说法正确的是
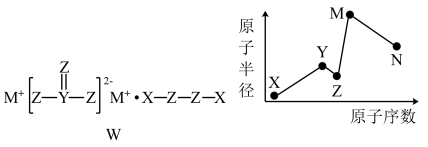

| A.X、Z形成的化合物与M、N形成的化合物可以发生氧化还原反应 |
| B.实验室中用CS2洗涤残留在试管壁上的N单质,利用了N单质的还原性 |
| C.Z的氢化物的沸点一定大于Y的氢化物的沸点 |
| D.化合物W常用作氧化剂,不宜在高温下使用 |
您最近一年使用:0次
2022-07-12更新
|
1721次组卷
|
8卷引用:江西省丰城中学2022-2023学年高一上学期期中考试化学试题(创新班)
江西省丰城中学2022-2023学年高一上学期期中考试化学试题(创新班)山东省日照市2021-2022学年高一下学期期末考试化学试题湖南长沙麓山国际实验中学2022-2023学年高一上学期期末线上化学试题湖南省株洲市九方中学2022-2023学年高三上学期第三次月考化学试题山东省新泰市第一中学2022-2023学年高一下学期第一次阶段性考试检测化学试题(已下线)查补易混易错03 基本概念和基础理论部分-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)辽宁省沈阳市东北育才学校2022-2023学年高三高考适应性测试(二)化学试题河北省部分高中2023-2024学年高三上学期12月期末化学试题
名校
解题方法
6 . 以高硫铝土矿(主要成分为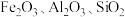 ,少量
,少量 和硫酸盐)为原料制备聚合硫酸铁
和硫酸盐)为原料制备聚合硫酸铁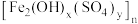 和明矾的部分工艺流程如下,下列说法错误的是
和明矾的部分工艺流程如下,下列说法错误的是
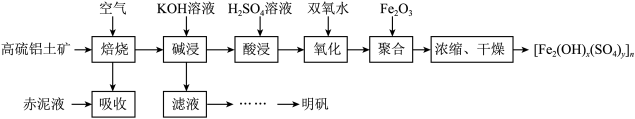
已知:赤泥液的主要成分为
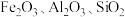 ,少量
,少量 和硫酸盐)为原料制备聚合硫酸铁
和硫酸盐)为原料制备聚合硫酸铁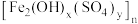 和明矾的部分工艺流程如下,下列说法错误的是
和明矾的部分工艺流程如下,下列说法错误的是
已知:赤泥液的主要成分为

A.赤泥液的作用是吸收“焙烧”阶段中产生的 |
B.聚合硫酸铁可用于净化自来水,与其组成中的 具有氧化性有关 具有氧化性有关 |
C.在“聚合”阶段,若增加 用量,会使 用量,会使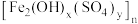 中x变小 中x变小 |
| D.从“滤液”到“明矾”的过程中还应有“除硅”步骤 |
您最近一年使用:0次
2022-05-12更新
|
828次组卷
|
7卷引用:江西省景德镇市第一中学2021-2022学年高二上学期期末(重点班)化学试题
江西省景德镇市第一中学2021-2022学年高二上学期期末(重点班)化学试题湖南省郴州市第一中学2022届高三下学期期中考试化学试题湖南省常宁市第一中学2022届高三下学期第三次模拟考试化学试题河南省大联考2022届高三上学期阶段性测试(一)化学试题(已下线)第二单元 化学物质及其变化(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)福建省龙岩第一中学2021-2022学年高三上学期第二次月考化学试题山西省怀仁市2021-2022学年高三上学期期中化学试题
名校
7 . 部分氧化的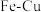 合金样品(氧化产物为
合金样品(氧化产物为 、
、 )共5.76g,经如图处理:
)共5.76g,经如图处理:

下列说法不正确的是
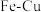 合金样品(氧化产物为
合金样品(氧化产物为 、
、 )共5.76g,经如图处理:
)共5.76g,经如图处理:
下列说法不正确的是
A.滤液A中的阳离子为Fe3+、Fe2+、 |
B.样品中 元素的质量为2.24g 元素的质量为2.24g |
C.溶解样品参与反应的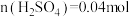 |
| D.V=896ml |
您最近一年使用:0次
名校
8 . 用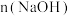 为
为 的
的 浓溶液吸收一定量的氯气,充分反应后溶液中只含有
浓溶液吸收一定量的氯气,充分反应后溶液中只含有 、
、 、
、 三种溶质。下列判断正确的是
三种溶质。下列判断正确的是
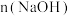 为
为 的
的 浓溶液吸收一定量的氯气,充分反应后溶液中只含有
浓溶液吸收一定量的氯气,充分反应后溶液中只含有 、
、 、
、 三种溶质。下列判断正确的是
三种溶质。下列判断正确的是A.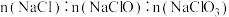 可能为 可能为 |
B.若反应中转移的电子的物质的量为 ,则 ,则 |
C.被吸收的氯气的物质的量为 |
D. 可能为 可能为 |
您最近一年使用:0次
2021-12-01更新
|
907次组卷
|
6卷引用:江西省宜春市铜鼓中学2021-2022学年高一下学期开学考化学试题
解题方法
9 . 无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用Al和氯气通过下装置制备。已知A中产生的氯气混有少许HCl和水蒸气。则下列说法正确的是
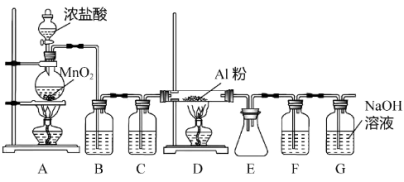

| A.试剂瓶B、C、F中分别盛饱和NaHCO3、浓硫酸、浓硫酸 |
| B.氯化铝产品最后在装置E中收集 |
| C.A、D两处酒精灯,实验开始时应先点燃A处 |
| D.装置F和G可用盛无水CaCl2的干燥管替换 |
您最近一年使用:0次
2021-11-26更新
|
1434次组卷
|
2卷引用:江西省丰城市第九中学2021-2022学年高一上学期第二次月考化学试卷
名校
解题方法
10 . A. B、C、D、E是原子序数依次增大的五种短周期元素且B、C相邻,A元素可以与B、C、E元素分别形成甲、乙、丙三种物质且甲、乙均为10电子化合物,丙为18电子化合物。D元素的最外层电子数与核外电子层数相等。已知:甲+ E2=丙+ B2,甲+丙=丁, 下列说法中正确的是
| A.离子半径: D>C> B |
| B.A与B两种元素共同形成的10电子粒子至少有3种 |
| C.D元素在周期表中的位置是第三周期第IIIA族 |
| D.丁物质属离子化合物 |
您最近一年使用:0次
2021-07-15更新
|
708次组卷
|
2卷引用:江西省景德镇市第一中学2021-2022学年高二上学期期末(重点班)化学试题



