解题方法
1 . 短周期元素W、X、Y、Z、Q,原子序数依次增大,W原子没有中子,X元素为地壳中含量最多的元素,Y、Z、Q同周期,且Y、Z、Q最外层电子数之和为14,Y与W同主族,下列结论不正确的是
| A.原子半径大小顺序为Y>Z>Q>X>W |
| B.W、X、Y形成的化合物中只有共价键 |
| C.X、Y可以形成的原子个数比1:1或1:2的化合物 |
| D.最高价氧化物对应的水化物酸性Z>Q |
您最近一年使用:0次
名校
解题方法
2 . 向200mLFe2(SO4)3和CuSO4的混合溶液中逐渐加入铁粉,充分反应后溶液中固体剩余物的质量与加入铁粉的质量如图所示。忽略溶液体积的变化,下列说法不正确的是
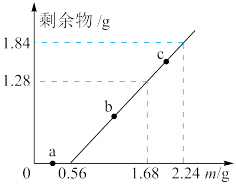

| A.a点时溶液中发生的反应为:Fe+Cu2+=Cu+Fe2+ |
| B.b点时溶液中的阳离子有:Cu2+、Fe2+ |
| C.c点时溶液中溶质的物质的量浓度为0.25mol/L |
| D.原溶液中Fe2(SO4)3和CuSO4的物质的量浓度之比为1∶1 |
您最近一年使用:0次
2022-12-10更新
|
350次组卷
|
2卷引用:江西省吉安市泰和黄冈学校2021-2022学年高一上学期期末考试化学试题
解题方法
3 . 向200mL1.5mol•L-1FeBr2溶液中逐渐通入Cl2,其中n(Fe2+):n(Br-)随通入Cl2的物质的量n(Cl2)变化如图所示。下列说法错误的是


| A.①代表Br-,②代表Fe2+ |
| B.还原性强弱:Fe2+>Br- |
| C.n(Cl2)=0.35mol时,溶液中c(Fe3+)=c(Br-) |
| D.n(Cl2)=0.45mol时,总的离子方程式为2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
您最近一年使用:0次
解题方法
4 . 某实验需要使用 的硫酸铜溶液,现用
的硫酸铜溶液,现用 配制该溶液,下列仪器中,肯定不需要使用的是
配制该溶液,下列仪器中,肯定不需要使用的是
 的硫酸铜溶液,现用
的硫酸铜溶液,现用 配制该溶液,下列仪器中,肯定不需要使用的是
配制该溶液,下列仪器中,肯定不需要使用的是| A | B | C | D |
 |  |  |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 1.52g铜镁合金完全溶解于50mL密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法正确的是
| A.该浓硝酸中HNO3的物质的量浓度为14mol/L |
| B.该合金中铜与镁的物质的量之比为1:2 |
| C.NO2和N2O4的混合气体中,NO2的体积分数是80% |
| D.得到2.54 g沉淀时,加入NaOH溶液的体积是600mL |
您最近一年使用:0次
2022-08-21更新
|
943次组卷
|
3卷引用:江西省吉安市遂川中学2022-2023学年高一上学期期末考试化学试题
名校
6 . 下列物质中,既能和盐酸反应,又能和氢氧化钠反应的是
| A.NaHCO3 | B.Na2CO3 | C.Al2O3 | D.Fe(OH)3 |
您最近一年使用:0次
2022-03-02更新
|
135次组卷
|
2卷引用:江西省吉安市泰和黄冈学校2021-2022学年高一上学期期末考试化学试题
7 . 下表中,陈述I和陈述II均正确且两者之间有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | Na2CO3可与盐酸反应 | 碳酸钠溶液可用于治疗胃酸过多 |
| B | Al具有良好的延展性和抗腐蚀性 | Al可制成铝箔包装物品 |
| C | 常温下,金属钠在空气中会生成过氧化钠 | 金属钠保存在煤油中,以隔绝空气 |
| D | Fe2O3是红棕色粉末 | Fe2O3可用作红色颜料 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 研究表明:多种海产品体内含有+5价的砷(As)元素,对人体无毒,而砒霜的成分是As2O3,有剧毒;青菜中含有维生素C。专家忠告:不要同时大量食用海鲜和青菜,否则容易中毒。下面有关解释正确的是
| A.As2O3中As元素为+3价 |
| B.维生素C能将+5价砷还原成As2O3 |
| C.致人中毒过程中砷发生氧化反应 |
| D.维生素C具有氧化性 |
您最近一年使用:0次
2016-12-09更新
|
203次组卷
|
5卷引用:江西省吉安市2021-2022学年高一上学期期末考试化学试题



