1 . 溴化亚铜(CuBr)微溶于水,不溶于乙醇,可用作有机合成中的催化剂。实验室可利用无水硫酸铜、溴化钠为主要原料制备溴化亚铜,流程如图:

已知:产率 =(实际产量/理论产量)×100%
(1)制备CuBr的反应在装置乙中进行,向其中加入32 g CuSO4和23 g NaBr配制成150 mL水溶液,然后通入足量的SO2(部分夹持及加热装置已略去)。
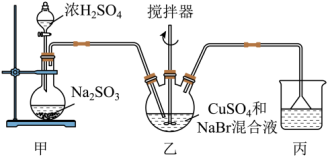
①装置甲中,不能采用稀硫酸,一般采用70%左右的浓硫酸,其原因是___________ 。
②写出装置乙中发生反应的离子方程式:___________ ,该反应需保持反应液在60℃,最佳加热方式为___________ 。
(2)洗涤CuBr沉淀时采用SO2的水溶液而不采用蒸馏水,其目的是___________ 。
(3)最后经洗涤、干燥得到24.48 g产品,则该实验的产率是___________ 。(保留两位有效数字)

已知:产率 =(实际产量/理论产量)×100%
(1)制备CuBr的反应在装置乙中进行,向其中加入32 g CuSO4和23 g NaBr配制成150 mL水溶液,然后通入足量的SO2(部分夹持及加热装置已略去)。

①装置甲中,不能采用稀硫酸,一般采用70%左右的浓硫酸,其原因是
②写出装置乙中发生反应的离子方程式:
(2)洗涤CuBr沉淀时采用SO2的水溶液而不采用蒸馏水,其目的是
(3)最后经洗涤、干燥得到24.48 g产品,则该实验的产率是
您最近一年使用:0次
2 . 非金属单质A经下图所示的过程可转化为含氧酸D,已知D为强酸。

(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是___________ 。
②在工业生产中,B气体大量排放,被雨水吸收后会形成___________ 污染环境。
(2)若A在常温下为气体,C是红棕色的气体。
①C和H2O反应生成D的过程中,氧化剂和还原剂的质量之比为___________ 。
②2mol锌和含5mol溶质的D溶液恰好完全反应,若反应只生成一种还原产物,则该还原产物为___________ 或___________ 。(填化学式)

(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是
②在工业生产中,B气体大量排放,被雨水吸收后会形成
(2)若A在常温下为气体,C是红棕色的气体。
①C和H2O反应生成D的过程中,氧化剂和还原剂的质量之比为
②2mol锌和含5mol溶质的D溶液恰好完全反应,若反应只生成一种还原产物,则该还原产物为
您最近一年使用:0次
3 . 钛铁矿(FeTiO3,其中Ti为+4价)在高温下经氯化得到四氯化钛,然后和Mg反应生成金属钛。其流程如图所示:
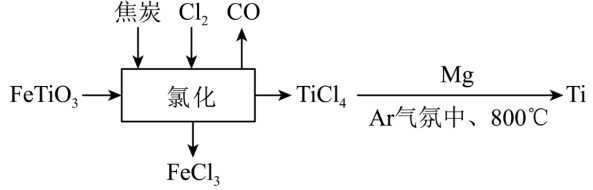
下列说法正确的是

下列说法正确的是
| A.制取金属钛时通Ar气的目的是隔绝空气 |
| B.氯化过程中氧化剂为Cl2 ,还原剂为焦炭 |
| C.根据流程,可推测在高温条件下的还原性:Ti>Mg |
| D.氯化过程中,每消耗22.4 L的氯气转移2 mol电子 |
您最近一年使用:0次
解题方法
4 . 下列各组离子能在溶液中大量共存的是
A.Na+、Fe2+、 、H+ 、H+ | B.Na+、OH-、HCO 、 、 |
C.K+、NH 、SO 、SO 、OH- 、OH- | D.H+、Cu2+、 、SO 、SO |
您最近一年使用:0次
2023-07-11更新
|
488次组卷
|
2卷引用:新疆维吾尔自治区昌吉回族自治州2022-2023学年高一下学期期末考试化学试题
解题方法
5 . 绿色化学的核心就是利用化学原理和技术手段从源头上减少或消除工业生产对环境的污染。下列做法不符合“绿色化学”理念的是
| A.尽可能采用对人类和环境无毒无害的合成路线 |
| B.用可降解塑料生产包装盒或快餐盒 |
| C.制备硝酸铜不用Cu和浓硝酸反应,应用Cu和稀硝酸反应 |
D.用反应2CH2=CH2 + O2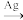 2 2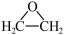 制备环氧乙烷 制备环氧乙烷 |
您最近一年使用:0次
名校
解题方法
6 . 如图为铁及其化合物的“价一类”二维图。
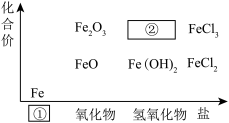
(1)填写二维图缺失的化学式②___________ 。
(2)利用以下试剂研究 性质,进行了如下预测:
性质,进行了如下预测:
a. b.Fe c.NaOH d.
b.Fe c.NaOH d. e.
e.
从物质类别上看, 属于盐,可能与
属于盐,可能与___________ 发生反应(填序号);从化合价角度看,体现 氧化性,可能与
氧化性,可能与___________ 反应(填序号)。
(3) 具有较强的还原性,容易被一些氧化剂氧化为
具有较强的还原性,容易被一些氧化剂氧化为 。
。
①向 溶液中加入KSCN溶液,无明显现象,再加入氯水,溶液变血红色。
溶液中加入KSCN溶液,无明显现象,再加入氯水,溶液变血红色。 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
②配制含 的溶液时,为防止
的溶液时,为防止 被氧化,应向溶液中加入少量
被氧化,应向溶液中加入少量___________ ,目的是___________ (用离子方程式表示)。
(4)工业中常用高铁酸钾( )作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成
)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成 胶体吸附杂质净水,同时还产生一种气体,该原理的离子方程式为
胶体吸附杂质净水,同时还产生一种气体,该原理的离子方程式为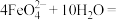
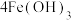 (胶体)
(胶体)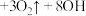 ,每生成1个
,每生成1个 ,
, 转移的电子数目为
转移的电子数目为___________ 个。

(1)填写二维图缺失的化学式②
(2)利用以下试剂研究
 性质,进行了如下预测:
性质,进行了如下预测:a.
 b.Fe c.NaOH d.
b.Fe c.NaOH d. e.
e.
从物质类别上看,
 属于盐,可能与
属于盐,可能与 氧化性,可能与
氧化性,可能与(3)
 具有较强的还原性,容易被一些氧化剂氧化为
具有较强的还原性,容易被一些氧化剂氧化为 。
。①向
 溶液中加入KSCN溶液,无明显现象,再加入氯水,溶液变血红色。
溶液中加入KSCN溶液,无明显现象,再加入氯水,溶液变血红色。 与
与 反应的离子方程式为
反应的离子方程式为②配制含
 的溶液时,为防止
的溶液时,为防止 被氧化,应向溶液中加入少量
被氧化,应向溶液中加入少量(4)工业中常用高铁酸钾(
 )作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成
)作为高效、多功能的自来水处理剂,高铁酸钾与水反应时,能生成 胶体吸附杂质净水,同时还产生一种气体,该原理的离子方程式为
胶体吸附杂质净水,同时还产生一种气体,该原理的离子方程式为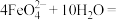
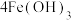 (胶体)
(胶体)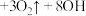 ,每生成1个
,每生成1个 ,
, 转移的电子数目为
转移的电子数目为
您最近一年使用:0次
名校
解题方法
7 . W、X、Y、Z是原子序数依次增大的短周期主族元素,X是非金属性最强的元素,Y的周期序数是其族序数的3倍,W与X同周期、与Y同主族,W的最外层电子数与Z的最外层电子数之和等于8。下列说法正确的是
| A.最高价氧化物对应水化物的碱性:W>Y |
| B.最简单气态氢化物的稳定性:X>Z |
| C.Y单质在空气中的燃烧产物只含离子键 |
| D.最简单离子半径大小关系:W<X<Y |
您最近一年使用:0次
2023-03-17更新
|
151次组卷
|
4卷引用:新疆昌吉回族自治州第二中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
8 . 下列有关化学用语表示正确的是
A. 的电子式: 的电子式: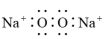 |
B.次氯酸的电子式: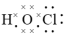 |
C.S原子结构示意图: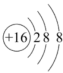 |
D.中子数为146、质子数为92的轴(U)原子: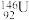 |
您最近一年使用:0次
2023-03-17更新
|
244次组卷
|
2卷引用:新疆昌吉回族自治州第二中学2022-2023学年高一上学期期末考试化学试题
9 . 下列化学用语正确的是
A.HCl的电子式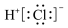 | B.质量数为37的氯原子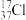 |
C.CO2的电子式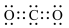 | D.Cl-的结构示意图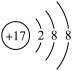 |
您最近一年使用:0次
2023-03-14更新
|
246次组卷
|
2卷引用:新疆昌吉州行知学校2022-2023学年高一上学期期末考试化学试题
名校
解题方法
10 . 元素的“价-类”二维图是我们学习元素及其化合物相关知识的重要模型和工具,它指的是以元素的化合价为纵坐标,以物质的类别为横坐标所绘制的二维平面图。下图为铁元素的“价-类”二维图,其中的箭头表示部分物质间的转化关系,下列说法正确的是
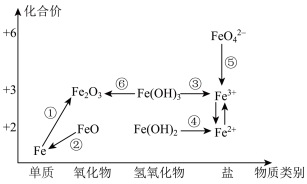

| A.在溶液中加入足量新制氯水,可实现图中Fe3+转化为Fe2+ |
| B.在溶液中滴加KSCN溶液,溶液显红色,证明原溶液中有Fe3+,无Fe2+ |
C.由图可预测:高铁酸盐(FeO )具有强氧化性 )具有强氧化性 |
| D.FeO是一种黑色粉末,只能用作还原剂 |
您最近一年使用:0次
2023-03-14更新
|
512次组卷
|
5卷引用:新疆昌吉州行知学校2022-2023学年高一上学期期末考试化学试题
新疆昌吉州行知学校2022-2023学年高一上学期期末考试化学试题上海市第四中学2022-2023学年高一下学期4月期中考试化学试题贵州省遵义市南白中学2022-2023学年高一下学期第一次联考化学试题(已下线)第3讲 铁盐及其亚铁盐(已下线)【精品卷】3.1.2 铁的重要化合物课堂例题-人教版2023-2024学年必修第一册



