名校
解题方法
1 . 十九世纪初,科学家用氰酸银(AgOCN)与NH4Cl在一定条件下反应制得尿素[CO(NH2)2]实现了由无机物到有机物的合成。下列有关说法正确的是
A.NH4Cl电子式为 | B.电负性:C<O<N |
| C.氰酸铵与尿素互为同分异构体 | D.尿素中所有原子可能处于同一平面 |
您最近半年使用:0次
名校
解题方法
2 . 铜离子可与含N、含O的微粒形成多种结构。向CuSO4溶液中滴加氨水可最终形成如图所示的配离子。___________ 。关于该微粒说法正确的是___________ 。
A.1mol该微粒中有22mol共价键
B.该微粒中的N、O原子构成了立方体结构
C.电负性N>O>H
D.该微粒中可与溶剂水分子形成氢键的只有N、O原子
(2)铜元素位于元素周期表的___________ 区。铜原子价电子排布式 为___________ 。
A.s区 B.p区 C.ds区 D.f区
(3)Cu2+无法与BF3中的B原子形成配位键的原因是___________ 。
(4)Cu2+可形成如图所示晶体。该晶胞中负离子为 CN—,“连接”着每一对相邻的Fe3+与Cu2+(部分 示例位置已用箭头标出)。___________ 个。
②已知相邻的Fe3+与Cu2+核间距为apm,则相邻的Fe3+与K+核间距为___________ pm。
③该晶体的化学式为___________ 。

A.1mol该微粒中有22mol共价键
B.该微粒中的N、O原子构成了立方体结构
C.电负性N>O>H
D.该微粒中可与溶剂水分子形成氢键的只有N、O原子
(2)铜元素位于元素周期表的
A.s区 B.p区 C.ds区 D.f区
(3)Cu2+无法与BF3中的B原子形成配位键的原因是
(4)Cu2+可形成如图所示晶体。该晶胞中

②已知相邻的Fe3+与Cu2+核间距为apm,则相邻的Fe3+与K+核间距为
③该晶体的化学式为
您最近半年使用:0次
名校
解题方法
3 . 反应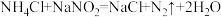 应用于石油开采。下列说法正确的是
应用于石油开采。下列说法正确的是
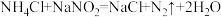 应用于石油开采。下列说法正确的是
应用于石油开采。下列说法正确的是A. 的电子式为 的电子式为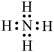 | B. 中 中 元素的化合价为+5 元素的化合价为+5 |
C.N2分子中存在 键 键 | D.H2O分子结构呈直线型 |
您最近半年使用:0次
名校
解题方法
4 . 硼和氮的化合物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态N原子电子自旋量子数和为___________ ,其价电子中成对电子数与未成对电子数之比是___________ 。
(2)硼烷-吡啶(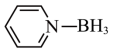 )是一种中等强度的还原性试剂,在质子性溶剂中,它的稳定性和溶解性均优于硼氢化钠(NaBH4),则硼氢化钠晶体类型是
)是一种中等强度的还原性试剂,在质子性溶剂中,它的稳定性和溶解性均优于硼氢化钠(NaBH4),则硼氢化钠晶体类型是___________ 。硼烷-吡啶组成元素属于第二周期的电负性从大到小的顺序是___________ 。
(3)吡啶(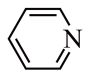 )和吡咯(
)和吡咯(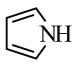 )均含有大
)均含有大 健,相同条件下,熔点吡啶
健,相同条件下,熔点吡啶___________ 吡咯(填“大于”或“小于”),其原因是___________ 。
(4)Ca与B组成的金属硼化物结构如图所示,硼原子全部组成B6正八面体,各个顶点通过B-B键互相连接成三维骨架,具有立方晶系的对称性。该晶体的化学式为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如M点原子的分数坐标为( ,
, ,
, ),已知B6八面体中B -B键的键长为r pm,晶胞参数为a pm,则N点原子的分数坐标为
),已知B6八面体中B -B键的键长为r pm,晶胞参数为a pm,则N点原子的分数坐标为 ___________ ,Ca与 B 原子间的最短距离d=___________ pm(列出计算式即可)。
(1)基态N原子电子自旋量子数和为
(2)硼烷-吡啶(
 )是一种中等强度的还原性试剂,在质子性溶剂中,它的稳定性和溶解性均优于硼氢化钠(NaBH4),则硼氢化钠晶体类型是
)是一种中等强度的还原性试剂,在质子性溶剂中,它的稳定性和溶解性均优于硼氢化钠(NaBH4),则硼氢化钠晶体类型是(3)吡啶(
 )和吡咯(
)和吡咯( )均含有大
)均含有大 健,相同条件下,熔点吡啶
健,相同条件下,熔点吡啶(4)Ca与B组成的金属硼化物结构如图所示,硼原子全部组成B6正八面体,各个顶点通过B-B键互相连接成三维骨架,具有立方晶系的对称性。该晶体的化学式为
 ,
, ,
, ),已知B6八面体中B -B键的键长为r pm,晶胞参数为a pm,则N点原子的分数坐标为
),已知B6八面体中B -B键的键长为r pm,晶胞参数为a pm,则N点原子的分数坐标为 
您最近半年使用:0次
名校
5 . 某种新型储氢材料(摩尔质量为188g∙mol–1)的立方晶胞如图,该晶胞可储存6个氢原子。已知M核内中子数比质子数多4,标准状况下氢气的密度为ρg∙cm–3,NA表示阿伏加德罗常数的值。下列说法正确的是

| A.晶胞中[M(NH3)6]n+和[BH4]–的配位数相同 |
| B.M离子最外层电子排布式为3d64s2 |
C.在晶胞体对角线的一维空间上会出现 的排布规律 的排布规律 |
D.该材料的储氢能力[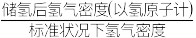 ]为 ]为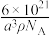 |
您最近半年使用:0次
名校
6 . 下列关于物质的结构或性质及解释都正确的是
| 选项 | 物质的结构或性质 | 解释 |
| A | 第一电离能:Zn>Cu | 元素金属性:Zn大于Cu |
| B | 熔点:SiO2>CO2 | 相对分子质量:SiO2大于CO2 |
| C | O2与O3分子极性相同 | 二者都是由非极性键构成的非极性分子 |
| D | 沸点:对羟基苯甲醛>邻羟基苯甲醛 | 对羟基苯甲醛形成分子间氢键,邻羟基苯甲醛形成分子内氢键 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
7 . 设NA为阿伏加德罗常数的值。下列说法不正确的是
| A.46g乙醇(CH3CH2OH)中sp3杂化的原子数为2NA |
| B.质量为12g的金刚石晶体中,C-C键数目为2NA |
C.62g白磷(P4)所含 键的数目为3NA 键的数目为3NA |
| D.20g D2O中含有的价电子数目为8NA |
您最近半年使用:0次
名校
8 . 下列有关化学用语正确的是
A.15N的原子结构示意图: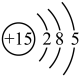 |
B.NaOH的电子式: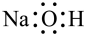 |
C.基态Cr原子的价层电子轨道表示式: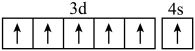 |
D.NH3分子的VSER模型: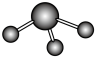 |
您最近半年使用:0次
名校
解题方法
9 . 比亚迪宣布推出基于磷酸铁锂技术的“刀片电池”,刀片电池能量密度大,安全性高。电池的正极活性材料是 。请回答下列问题
。请回答下列问题
(1)铁元素位于周期表第四周期第________ 族;基态 的最外层电子排布式为
的最外层电子排布式为________ 。
(2)正极材料 的阴离子
的阴离子 的空间结构为
的空间结构为________ 。
(3)Fe原子或离子外围有较多能量相近的空轨道,能与SCN、 、
、 等形成配合物。
等形成配合物。 与
与 形成配位键时,提供孤电子对的原子是
形成配位键时,提供孤电子对的原子是________ ,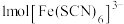 的σ键数目为
的σ键数目为________  。
。
 。请回答下列问题
。请回答下列问题(1)铁元素位于周期表第四周期第
 的最外层电子排布式为
的最外层电子排布式为(2)正极材料
 的阴离子
的阴离子 的空间结构为
的空间结构为(3)Fe原子或离子外围有较多能量相近的空轨道,能与SCN、
 、
、 等形成配合物。
等形成配合物。 与
与 形成配位键时,提供孤电子对的原子是
形成配位键时,提供孤电子对的原子是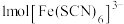 的σ键数目为
的σ键数目为 。
。
您最近半年使用:0次
今日更新
|
12次组卷
|
2卷引用:辽宁省鞍山市2023-2024学年高二下学期4月月考化学试题
名校
解题方法
10 . 钼(Mo)及其化合物广泛地应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以NiS和 形式存在,从镍钼矿中分离钼,并得到
形式存在,从镍钼矿中分离钼,并得到 的一种工艺流程如下:
的一种工艺流程如下:
(1) 元素的基态原子核外电子排布式为
元素的基态原子核外电子排布式为_______ 。
(2)“焙烧”中生成 的化学方程式为
的化学方程式为_______ 。
(3) 实验用量与理论用量的比值为1.0、1.1、1.2、1.3时,
实验用量与理论用量的比值为1.0、1.1、1.2、1.3时, 的浸出率和
的浸出率和 残留浓度的变化如图所示,则
残留浓度的变化如图所示,则 的最佳用量比为
的最佳用量比为_______ ,结合图1中信息说明理由:_______ 。 、
、 的溶解度曲线如图所示,为充分分离
的溶解度曲线如图所示,为充分分离 ,工艺流程中的“操作X”应为
,工艺流程中的“操作X”应为_______ (填标号)。
(5)锂化二硫化钼纳米片可用于高性能锂硫电池,其工作原理为: ,放电时负极的电极反应式为
,放电时负极的电极反应式为_______ 。
 形式存在,从镍钼矿中分离钼,并得到
形式存在,从镍钼矿中分离钼,并得到 的一种工艺流程如下:
的一种工艺流程如下: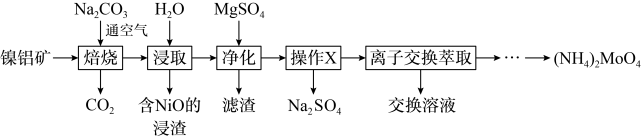
(1)
 元素的基态原子核外电子排布式为
元素的基态原子核外电子排布式为(2)“焙烧”中生成
 的化学方程式为
的化学方程式为(3)
 实验用量与理论用量的比值为1.0、1.1、1.2、1.3时,
实验用量与理论用量的比值为1.0、1.1、1.2、1.3时, 的浸出率和
的浸出率和 残留浓度的变化如图所示,则
残留浓度的变化如图所示,则 的最佳用量比为
的最佳用量比为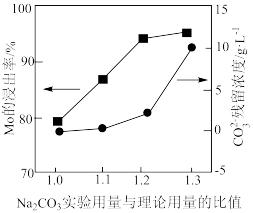
 、
、 的溶解度曲线如图所示,为充分分离
的溶解度曲线如图所示,为充分分离 ,工艺流程中的“操作X”应为
,工艺流程中的“操作X”应为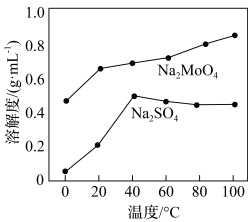
(5)锂化二硫化钼纳米片可用于高性能锂硫电池,其工作原理为:
 ,放电时负极的电极反应式为
,放电时负极的电极反应式为
您最近半年使用:0次



