2022·浙江·高考真题
1 . 亚硝酸钠俗称“工业盐”,其外观、口感与食盐相似,人若误服会中毒。现将适量某样品(成分为亚硝酸钠或氯化钠)溶于水配成溶液,分别取少量该溶液于试管中进行实验。下列方案设计、现象和结论都正确的是
| 方案设计 | 现象和结论 | |
| A | 先加入少量 溶液,再加 溶液,再加 溶液和足量稀硝酸,振荡 溶液和足量稀硝酸,振荡 | 若产生白色沉淀,则样品为亚硝酸钠 |
| B | 加到少量 溶液中,再加硫酸酸化,振荡 溶液中,再加硫酸酸化,振荡 | 若溶液褪色,则样品为亚硝酸钠 |
| C | 先加到少量 溶液中,再加入稀盐酸酸化,振荡 溶液中,再加入稀盐酸酸化,振荡 | 若溶液变黄色,则样品为亚硝酸钠 |
| D | 先加入少量 溶液,再加入 溶液,再加入 溶液和稀硝酸,振荡 溶液和稀硝酸,振荡 | 若产生白色沉淀,则样品为亚硝酸钠 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-06-14更新
|
11165次组卷
|
30卷引用:考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)
(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第14讲 氮及其化合物(练)-2023年高考化学一轮复习讲练测(全国通用)河南省南阳一中2022-2023学年高三上学期第一次阶段性考试化学试题内蒙古包头市2022-2023学年高三上学期开学调研考试化学试题(已下线)第27讲 物质的制备与性质实验(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题43 常见物质的分离、提纯和鉴别-备战2023年高考化学考点微专题(全国版)黑龙江省哈尔滨市尚志中学2022-2023学年高三上学期第二次月考化学试题天津市第一中学2022-2023学年高三上学期第一次月考化学试题(已下线)易错点10 硫元素及其化合物-备战2023年高考化学考试易错题北京清华附中2022-2023学年高三上学期10月统练(三)化学试题(已下线)易错点11 氮元素及其化合物-备战2023年高考化学考试易错题天津市河东区2022-2023学年高三上学期期中检测化学试题(已下线)热点情景汇编-专题四 元素及其化合物突破超重点 牢固掌握实验重点 超重点4 物质检验与鉴别的方法(已下线)专题10 常见非金属元素的性质及应用-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题23 化学实验基础性选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题14 化学实验方案的设计与评价(已下线)专题14 化学实验方案的设计与评价(已下线)考点03 离子共存、离子的检验与推断(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点巩固卷12 化学实验基础(一)(3大考点67题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)宁夏银川市第二中学2023-2024学年高三上学期统练四 化学试题(已下线)第3讲 物质制备实验的设计与评价2022年6月浙江省普通高校招生选考化学试题(已下线)2022年浙江省6月高考真题变式题21-25吉林省延边第二中学2022-2023学年高三上学期开学调研考试化学试题山东省枣庄市第三中学2022-2023学年高三上学期开学考试化学试题江苏省华罗庚中学2023-2024学年高三夏令营学习能力测试化学试题
2021·山东·高考真题
真题
名校
2 . 工业上以SO2和纯碱为原料制备无水NaHSO3的主要流程如图,下列说法错误的是
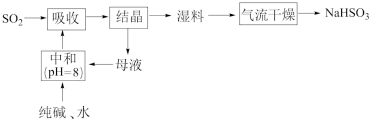
| A.吸收过程中有气体生成 | B.结晶后母液中含有NaHCO3 |
| C.气流干燥湿料时温度不宜过高 | D.中和后溶液中含Na2SO3和NaHCO3 |
您最近一年使用:0次
2021-06-29更新
|
13398次组卷
|
39卷引用:课时22 硫及其化合物-2022年高考化学一轮复习小题多维练(全国通用)
(已下线)课时22 硫及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题12 硫及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练(已下线)第四单元 非金属及其化合物(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)安徽省合肥市第一中学2021-2022学年高三上学期10月月考化学试题内蒙古北京八中乌兰察布分校2021-2022学年高三上学期学科素养评估一化学试题(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)卷09 物质的分离、提纯-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)卷05 工艺流程型选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)卷05 小题仿真卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)押新高考卷03题 元素化合物的性质-备战2022年高考化学临考题号押题(新高考通版)上海市奉贤区2022届高三下学期等级考二模化学试题(已下线)微专题21 二氧化硫性质四重性探究-备战2023年高考化学一轮复习考点微专题(已下线)第13讲 硫及其化合物(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第12练 硫及其化合物-2023年高考化学一轮复习小题多维练(全国通用)(已下线)微专题30 非金属及其化合物制备流程与实验探究(S、Se、Te、Cl、Br、I)-备战2023年高考化学一轮复习考点微专题新疆乌鲁木齐市第八中学2022-2023学年高三上学期第一次月考化学试题(已下线)易错点34 化学实验方案的设计与评价-备战2023年高考化学考试易错题江苏省扬州市广陵区名校2022-2023学年高一上学期12月月考化学试题(已下线)专题14 工艺流程选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)第四章 非金属及其化合物 第20讲 硫及其氧化物(已下线)上海市静安区2022-2023学年高三下学期二模变式题(选择题11-15)(已下线)专题10 物质的反应及转化(已下线)专题10 物质的反应及转化(已下线)考点10 硫及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第3讲 硫及其重要化合物(已下线)专题07 无机物的转化 微型工艺流程-2023年高考化学真题题源解密(全国通用)四川省宜宾市叙州区第一中学校2022-2023学年高一下学期6月期末考试化学试题北京市中国人民大学附属中学2023-2024学年高三上学期11月统练三 化学试题天津市第一中学2023-2024学年高二上学期11月期中考试化学试题河南省信阳高级中学2023-2024学年高三上学期1月月考理综试题-高中化学2021年新高考山东化学高考真题江西省赣县第三中学2021-2022学年高二上学期入学考试化学试题(已下线)专题12 工艺流程选择题-备战2022年高考化学真题及地市好题专项集训【山东专用】2021年山东高考化学试题变式题1-10(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)山东省济宁市邹城市孟子湖中学2021-2022学年高三下学期开学考试化学试题新疆石河子第一中学2023-2024学年高三上学期第三次月考化学试题山东省潍坊市昌乐二中2023-2024学年高三上学期第一次月考化学试题江苏省常州市田家炳2高级中学023-2024学年高一上学期12月阶段性调研化学学科试卷
3 . 下列由实验现象所得结论错误的是
A.向NaHSO3溶液中滴加氢硫酸,产生淡黄色沉淀,证明HSO 具有氧化性 具有氧化性 |
| B.向酸性KMnO4溶液中加入Fe3O4粉末,紫色褪去,证明Fe3O4中含Fe(Ⅱ) |
| C.向浓HNO3中插入红热的炭,产生红棕色气体,证明炭可与浓HNO3反应生成NO2 |
| D.向NaClO溶液中滴加酚酞试剂,先变红后褪色,证明NaClO在溶液中发生了水解反应 |
您最近一年使用:0次
2021-06-29更新
|
9678次组卷
|
21卷引用:山东省临沂市兰山区2020-2021学年高一下学期期末考试化学试题
山东省临沂市兰山区2020-2021学年高一下学期期末考试化学试题(已下线)课时23 氮及其化合物-2022年高考化学一轮复习小题多维练(全国通用)内蒙古北京八中乌兰察布分校2021-2022学年高三上学期学科素养评估一化学试题(已下线)专题07 非金属及其化合物-2022年高考化学二轮复习重点专题常考点突破练(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)秘籍05 微型实验方案设计与评价-备战2022年高考化学抢分秘籍(全国通用)(已下线)押新高考卷05题 化学实验基础-备战2022年高考化学临考题号押题(新高考通版)天津市第一中学2021-2022学年高三下学期4月月考化学试题山东省威海乳山市银滩高级中学2022-2023学年高三9月月考化学试题新疆乌鲁木齐市第八中学2022-2023学年高三上学期第一次月考化学试题河北省石家庄市第十五中学2022-2023学年高三上学期阶段性考试化学试题(已下线)专题24 实验分析设计型选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型182 综合实验突破(已下线)专题07 无机物的转化 微型工艺流程-2023年高考化学真题题源解密(全国通用)河北省唐山市第一中学2022-2023学年高三上学期11月期中考试化学试题2021年新高考山东化学高考真题吉林省松原市实验高级中学2020-2021学年高一下学期期末考试化学试题(已下线)专题05 元素及其化合物-备战2022年高考化学真题及地市好题专项集训【山东专用】2021年山东高考化学试题变式题1-10(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)山东省济宁市邹城市孟子湖中学2021-2022学年高三下学期开学考试化学试题
4 . 为探究Na2SO3的性质,实验小组同学进行了如下实验:

| A.③和④中产生的气体成分完全相同 | B.②和⑥中沉淀的主要成分不同 |
| C.①→②和④→⑥均只发生了复分解反应 | D. 的还原性在酸性条件下增强 的还原性在酸性条件下增强 |
您最近一年使用:0次
2023-04-06更新
|
2546次组卷
|
11卷引用:北京市海淀区2022-2023学年高三下学期期中练习化学试题
北京市海淀区2022-2023学年高三下学期期中练习化学试题浙江省杭州第四中学2022-2023学年高一下学期期中考试化学试题(已下线)【2023】【高一下】【期中考】【杭四下沙】【高中化学】【罗梦宇收集】(已下线)题型35 微型成套装置实验流程(已下线)题型45 物质性质探究型综合实验山西省晋城一中2022-2023学年高一下学期第三次调研考试化学试题天津市滨海新区2023-2024学年塘沽第一中学高三上学期第二次月考化学试题(已下线)热点19 化学微型实验北京一零一中2023-2024学年高三上学期第一次月考(开学考)化学试卷 北京市顺义区第二中学2023-2024学年高三下学期开学测化学试题山东省东营市第一中学2023届高三下学期二模化学试题
2023·上海·模拟预测
5 . 向饱和氯水中加入少量 亚硫酸钠固体,下列说法正确的是
亚硫酸钠固体,下列说法正确的是
 亚硫酸钠固体,下列说法正确的是
亚硫酸钠固体,下列说法正确的是| A.溶液pH减小 | B.溶液颜色变深 | C.漂白性增强 | D.导电性减弱 |
您最近一年使用:0次
6 . 某小组进行如下实验:向0.1mol·L-1 FeCl3溶液中通入SO2或加入Na2SO3溶液,均得到红色溶液。
已知:溶液中+4价含硫微粒物质的量分数随pH变化的曲线如下图所示。
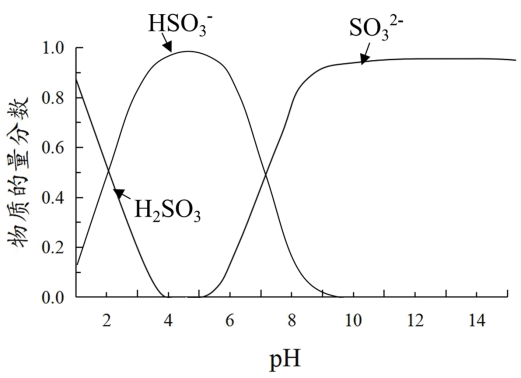
I.推测Fe3+与溶液中的某种+4价含硫微粒形成了红色的配离子。设计如下实验(均在常温下进行):
(1)将上述实验补充完整________ 。
(2)配离子的配体为 的实验证据是
的实验证据是_______ 。
II.探究pH对FeCl3和Na2SO3反应的影响。设计如下实验:
(3)探究实验b中溶液褪色更快的原因:
i.甲认为pH降低,有利于Fe3+氧化 ,导致实验b中溶液褪色更快。
,导致实验b中溶液褪色更快。
①从电极反应的角度,进行理论分析:
还原反应为:Fe3++e-=Fe2+氧化反应为:_______ 。
②已知上述实验条件下pH对Fe3+的氧化性几乎没有影响。从平衡移动的角度判断pH对 还原性的影响是
还原性的影响是_______ (填“增强”或“减弱”)。
③通过理论分析,甲认为其猜测_______ (填“成立”或“不成立”),并进一步实验,获得了证据。实验方案为:反应相同时间,分别取实验a和b中的溶液,检测_______ 浓度(填离子符号),比较其大小关系。
ii.乙猜测pH降低,有利于_______氧化 ,导致实验b中溶液褪色更快。
,导致实验b中溶液褪色更快。
④将乙的假设补充完整_______ (填化学式)。
⑤乙设计实验进行验证:
取10mL 0.1mol·L-1 Na2SO3溶液加硫酸调pH=1.7,用KMnO4溶液滴定,消耗体积为V1。另取一份相同的溶液放置10分钟后,再用KMnO4溶液滴定,消耗体积为V2.前后差值(V1-V2)为ΔVa。用同样的方法对10mL 0.1mol·L-1 Na2SO3(含H2SO4)pH=1.3进行滴定,消耗KMnO4溶液前后体积差值为ΔVb。
经对比可知,ΔVa>△Vb,由此得出的实验结论是_______ 。
(4)综合上述分析,pH降低,有利于_______ 反应的发生,导致实验b中溶液褪色更快。
已知:溶液中+4价含硫微粒物质的量分数随pH变化的曲线如下图所示。

I.推测Fe3+与溶液中的某种+4价含硫微粒形成了红色的配离子。设计如下实验(均在常温下进行):
| 实验 | 溶液1(1mL) | 溶液2(10mL) | 现象 |
| A | 0.1mol·L-1 FeCl3溶液 | SO2的饱和溶液 | 溶液1与溶液2混合后,实验A、B、C所得溶液红色依次加深 |
| B | 0.1mol·L-1 FeCl3溶液 | SO2的饱和溶液,用NaOH固体调 pH=5.0 | |
| C | 0.1mol·L-1 FeCl3溶液 | _______ |
(2)配离子的配体为
 的实验证据是
的实验证据是II.探究pH对FeCl3和Na2SO3反应的影响。设计如下实验:
| 序号 | 实验a | 实验b |
| 方案 | 5mL酸化的0.1mol·L-1 FeCl3与2mL 0.1mol·L-1 Na2SO3混合得红色溶液,测得pH=1.7 | 5mL酸化的0.1mol·L-1 FeCl3与2mL 0.1mol·L-1 Na2SO3混合得红色溶液,加几滴浓盐酸,调pH=1.3 |
| 现象 | 放置10分钟后,溶液红色均褪去,实验b中溶液褪色更快。经检验,褪色后的溶液中均存在Fe2+。 | |
i.甲认为pH降低,有利于Fe3+氧化
 ,导致实验b中溶液褪色更快。
,导致实验b中溶液褪色更快。①从电极反应的角度,进行理论分析:
还原反应为:Fe3++e-=Fe2+氧化反应为:
②已知上述实验条件下pH对Fe3+的氧化性几乎没有影响。从平衡移动的角度判断pH对
 还原性的影响是
还原性的影响是③通过理论分析,甲认为其猜测
ii.乙猜测pH降低,有利于_______氧化
 ,导致实验b中溶液褪色更快。
,导致实验b中溶液褪色更快。④将乙的假设补充完整
⑤乙设计实验进行验证:
取10mL 0.1mol·L-1 Na2SO3溶液加硫酸调pH=1.7,用KMnO4溶液滴定,消耗体积为V1。另取一份相同的溶液放置10分钟后,再用KMnO4溶液滴定,消耗体积为V2.前后差值(V1-V2)为ΔVa。用同样的方法对10mL 0.1mol·L-1 Na2SO3(含H2SO4)pH=1.3进行滴定,消耗KMnO4溶液前后体积差值为ΔVb。
经对比可知,ΔVa>△Vb,由此得出的实验结论是
(4)综合上述分析,pH降低,有利于
您最近一年使用:0次
2022-04-29更新
|
1792次组卷
|
6卷引用:北京市丰台区2022届高三二模化学试题
北京市丰台区2022届高三二模化学试题(已下线)化学-2022年高考押题预测卷03(北京卷)(已下线)专项14 化学实验综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)北京市顺义区第一中学2022届高三下学期三模化学试题湖北省华中师范大学第一附属中学2022-2023学年高一上学期竞赛生10月测试化学试题天天练6-10
解题方法
7 . 科研人员提出了雾霾微粒中硫酸盐生成的三个阶段的转化机理,其主要过程示意图如图。下列说法错误的是
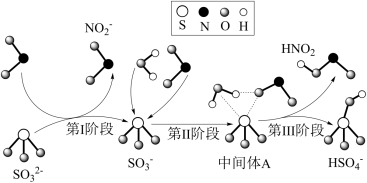

A.氧化性:NO2>SO ,还原性:SO ,还原性:SO >HNO2 >HNO2 |
B.第II、III阶段总的化学方程式为:SO +H2O+NO2=HNO2+HSO +H2O+NO2=HNO2+HSO |
| C.NO2在所有过程中都是被还原 |
| D.上述反应过程中,S的成键数目保持不变 |
您最近一年使用:0次
2022-11-20更新
|
1298次组卷
|
3卷引用:山西省吕梁市2022-2023学年高三上学期阶段性测试化学试题
山西省吕梁市2022-2023学年高三上学期阶段性测试化学试题(已下线)专题04 氧化还原反应及其应用 (测)-2023年高考化学二轮复习讲练测(新高考专用)山东日照市莒县一中2022-2023学年高一下学期3月月考化学试题
8 . 向2mL0.2mol/LCuSO4溶液中滴加0.2mol/LNa2SO3溶液时溶液变绿,继续滴加产生棕黄色沉淀,经检验棕黄色沉淀中不含 。通过实验探究棕黄色沉淀的成分。
。通过实验探究棕黄色沉淀的成分。
实验1:向棕黄色沉淀中加入稀硫酸,观察到溶液变蓝,产生红色固体
实验2: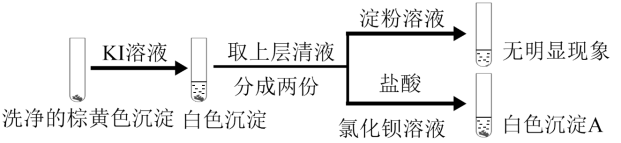
已知: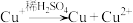 ,
,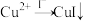 (白色)
(白色)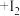 。
。
下列同学对实验现象的分析正确的是
 。通过实验探究棕黄色沉淀的成分。
。通过实验探究棕黄色沉淀的成分。实验1:向棕黄色沉淀中加入稀硫酸,观察到溶液变蓝,产生红色固体
实验2:

已知:
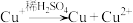 ,
,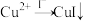 (白色)
(白色)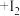 。
。下列同学对实验现象的分析正确的是
A.实验1中加入稀 后溶液变蓝可证实棕黄色沉淀中含有 后溶液变蓝可证实棕黄色沉淀中含有 |
B.实验2中加入KI溶液后产生白色沉淀,可证实棕黄色沉淀中含有 |
C.实验2中加入淀粉溶液后无明显现象,说明不存在 |
D.在 的存在下, 的存在下, 与 与 发生了氧化还原反应,产生CuI沉淀和 发生了氧化还原反应,产生CuI沉淀和 ,说明棕黄色沉淀中含有 ,说明棕黄色沉淀中含有 和 和 |
您最近一年使用:0次
2022-05-28更新
|
1292次组卷
|
11卷引用:北京市中国人民大学附属中学2022届高三下学期第三次适应性练习化学试题
北京市中国人民大学附属中学2022届高三下学期第三次适应性练习化学试题(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点16 铜及其金属材料-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第13讲 硫及其化合物(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题三 金属及其化合物 能力提升检测卷(测)-2023年高考化学一轮复习讲练测(新教材新高考)北京首都师范大学附属中学2023届高三3月月考化学试题(已下线)考点10 硫及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点16 铜及其金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)四川省泸州市合江县马街中学校2022-2023学年高一下学期4月期中考试化学试题辽宁省实验中学2023-2024学年高三上学期阶段测试化学试题浙江省舟山市舟山中学2021-2022学年高三上学期开学考试化学试题
2021·湖北·模拟预测
解题方法
9 . 不能正确表示下列反应的离子方程式是
A.将少量溴水滴入过量 溶液中: 溶液中: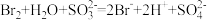 |
B.将足量 溶液滴入 溶液滴入 浊液中: 浊液中: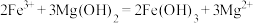 |
C.将过量 通入 通入 溶液中: 溶液中: |
D.将葡萄糖溶液与足量银氨溶液共热: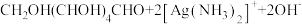  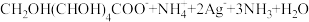 |
您最近一年使用:0次
2021-01-25更新
|
2279次组卷
|
6卷引用:专题04 离子反应-2022年高考化学二轮复习重点专题常考点突破练
(已下线)专题04 离子反应-2022年高考化学二轮复习重点专题常考点突破练(已下线)微专题 与量有关的离子方程式的书写湖北省2021年普通高中学业水平选择考适应性测试化学试题广东省江门市2021-2022学年高三下学期一模考试化学试题(已下线)押广东卷化学第15题 离子方程式正误判断-备战2022年高考化学临考题号押题(广东卷)(已下线)专题14 离子方程式正误判断-备战2023年高考化学母题题源解密(广东卷)
10 . 铂钌催化剂是甲醇燃料电池的阳极催化剂。一种以钌矿石[主要含Ru(CO3)2,还含少量的FeO、MgO、RuO4、CaO、SiO2]为原料制备钌(Ru)的流程如图。回答下列问题:
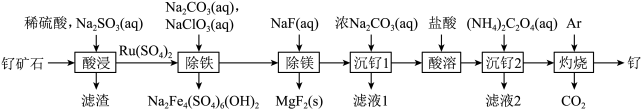
(1)Na2Fe4(SO4)6(OH)2中Fe的化合价为____ 。
(2)“酸浸”时,Na2SO3的作用____ 。“滤渣”的主要成分有SiO2和____ (填化学式)。“酸浸”中钌的浸出率与浸出温度、pH的关系如图所示,“酸浸”的最佳条件是____ 。
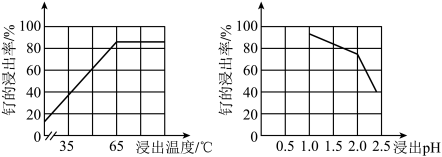
(3)“除铁”的离子方程式为____ 。(提示:1molNaClO3参与反应,转移6mol电子)
(4)从“滤液2”中可提取一种化肥,其电子式为____ 。
(5)“灼烧”时Ar的作用是____ 。
(6)某工厂用10t钌矿石[含8.84tRu(CO3)2、165kgRuO4],最终制得3636kgRu,则Ru的产率为____ 。(保留三位有效数字)

(1)Na2Fe4(SO4)6(OH)2中Fe的化合价为
(2)“酸浸”时,Na2SO3的作用

(3)“除铁”的离子方程式为
(4)从“滤液2”中可提取一种化肥,其电子式为
(5)“灼烧”时Ar的作用是
(6)某工厂用10t钌矿石[含8.84tRu(CO3)2、165kgRuO4],最终制得3636kgRu,则Ru的产率为
您最近一年使用:0次
2022-05-10更新
|
1867次组卷
|
15卷引用:河南省新乡市2022届高三第三次模拟理科综合化学试题
河南省新乡市2022届高三第三次模拟理科综合化学试题河北省保定市2022届高三第二次模拟考试化学试题河南省名校联盟2022届高三下学期5月大联考理科综合化学试题(已下线)专题15工艺流程题-2022年高考真题+模拟题汇编(全国卷)(已下线)专题16工艺流程题-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题16工艺流程题-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题15 工艺流程题-2022年高考真题模拟题分项汇编广东省广州市海珠外国语实验中学2022-2023学年高三上学期第二次阶段性考试化学试题福建省福州第一中学2022-2023学年高三上学期检考前适应性考试化学试题(已下线)专题29 无机化工流程综合分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)考前特训 [综合大题分类规范练](已下线)专题01 工艺流程专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)四川省泸州市泸县第一中学2023-2024学年高一上学期1月期末化学试题湖南省株洲市北附高级中学2022-2023学年高三上学期第五次月考化学试题山东新高考2022-2023学年高一上学期质量测评模拟演练化学试题



