1 . 实验室制备SO2并探究其性质的方案如图,回答下列问题:
Ⅰ.制备SO2(部分固定装置略)
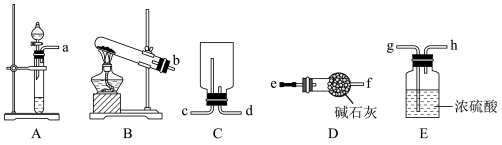
(1)制备SO2可以选择的发生装置为___ (填大写字母),其反应的化学方程式为___ 。
(2)选用图中装置制备并收集一瓶干燥的SO2,其连接顺序为:发生装置→___ (按气流方向,填小写字母)。
Ⅱ.探究SO2与Cu(OH)2悬浊液的反应
查阅资料:SO2在酸性条件下还原性较差,碱性条件下较强。
实验步骤:ⅰ.配制Cu(OH)2悬浊液:往NaOH溶液中加入CuSO4溶液可得到Cu(OH)2悬浊液。
ⅱ.将SO2通入Cu(OH)2悬浊液中(实验装置如图F)。
实验现象:F中出现少量红色固体,稍后,溶液呈绿色,与CuSO4溶液、CuCl2溶液的颜色有明显不同。

(3)配制Cu(OH)2悬浊液时,要保证___ 溶液过量。(填“NaOH”或“CuSO4”)
(4)为确定红色固体成分,进行以下实验:
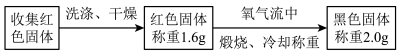
①根据上述实验可得结论:该红色固体为___ 。
②产生红色固体的原因是___ (用离子方程式表示)。
(5)为探究F中溶液呈绿色而不是蓝色的原因,实验如下:
ⅰ.向4mL1mol·L-1的CuSO4溶液中通入过量SO2,未见溶液颜色发生变化。
ⅱ.取少量F中滤液,加入少量稀盐酸,产生无色刺激性气味的气体,得到澄清的蓝色溶液。再加入BaCl2溶液,出现白色沉淀。
①实验ⅰ的目的是___ 。
②溶液显绿色的原因可能是溶液中含有较多Cu(HSO3)2。小组同学通过进一步实验确认了这种可能性,在少量1mol·L-1的CuSO4溶液中加入___ (填化学式),得到绿色溶液。
Ⅰ.制备SO2(部分固定装置略)

(1)制备SO2可以选择的发生装置为
(2)选用图中装置制备并收集一瓶干燥的SO2,其连接顺序为:发生装置→
Ⅱ.探究SO2与Cu(OH)2悬浊液的反应
查阅资料:SO2在酸性条件下还原性较差,碱性条件下较强。
实验步骤:ⅰ.配制Cu(OH)2悬浊液:往NaOH溶液中加入CuSO4溶液可得到Cu(OH)2悬浊液。
ⅱ.将SO2通入Cu(OH)2悬浊液中(实验装置如图F)。
实验现象:F中出现少量红色固体,稍后,溶液呈绿色,与CuSO4溶液、CuCl2溶液的颜色有明显不同。

(3)配制Cu(OH)2悬浊液时,要保证
(4)为确定红色固体成分,进行以下实验:

①根据上述实验可得结论:该红色固体为
②产生红色固体的原因是
(5)为探究F中溶液呈绿色而不是蓝色的原因,实验如下:
ⅰ.向4mL1mol·L-1的CuSO4溶液中通入过量SO2,未见溶液颜色发生变化。
ⅱ.取少量F中滤液,加入少量稀盐酸,产生无色刺激性气味的气体,得到澄清的蓝色溶液。再加入BaCl2溶液,出现白色沉淀。
①实验ⅰ的目的是
②溶液显绿色的原因可能是溶液中含有较多Cu(HSO3)2。小组同学通过进一步实验确认了这种可能性,在少量1mol·L-1的CuSO4溶液中加入
您最近一年使用:0次
2022-02-19更新
|
576次组卷
|
3卷引用:押广东卷化学第17题 化学实验综合题-备战2022年高考化学临考题号押题(广东卷)
(已下线)押广东卷化学第17题 化学实验综合题-备战2022年高考化学临考题号押题(广东卷)广东省梅州市2022届高三下学期第一次质检化学试题湖南省株洲市醴陵市第一中学2021-2022学年高三下学期期中考试化学试题
20-21高三上·江苏泰州·期中
解题方法
2 . 资料显示: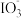 在酸性溶液中能氧化I-,反应为
在酸性溶液中能氧化I-,反应为 +5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。
+5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。
(1)甲同学对这一现象做出如下假设:t秒前生成了I2,但由于存在Na2SO3,I2被消耗,该反应的离子方程式为________ , 的还原性
的还原性________ I-(填“>”“=”或“<”)。
(2)为验证他的猜想,甲同学向反应后的蓝色溶液中加入________ ,蓝色迅速消失,随后再次变蓝。
(3)甲同学设计了如下实验,进一步研究Na2SO3溶液和KIO3溶液反应的过程。
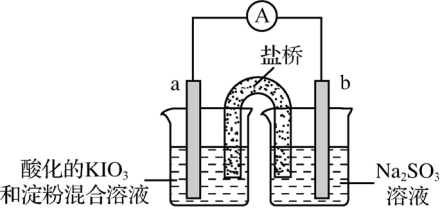
①甲同学在b电极附近的溶液中检测出了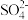
②刚开始放电时,a电极附近溶液未变蓝;取出a电极附近溶液于试管中,溶液变蓝。 在a极放电的产物是
在a极放电的产物是________ 。
③放电一段时间后,a电极附近溶液短暂出现蓝色,随即消失,重复多次后,蓝色不再褪去。电流表显示电路中时而出现电流,时而归零,最终电流消失。电流表短暂归零的原因是________ 。
④下列说法正确的是________ 。
a. a电极附近蓝色不再褪去时, 尚未完全氧化
尚未完全氧化
b. a电极附近短暂出现蓝色,随即消失的原因可能是因为I2被 还原
还原
c. 电流消失后,向b电极附近加入过量Na2SO3溶液,重新产生电流,a电极附近蓝色褪去
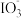 在酸性溶液中能氧化I-,反应为
在酸性溶液中能氧化I-,反应为 +5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。
+5I-+6H+=3I2+3H2O。为探究Na2SO3溶液和KIO3溶液的反应,甲同学向过量的KIO3酸性溶液中加入Na2SO3溶液,并加入两滴淀粉溶液:开始时无明显现象,t秒后溶液突然变为蓝色。(1)甲同学对这一现象做出如下假设:t秒前生成了I2,但由于存在Na2SO3,I2被消耗,该反应的离子方程式为
 的还原性
的还原性(2)为验证他的猜想,甲同学向反应后的蓝色溶液中加入
(3)甲同学设计了如下实验,进一步研究Na2SO3溶液和KIO3溶液反应的过程。

①甲同学在b电极附近的溶液中检测出了
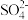
②刚开始放电时,a电极附近溶液未变蓝;取出a电极附近溶液于试管中,溶液变蓝。
 在a极放电的产物是
在a极放电的产物是③放电一段时间后,a电极附近溶液短暂出现蓝色,随即消失,重复多次后,蓝色不再褪去。电流表显示电路中时而出现电流,时而归零,最终电流消失。电流表短暂归零的原因是
④下列说法正确的是
a. a电极附近蓝色不再褪去时,
 尚未完全氧化
尚未完全氧化b. a电极附近短暂出现蓝色,随即消失的原因可能是因为I2被
 还原
还原c. 电流消失后,向b电极附近加入过量Na2SO3溶液,重新产生电流,a电极附近蓝色褪去
您最近一年使用:0次
3 . “价—类”二维图是研究物质性质的一种方法,图中a~f表示的均是含硫物质。下列说法正确的是

| A.a可用硫化亚铁与稀硝酸反应制取 |
B.可发生反应: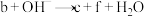 (未配平) (未配平) |
| C.c能使溴水褪色,证明c有漂白性 |
| D.f既有氧化性又有还原性 |
您最近一年使用:0次
2024-02-14更新
|
634次组卷
|
8卷引用:专题01 硫及其化合物(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
(已下线)专题01 硫及其化合物(考题猜想)(8大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)河北省承德市2023-2024学年高一上学期期末考试化学试题河北省石家庄市第二十三中学2023-2024学年高一下学期第一次月考(3月)化学试题安徽省淮南市第二中2023-2024学年高一下学期第一次月考化学试题河南省新乡市原阳县实验高级中学2023-2024学年高一下学期3月月考化学试题河南省南阳市社旗县第一高级中学2023-2024学年高一下学期4月期中考试化学试题重庆市璧山来凤中学校2023-2024学年高一下学期3月月考化学试题江苏省南宁市第三十三中学2023-2024学年高一下学期3月月考化学试题
2023·江苏·一模
名校
解题方法
4 . 硫及其化合物有着广泛的作用。硫元素具有多种化合价,在一定条件下能发生相互转化。不同温度下硫单质的状态和分子结构不同,S8环状分子的结构为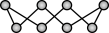 。合理应用和处理含硫的化合物,在生产生活中有重要意义。下列有关硫及其化合物的性质与用途具有对应关系的是
。合理应用和处理含硫的化合物,在生产生活中有重要意义。下列有关硫及其化合物的性质与用途具有对应关系的是
 。合理应用和处理含硫的化合物,在生产生活中有重要意义。下列有关硫及其化合物的性质与用途具有对应关系的是
。合理应用和处理含硫的化合物,在生产生活中有重要意义。下列有关硫及其化合物的性质与用途具有对应关系的是| A.硫单质呈黄色,可用作橡胶硫化剂 |
| B.SO2具有氧化性,可用于漂白草编织物 |
| C.Na2SO3具有还原性,可用于处理自来水中残留的Cl2 |
| D.浓硫酸具有强氧化性,可用作酯化反应的催化剂 |
您最近一年使用:0次
2023-03-23更新
|
687次组卷
|
4卷引用:专题05 元素化合物性质
(已下线)专题05 元素化合物性质(已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(选择题6-10)江苏省苏锡常镇四市2022-2023学年高三下学期教学情况调研(一)(3月)化学试题江苏省连云港高级中学2022-2023学年高二下学期第二次学情检测化学试题
2022·山东淄博·三模
名校
5 . 在“价一类”二维图中融入“杠杆模型”,可直观辨析部分物质转化及其定量关系。图中的字母分别代表硫及其常见化合物,相关推断不合理的是
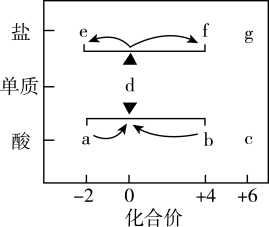

| A.b、d、f既具有氧化性又具有还原性 |
| B.硫酸型酸雨的形成过程涉及b到c的转化 |
| C.d与c在一定条件下反应可生成b或a |
D.d在加热条件下与强碱溶液反应生成e和f,且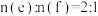 |
您最近一年使用:0次
2022-05-31更新
|
631次组卷
|
6卷引用:考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)
(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第13讲 硫及其化合物(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第4讲 浓硫酸 不同价态含硫物质的转化山东省淄博市2022届高三三模化学试题上海市金山区2022-2023学年高三第一次质量调研(一模)化学试题福建省德化第一中学2023-2024学年高三上学期第一次月考化学试题
19-20高二下·黑龙江哈尔滨·阶段练习
6 . 根据下列实验操作和现象所得到的结论错误的是( )
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向2mL0.1FeCl3的溶液中加足量铁粉,振荡,加1滴KSCN溶液,黄色逐渐消失,加KSCN溶液颜色不变 | 还原性:Fe>Fe2+ |
| B | 向久置的Na2SO3溶液中加入足量BaCl2溶液,出现白色沉淀;再加入足量稀盐酸,部分沉淀溶解 | 部分Na2SO3被氧化 |
| C | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液加入淀粉后溶液变成蓝色 | 氧化性:Cl2>I2 |
| D | 向某黄色溶液中加入淀粉KI溶液,溶液呈蓝色 | 溶液中含Br2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-07-03更新
|
274次组卷
|
3卷引用:第二单元 化学物质的变化测试题-2021年高考化学一轮复习名师精讲练
(已下线)第二单元 化学物质的变化测试题-2021年高考化学一轮复习名师精讲练黑龙江省哈尔滨市第三中学2019-2020学年高二下学期6月阶段性测试化学试题A山东省临沂市莒南第二中学2021届高三10月月考化学试题
2023·北京丰台·一模
7 . 某小组实验探究不同条件下 溶液与
溶液与 溶液的反应。
溶液的反应。
已知:
i. 在一定条件下可被还原为:
在一定条件下可被还原为: (绿色)、
(绿色)、 (无色)、
(无色)、 (棕黑色)。
(棕黑色)。
ii. 在中性、酸性溶液中不稳定,易发生歧化反应,产生棕黑色沉淀,溶液变为紫色。
在中性、酸性溶液中不稳定,易发生歧化反应,产生棕黑色沉淀,溶液变为紫色。
(1)实验I~III的操作过程中,加⼊ 溶液和物质a时,应先加
溶液和物质a时,应先加___________ 。
(2)实验I中, 的还原产物为
的还原产物为___________ 。
(3)实验II中发生反应的离子方程式为___________ 。
(4)已知:可从电极反应⻆度分析物质氧化性和还原性的变化。用电极反应式表示实验III中溶液变绿时发⽣的氧化反应___________ 。
(5)解释实验III中“⼀段时间后绿色消失,产生棕黑色沉淀”的原因___________ 。
(6)若想观察 溶液与
溶液与 溶液反应后溶液为持续稳定的绿色,设计实验方案
溶液反应后溶液为持续稳定的绿色,设计实验方案___________ 。
(7)改用0.1
 溶液重复实验I,发现紫色溶液变浅并产生棕黑沉淀,写出产生棕黑色沉淀的离子方程式
溶液重复实验I,发现紫色溶液变浅并产生棕黑沉淀,写出产生棕黑色沉淀的离子方程式___________ 。
 溶液与
溶液与 溶液的反应。
溶液的反应。已知:
i.
 在一定条件下可被还原为:
在一定条件下可被还原为: (绿色)、
(绿色)、 (无色)、
(无色)、 (棕黑色)。
(棕黑色)。ii.
 在中性、酸性溶液中不稳定,易发生歧化反应,产生棕黑色沉淀,溶液变为紫色。
在中性、酸性溶液中不稳定,易发生歧化反应,产生棕黑色沉淀,溶液变为紫色。| 实验 | 序号 | 物质a | 实验现象 |
| 4滴物质a 6滴(约0.3mL)0.1   溶液 溶液
  溶液 溶液 | I | 3  溶液 溶液 | 紫色溶液变浅至几乎无色 |
| II |  | 紫色褪去,产生棕黑色沉淀 | |
| III | 6 NaOH溶液 NaOH溶液 | 溶液变绿,⼀段时间后绿色消失,产生棕黑色沉淀 |
 溶液和物质a时,应先加
溶液和物质a时,应先加(2)实验I中,
 的还原产物为
的还原产物为(3)实验II中发生反应的离子方程式为
(4)已知:可从电极反应⻆度分析物质氧化性和还原性的变化。用电极反应式表示实验III中溶液变绿时发⽣的氧化反应
(5)解释实验III中“⼀段时间后绿色消失,产生棕黑色沉淀”的原因
(6)若想观察
 溶液与
溶液与 溶液反应后溶液为持续稳定的绿色,设计实验方案
溶液反应后溶液为持续稳定的绿色,设计实验方案(7)改用0.1

 溶液重复实验I,发现紫色溶液变浅并产生棕黑沉淀,写出产生棕黑色沉淀的离子方程式
溶液重复实验I,发现紫色溶液变浅并产生棕黑沉淀,写出产生棕黑色沉淀的离子方程式
您最近一年使用:0次
2023-03-24更新
|
493次组卷
|
3卷引用:专题21 实验探究题
2023高三·全国·专题练习
解题方法
8 . 完成下列实验设计题:
(1)证明CO2中含有CO___________
(2)证明SO2中含有CO2___________
(3)证明SO 中含有SO
中含有SO
___________
(4)①证明H2C2O4是弱酸;②证明草酸的酸性强于碳酸;③证明草酸是二元酸___________ (提供的试剂:0.1 mol·L-1 NaHCO3溶液、0.1 mol·L-1草酸溶液、0.1 mol·L-1 NaOH溶液、Na2C2O4晶体、甲基橙、酚酞、pH试纸)
(5)设计一个实验方案证明酸性条件下NaNO2具有氧化性___________ (提供的试剂:0.10 mol·L-1 NaNO2溶液、KMnO4溶液、0.10 mol·L-1 KI溶液、淀粉溶液、稀硝酸、稀硫酸)
(1)证明CO2中含有CO
(2)证明SO2中含有CO2
(3)证明SO
 中含有SO
中含有SO
(4)①证明H2C2O4是弱酸;②证明草酸的酸性强于碳酸;③证明草酸是二元酸
(5)设计一个实验方案证明酸性条件下NaNO2具有氧化性
您最近一年使用:0次
21-22高三上·江西宜春·阶段练习
名校
解题方法
9 . 连二亚硫酸钠(Na2S2O4)俗称保险粉,有强还原性,在空气中极易被氧化。用NaHSO3还原法制备保险粉的流程如下:
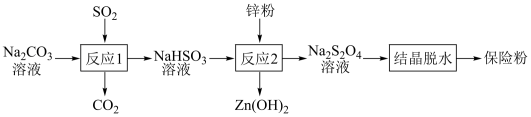
下列说法错误的是

下列说法错误的是
| A.反应1说明酸性:H2SO3>H2CO3 |
| B.反应2中消耗的氧化剂和还原剂的物质的量之比为1∶2 |
| C.反应2最好在无氧条件下进行 |
| D.反应1结束后,可用盐酸酸化的BaCl2溶液检验NaHSO3是否被氧化 |
您最近一年使用:0次
2021-11-04更新
|
803次组卷
|
5卷引用:专题40 硫的含氧酸盐-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
(已下线)专题40 硫的含氧酸盐-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)江西省奉新县第一中学2021-2022学年上学期高三第一次月考化学试题(已下线)3.2.2 硫酸 不同价态硫元素间的转化-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)陕西省安康市2022-2023学年高二上学期11月期中化学试题陕西省安康市2022-2023学年高二下学期开学摸底考试化学试题
2023·江苏·一模
解题方法
10 . 室温下,下列实验方案能得出相应结论的是
| 选项 | 方案 | 结论 |
| A | 将灼热的木炭加入到浓硝酸中,有红棕色气体产生 | 木炭在加热条件下能与浓硝酸反应 |
| B | 用pH计分别测定0.1 mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH,前者pH大于后者 | HClO酸性强于CH3COOH |
| C | 向Fe(NO3)2和KSCN的混合溶液中滴入酸化的AgNO3溶液振荡,溶液颜色变红 | 氧化性: Ag+>Fe3+ |
| D | 向Na2SO3溶液中滴入酚酞试液,溶液变红,再加入BaCl2溶液后产生白色沉淀且红色褪去 | Na2SO3溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次