名校
解题方法
1 . 下列有关实验操作、现象和结论都正确的是
| 实验操作 | 现象 | 解释或结论 | |
| A. | 向某无色溶液中通入过量的CO2气体 | 产生白色沉淀 | 该溶液中可能含有 |
| B | Cu与浓硫酸反应,冷却后,再将冷水缓慢加入盛有反应混合物的试管中 | 溶液变蓝 | 证明反应生成了Cu2+ |
| C | 向亚硫酸钠溶液中依次滴加稀盐酸和硝酸钡溶液 | 产生白色沉淀 | 亚硫酸钠溶液已变质 |
| D. | 某铁的氧化物样品用足量浓盐酸溶解后,再滴入少量酸性高锰酸钾 | 紫红色褪去 | 铁的氧化物中含+2价铁 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
2 .  在生产和生活中用途广泛。
在生产和生活中用途广泛。
Ⅰ. 溶液的配制及浓度的标定
溶液的配制及浓度的标定
(1) 溶液的配制
溶液的配制
①配制100mL一定浓度的 溶液需用到的仪器有
溶液需用到的仪器有___________ (填字母)。 溶液时,需要将
溶液时,需要将 固体溶解在浓盐酸中,原因为
固体溶解在浓盐酸中,原因为___________ 。
(2) 溶液浓度的标定
溶液浓度的标定
量取10.00mL 溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用
溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用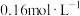
 标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗
标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗 标准溶液的体积为20.00mL,已知:
标准溶液的体积为20.00mL,已知: ,则该
,则该 溶液的浓度为
溶液的浓度为___________  。
。
Ⅱ. 与
与 反应的探究
反应的探究
(3)预测现象1:向 溶液中加入
溶液中加入 溶液,溶液由黄色变为浅绿色。作出该预测的原因为
溶液,溶液由黄色变为浅绿色。作出该预测的原因为___________ (用离子方程式表示)。
预测现象2:向 溶液中加入
溶液中加入 溶液,生成红褐色沉淀。
溶液,生成红褐色沉淀。
(4)实验验证:小组同学设计以下实验探究溶液中 浓度相同时
浓度相同时 的加入量对反应的影响,其中
的加入量对反应的影响,其中 溶液为Ⅰ中所配溶液,
溶液为Ⅰ中所配溶液, 溶液浓度为
溶液浓度为 。静置6小时观察现象,测定反应后溶液的pH,并记录数据:
。静置6小时观察现象,测定反应后溶液的pH,并记录数据:
①请补充表格中的数据:a=___________ 。
②实验ⅱ~ⅳ中,反应后溶液的pH基本不变,其原因可能是___________ 。
③实验ⅵ和ⅶ的实验现象说明溶液中 的水解与
的水解与 的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:
的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:___________ 。
④甲同学认为实验ⅵ和ⅶ中, 与
与 除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,
除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,___________ (填实验操作与现象),则说明猜想成立。
(5)请举出一种水解反应在生产或生活中的应用:___________ 。
 在生产和生活中用途广泛。
在生产和生活中用途广泛。Ⅰ.
 溶液的配制及浓度的标定
溶液的配制及浓度的标定(1)
 溶液的配制
溶液的配制①配制100mL一定浓度的
 溶液需用到的仪器有
溶液需用到的仪器有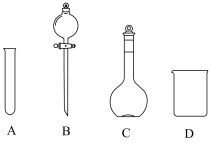
 溶液时,需要将
溶液时,需要将 固体溶解在浓盐酸中,原因为
固体溶解在浓盐酸中,原因为(2)
 溶液浓度的标定
溶液浓度的标定量取10.00mL
 溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用
溶液于碘量瓶中,加入过量KI溶液,充分反应后加入少量淀粉溶液、再用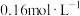
 标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗
标准溶液滴定至蓝色恰好消失,重复操作三次,平均消耗 标准溶液的体积为20.00mL,已知:
标准溶液的体积为20.00mL,已知: ,则该
,则该 溶液的浓度为
溶液的浓度为 。
。Ⅱ.
 与
与 反应的探究
反应的探究(3)预测现象1:向
 溶液中加入
溶液中加入 溶液,溶液由黄色变为浅绿色。作出该预测的原因为
溶液,溶液由黄色变为浅绿色。作出该预测的原因为预测现象2:向
 溶液中加入
溶液中加入 溶液,生成红褐色沉淀。
溶液,生成红褐色沉淀。(4)实验验证:小组同学设计以下实验探究溶液中
 浓度相同时
浓度相同时 的加入量对反应的影响,其中
的加入量对反应的影响,其中 溶液为Ⅰ中所配溶液,
溶液为Ⅰ中所配溶液, 溶液浓度为
溶液浓度为 。静置6小时观察现象,测定反应后溶液的pH,并记录数据:
。静置6小时观察现象,测定反应后溶液的pH,并记录数据:| 序号 | ⅰ | ⅱ | ⅲ | ⅳ | ⅴ | ⅵ | ⅶ |
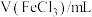 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 |
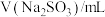 | 0 | 1.0 | 2.0 | 5.0 | a | 20.0 | 26.0 |
 | 38.0 | 37.0 | 36.0 | 33.0 | 23.0 | 18.0 | 12.0 |
| 现象 | 溶液接近无色透明 | 出现褐色沉淀 | |||||
| pH | 1.7 | 1.7 | 1.7 | 1.8 | 2.8 | 5.4 | 6.2 |
②实验ⅱ~ⅳ中,反应后溶液的pH基本不变,其原因可能是
③实验ⅵ和ⅶ的实验现象说明溶液中
 的水解与
的水解与 的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:
的水解相互促进(即发生了双水解反应),请写出反应的化学方程式:④甲同学认为实验ⅵ和ⅶ中,
 与
与 除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,
除发生双水解反应外,还发生了氧化还原反应。请设计实验证明猜想:分别取实验ⅵ和ⅶ中上层清液于两支试管中,(5)请举出一种水解反应在生产或生活中的应用:
您最近半年使用:0次
名校
3 . N-Zn/TiO2光催化氧化可用于工业上含硫废液的处理,光生电子(e-)与水电离出的H+、O2作用生成过羟基自由基(HO2·),空穴(h+)与水电离出的OH-作用生成羟基自由基(·OH),HO2·和·OH分别与 反应生成
反应生成 ,变化过程如下图所示。下列说法错误的是
,变化过程如下图所示。下列说法错误的是
 反应生成
反应生成 ,变化过程如下图所示。下列说法错误的是
,变化过程如下图所示。下列说法错误的是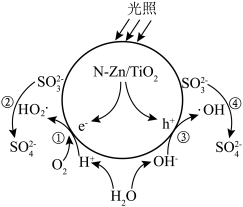
A.·OH氧化 的反应为 的反应为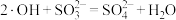 |
B.①②过程和③④过程产生的 之比为1:1 之比为1:1 |
| C.pH过低或过高均会影响催化剂的催化效果 |
D.氧化含硫废液的总反应为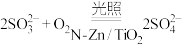 |
您最近半年使用:0次
7日内更新
|
132次组卷
|
2卷引用:东北三省四城市联考暨沈阳市高三下学期质量监测(二)化学试题
2024高三下·全国·专题练习
解题方法
4 . 纯ClO2遇热易发生分解,工业上通常制成NaClO2固体以便运输和储存。制备NaClO2的实验装置如图所示(夹持装置省略),其中A装置制备ClO2,C装置用于制备NaClO2。回答下列问题:_______ 。
(2)装置A中发生反应的离子方程式为_______ 。向装置A中通入空气的目的是_______ 。
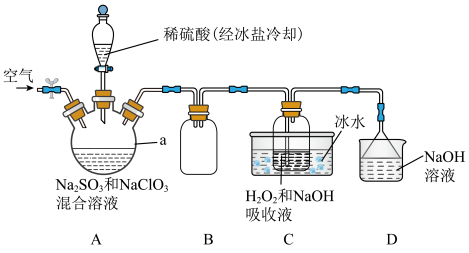
(2)装置A中发生反应的离子方程式为
您最近半年使用:0次
名校
解题方法
5 . 根据下列实验操作及现象所得结论正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 向少量酸性 溶液中滴入 溶液中滴入 溶液,溶液褪色 溶液,溶液褪色 | +4价硫具有还原性 |
| B | 将红色鲜花置于盛有干燥 的集气瓶中,鲜花褪色 的集气瓶中,鲜花褪色 |  具有漂白性 具有漂白性 |
| C | 将集满 的试管倒置于水中,水柱上升,但不能充满试管 的试管倒置于水中,水柱上升,但不能充满试管 |  微溶于水 微溶于水 |
| D | 在水玻璃中滴加稀盐酸,出现白色胶状浑浊 | 非金属性: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
6 . CuCl是一种难溶于水和乙醇的白色固体,可溶于浓盐酸或者浓氨水(形成络合物),易被氧化为高价绿色铜盐,见光受热易分解。在催化领域广泛应用,纺织工业中常作脱色剂,可利用如图装置(夹持装置略去)将SO2通入新制氢氧化铜悬浊液中制备CuCl。
①向C中先加入10.00mL0.5mol•L-1CuCl2溶液,再加入30mL0.6mol•L-1NaOH溶液;
②取下A中分液漏斗上的玻璃塞,然后打开分液漏斗的活塞,产生SO2气体至过量,直至C中出现较多的白色沉淀,上层是淡绿色的溶液;
③将C中混合物过滤,依次用水和乙醇洗涤低温晾干,精确称量所得固体质量为0.398g。
回答下列问题:
(1)针对步骤2中的现象查阅资料得知:
i.白色沉淀为CuCl;
ii.上层淡绿色溶液中的主要溶质为NaCl和少量Cu(HSO3)2。
结论:本实验中较多量的新制氢氧化铜与二氧化硫发生了氧化还原反应,少量与之发生了复分解反应,二者为竞争关系。检验淡绿色溶液中含有 的操作方法是
的操作方法是_______ 。
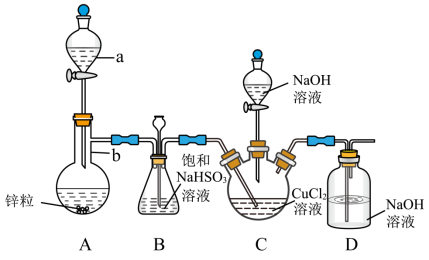
①向C中先加入10.00mL0.5mol•L-1CuCl2溶液,再加入30mL0.6mol•L-1NaOH溶液;
②取下A中分液漏斗上的玻璃塞,然后打开分液漏斗的活塞,产生SO2气体至过量,直至C中出现较多的白色沉淀,上层是淡绿色的溶液;
③将C中混合物过滤,依次用水和乙醇洗涤低温晾干,精确称量所得固体质量为0.398g。
回答下列问题:
(1)针对步骤2中的现象查阅资料得知:
i.白色沉淀为CuCl;
ii.上层淡绿色溶液中的主要溶质为NaCl和少量Cu(HSO3)2。
结论:本实验中较多量的新制氢氧化铜与二氧化硫发生了氧化还原反应,少量与之发生了复分解反应,二者为竞争关系。检验淡绿色溶液中含有
 的操作方法是
的操作方法是
您最近半年使用:0次
解题方法
7 . “价-类二维图”是元素化合物知识学习的重要模型,下图是某短周期主族元素的“价-类二维图”,其最高化合价c与最低化合价a的代数和为4。
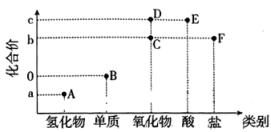
A.实验室可用 溶液吸收气体A 溶液吸收气体A |
| B.C分子的VSEPR模型为V形 |
| C.可用溴水检验F是否变质 |
| D.工业上通过B→D→E两步转化制备E |
您最近半年使用:0次
8 . “科学探究与创新意识”是化学学科核心素养之一、某研究小组用下图装置进行探究实验。下列说法正确的是
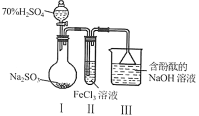
A.Ⅰ中70% 在反应中作氧化剂 在反应中作氧化剂 |
B.取少量反应后Ⅱ中溶液加入 溶液有蓝色沉淀生成 溶液有蓝色沉淀生成 |
C.Ⅱ中发生反应的离子方程式为: |
D.Ⅲ中溶液褪色,说明 具有漂白性 具有漂白性 |
您最近半年使用:0次
解题方法
9 . 研究发现,利用烟气脱硫脱硝一体化技术,脱硫的同时也可以脱硝。_____

您最近半年使用:0次
名校
10 . 下列指定反应的离子方程式正确的是
A.用惰性电极电解CuCl2溶液: 2H2O + Cu2++ 2Cl- Cu(OH)2+ H2↑+ Cl2↑ Cu(OH)2+ H2↑+ Cl2↑ |
B.将少量氯气通入NaHSO3溶液中:HSO + H2O +Cl2=2Cl-+ 3H++SO + H2O +Cl2=2Cl-+ 3H++SO |
C.0.1mol/L AgNO3溶液中加入过量浓氨水:Ag+ + 2NH3·H2O =Ag(NH3)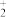 + 2H2O + 2H2O |
D.将NaHSO3溶液滴入Ba(NO3)2溶液产生白色沉淀:2HSO + Ba2+ =H2O+SO2↑+BaSO3↓ + Ba2+ =H2O+SO2↑+BaSO3↓ |
您最近半年使用:0次



