名校
解题方法
1 . 根据如下装置图,以下说法不正确 的是

| A.该实验证明氨气极易溶于水 |
| B.溶液未充满烧瓶,说明氨在水中的溶解达到最大限度 |
C.含氮微粒的物质的量在水进入烧瓶前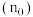 、后 、后 存在: 存在: |
D.烧瓶充满 ,胶头滴管和烧杯中加入浓碱液也可能形成喷泉 ,胶头滴管和烧杯中加入浓碱液也可能形成喷泉 |
您最近一年使用:0次
解题方法
2 . 某实验小组研究FeCl3溶液与Na2SO3溶液之间的反应,进行如下实验探究:
查阅资料:
| 编号 | 实验试剂及用量 | 开始混合时现象 | 30min时 | 3天后 |
| I | 取1.0mol/LFeCl3溶液2mL滴加1.0mol/LNa2SO3溶液2滴 | 溶液立即变为红色 | 红色明显变浅 | 溶液呈黄绿色 | |
| Ⅱ | 取1.0mol/LNa2SO3溶液2mL滴加1.0mol/LFeCl3溶液2滴 | 溶液立即变为红色,比I中略浅 | 与开始混合时一致 | 溶液呈黄绿色 |

| A.配制 FeCl3溶液时,先将FeCl3溶于浓盐酸,再稀释至指定浓度是为了抑制Fe3+的水解 |
| B.上述实验在开始混合时观察到的现象不涉及氧化还原反应,实验Ⅱ中红色比I中略浅的原因可能是Fe3+起始浓度小 |
| C.1~30min立即变红,随后变浅,证明生成红色配合物速率较快,红色配合物生成橙色配合物速率较慢 |
| D.取黄绿色溶液先滴加HCl溶液,再滴加BaCl2溶液,出现白色沉淀,可证明FeCl3溶液与Na2SO3溶液发生了氧化还原反应 |
您最近一年使用:0次
名校
解题方法
3 . 验证FeSO4的性质,进行如下实验。
实验序号 | 验证性质 | 实验装置 | 试剂X | 实验现象 |
① | 能与某些盐反应 |
| BaCl2溶液 | 产生白色沉淀 |
② | 能与碱反应 | NaOH溶液 | 产生白色絮状沉淀,迅速变为灰绿色,一段时间后变成红褐色 | |
③ | 具有氧化性 | 锌粒 | 锌粒表面变黑,溶液浅绿色褪去 | |
④ | 具有还原性 | KSCN溶液氯水 | 滴加KSCN溶液,无明显现象,再滴加氯水,溶液变为红色 |
下列关于该实验的说法不正确的是
A.①中产生白色沉淀的原因: |
B.②中沉淀变成红褐色的原因: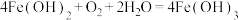 |
| C.③中用镁条(已打磨)替换锌粒,也可以证明FeSO4具有氧化性 |
| D.④中调换试剂的加入顺序,也可以证明FeSO4具有还原性 |
您最近一年使用:0次
名校
解题方法
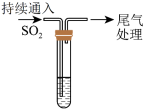
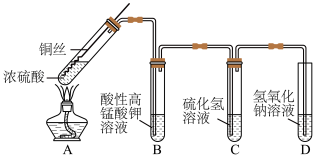
4 . 某化学实验小组的同学利用铜与浓硫酸反应制取二氧化硫并研究其性质,所用实验装置如下:
(1)向外拉铜丝,终止反应,冷却后,进一步证明A装置试管中反应所得产物含有铜离子的操作是___________ 。
(2)用化学方程式表示氢氧化钠溶液的作用是___________ 。
(3)装置A中反应的化学方程式是___________ 。
(4)装置B中反应的离子方程式是___________ 。装置C中反应的化学方程式是___________ 。
(5)化学实验小组的同学发现试管中有黑色物质产生,猜测黑色物质中可能含有CuO、 和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是___________(填字母)。已知:
和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是___________(填字母)。已知: 、CuS不溶于稀硫酸。
、CuS不溶于稀硫酸。
(1)向外拉铜丝,终止反应,冷却后,进一步证明A装置试管中反应所得产物含有铜离子的操作是
(2)用化学方程式表示氢氧化钠溶液的作用是
(3)装置A中反应的化学方程式是
(4)装置B中反应的离子方程式是
(5)化学实验小组的同学发现试管中有黑色物质产生,猜测黑色物质中可能含有CuO、
 和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是___________(填字母)。已知:
和CuS,针对产生的黑色物质,该小组同学利用装置A用不同浓度的浓硫酸与铜反应继续实验探究,并获得数据如下表。下列说法错误的是___________(填字母)。已知: 、CuS不溶于稀硫酸。
、CuS不溶于稀硫酸。硫酸浓度/(mol·L ) ) | 黑色物质出现的温度/℃ | 黑色物质消失的温度/℃ |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
| A.取黑色物质洗涤、干燥后称量,加入足量稀硫酸充分混合,再取固体洗涤、干燥后称量,固体质量不变,说明黑色物质中不含CuO |
B.黑色物质消失过程中有 、 、 生成 生成 |
| C.相同条件下,硫酸浓度越大,反应速率越快,黑色物质越易出现、越易消失 |
| D.硫酸浓度为16 mol/L时,先升温至:250℃以上,再将铜丝与浓硫酸接触,可以避免产生黑色物质 |
您最近一年使用:0次
5 . 高分子 的合成方法如图:
的合成方法如图:
 的合成方法如图:
的合成方法如图:
A.高分子 可降解为小分子 可降解为小分子 |
| B.酪氨酸到环二肽的过程中,可能有聚合物生成 |
| C.环二肽可使酸性高锰酸钾溶液褪色,证明其分子中含有羟基 |
| D.以上合成路线中的4种有机物,都既能与酸反应也能与碱反应 |
您最近一年使用:0次
名校
解题方法
6 . 某化学小组欲探究反应“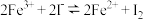 ”为可逆反应,做了如下实验:
”为可逆反应,做了如下实验:

已知:
现象为:实验ii中产生了黄色沉淀;实验iii中溶液变蓝;实验iv中溶液不变蓝,下列说法中不正确 的是
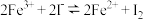 ”为可逆反应,做了如下实验:
”为可逆反应,做了如下实验:
已知:

现象为:实验ii中产生了黄色沉淀;实验iii中溶液变蓝;实验iv中溶液不变蓝,下列说法中
A.实验ii中产生黄色沉淀的离子方程式为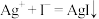 |
B.实验iii加淀粉溶液变蓝,证明棕黄色溶液中有 生成 生成 |
C.设计实验iv的目的是为了排除空气中氧气氧化 的可能 的可能 |
D.通过上述实验可以证明“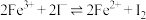 ”为可逆反应 ”为可逆反应 |
您最近一年使用:0次
2024-01-20更新
|
148次组卷
|
3卷引用:北京市顺义区2023-2024学年高二上学期期末质量监测化学试题
名校
解题方法
7 . 25℃时,向40 mL 0.05 mol/L的 溶液中一次性加入10 mL 0.15 mol/L的KSCN溶液(体积变化忽略不计),发生反应
溶液中一次性加入10 mL 0.15 mol/L的KSCN溶液(体积变化忽略不计),发生反应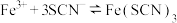 ,混合溶液中
,混合溶液中 与反应时间(t)的变化如图所示。下列说法不正确的是
与反应时间(t)的变化如图所示。下列说法不正确的是
 溶液中一次性加入10 mL 0.15 mol/L的KSCN溶液(体积变化忽略不计),发生反应
溶液中一次性加入10 mL 0.15 mol/L的KSCN溶液(体积变化忽略不计),发生反应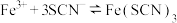 ,混合溶液中
,混合溶液中 与反应时间(t)的变化如图所示。下列说法不正确的是
与反应时间(t)的变化如图所示。下列说法不正确的是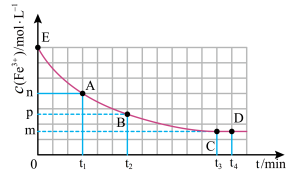
A. 时向溶液中加入50 mL 0.1 mol/L KCl溶液,平衡逆向移动。 时向溶液中加入50 mL 0.1 mol/L KCl溶液,平衡逆向移动。 |
| B.E点对应的坐标为(0,0.04) |
C.在25℃时该反应的平衡常数为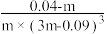 |
D. 分钟后加入少量KSCN固体,溶液红色加深,该现象可以证明 分钟后加入少量KSCN固体,溶液红色加深,该现象可以证明 与SCN-的反应是可逆反应 与SCN-的反应是可逆反应 |
您最近一年使用:0次
2023-12-12更新
|
234次组卷
|
3卷引用:北京市第十二中学2023-2024学年高二上学期期中考试化学试题
名校
8 . 小组同学探究盐溶液对反应 (血红色)的影响。将
(血红色)的影响。将
 的
的 溶液与
溶液与 的
的 溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
ii. (黄色)
(黄色)
iii.已知 对实验无影响
对实验无影响
下列说法不正确的是
 (血红色)的影响。将
(血红色)的影响。将
 的
的 溶液与
溶液与 的
的 溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。
溶液混合,分别加入等量的试剂①~④,测得平衡后体系的透光率如下图所示。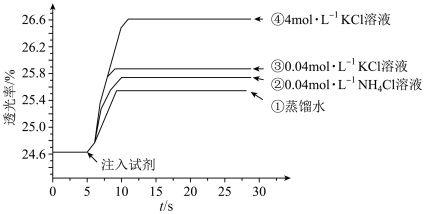
ii.
 (黄色)
(黄色)iii.已知
 对实验无影响
对实验无影响下列说法不正确的是
A.注入试剂①后溶液透光率增大,证明 逆向移动 逆向移动 |
B.透光率③比②高,可能是阳离子种类或溶液 不同导致的 不同导致的 |
C.透光率④比③高,可能发生了反应 |
D.若要证明试剂③中 对平衡体系有影响,还应使用 对平衡体系有影响,还应使用 的 的 溶液进行对照实验 溶液进行对照实验 |
您最近一年使用:0次
2023-11-21更新
|
366次组卷
|
7卷引用:北京市对外经济贸易大学附属中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
9 . 某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如下:
已知:CuCl为白色固体,难溶于水,能溶于浓盐酸。下列说法不正确的是
| 装置 |
| |
| 序号 | 试管中的药品 | 现象 |
| 实验Ⅰ | 1.5mL1mol·L-1CuSO4溶液和3.5mL1mol·L-1NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
| 实验Ⅱ | 1.5mL1mol·L-1CuCl2溶液和3.5mL1mol·L-1NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
| A.取少量Cu2O固体于试管中,加入5mL0.1mol·L-1NaOH溶液,持续通入SO2,若试管底部有少量紫红色固体,溶液呈绿色,证明实验Ⅰ中砖红色沉淀为Cu2O |
| B.将实验Ⅱ中白色沉淀洗涤干净后,加入浓盐酸,沉淀溶解,然后加入蒸馏水,产生白色沉淀,证明白色沉淀为CuCl |
| C.实验Ⅱ与实验Ⅰ现象不同是因为阴离子不同造成的 |
D.实验Ⅰ、Ⅱ中不一定生成了SO |
您最近一年使用:0次
名校
10 . 某学习小组通过如图所示装置探究 与
与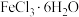 ,能否反应产生
,能否反应产生 ,已知
,已知 的升华温度为315℃。下列相关说法
的升华温度为315℃。下列相关说法不正确 的是
 与
与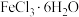 ,能否反应产生
,能否反应产生 ,已知
,已知 的升华温度为315℃。下列相关说法
的升华温度为315℃。下列相关说法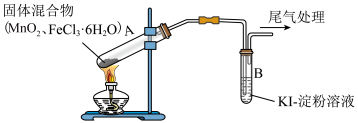
| 操作 | 现象 |
| 点燃酒精灯,加热 | ⅰ.试管A中部分固体溶解,上方出现白雾 ⅱ.稍后,试管A中产生黄色气体,管壁附着黄色液滴 ⅲ.试管B中溶液变蓝 |
A.为保证实验的严谨性,应另设置加热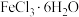 的对照实验 的对照实验 |
B.黄色气体中可能含有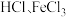 和 和 |
C.为进一步确认黄色气体是否含有 ,应在A、B间增加盛有 ,应在A、B间增加盛有 饱和溶液的洗气瓶 饱和溶液的洗气瓶 |
D.若实验证明A中产生 ,综合上述现象,试管A中的固体产物可能为 ,综合上述现象,试管A中的固体产物可能为 |
您最近一年使用:0次
2024-01-27更新
|
318次组卷
|
3卷引用: 北京市首都师范大学附属中学2023-2024学年高三上学期1月阶段化学练习