名校
解题方法
1 . 如图是中学化学常见物质的转化关系,部分物质和反应条件略去。其中A是地壳中含量最多的金属元素的单质,B是一种红棕色粉末;通常情况下,乙为黄绿色气体单质,H是有刺激性气味的气体,在工业上可通过反应⑥在高温高压、催化剂条件下合成;J为难溶于水的红褐色固体;反应⑦在工业上可用于制作印刷电路板。
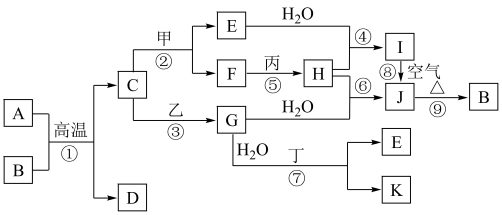
请回答下列问题:
(1)组成物质C的元素在元素周期表中的位置为___________ 。
(2)在反应①~⑨中,不属于氧化还原反应的是___________ 。
(3)写出下列反应的化学方程式:
反应①:___________ 。
反应⑧:___________ 。
(4)写出乙与E在溶液中反应的离子方程式:___________ 。
(5)在E溶液中加入与E等物质的量的一种淡黄色固体,恰好使E转化为J,写出该反应的离子方程式:___________ 。
(6)检验G中阳离子的试剂的化学式为___________ ,反应现象为___________ 。

请回答下列问题:
(1)组成物质C的元素在元素周期表中的位置为
(2)在反应①~⑨中,不属于氧化还原反应的是
(3)写出下列反应的化学方程式:
反应①:
反应⑧:
(4)写出乙与E在溶液中反应的离子方程式:
(5)在E溶液中加入与E等物质的量的一种淡黄色固体,恰好使E转化为J,写出该反应的离子方程式:
(6)检验G中阳离子的试剂的化学式为
您最近一年使用:0次
2 . 氟他胺 G 是一种可用于治疗肿瘤的药物。实验室由芳香烃 A 制备 G 的合成路线如下:
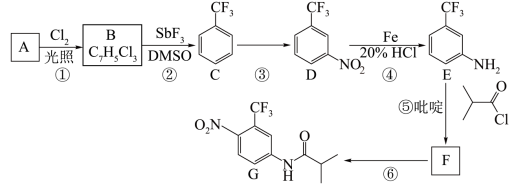
回答下列问题:
(1)C 的名称是_____________ 。
(2)③的反应试剂和反应条件分别是_____________ ,该反应类型是_____________ 。
(3)⑤的反应方程式为______________ 。
(4)G 的分子式为_____________ 。
(5)H 是G 的同分异构体,其苯环上的取代基与G 的相同但位置不同,则H 可能的结构有_____________ 种。
(6)4-甲氧基乙酰苯胺(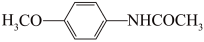 )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(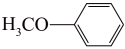 )制备 4-甲氧基乙酰苯胺的合成路线
)制备 4-甲氧基乙酰苯胺的合成路线______________ (用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件,其他试剂任选)

回答下列问题:
(1)C 的名称是
(2)③的反应试剂和反应条件分别是
(3)⑤的反应方程式为
(4)G 的分子式为
(5)H 是G 的同分异构体,其苯环上的取代基与G 的相同但位置不同,则H 可能的结构有
(6)4-甲氧基乙酰苯胺(
 )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚( )制备 4-甲氧基乙酰苯胺的合成路线
)制备 4-甲氧基乙酰苯胺的合成路线
您最近一年使用:0次
名校
3 . A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请用化学用语回答下列问题。
(1)写出元素符号A:___________ B:___________ G___________ ,写出元素B的基态原子的轨道表示式:___________ 。
(2)C、D、E三种元素的原子半径由大到小的顺序___________ 。
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,其空间构型分别为:___________ ,___________ ,___________ ,其中C的简单气态氢化物的键角为:___________ 。
(4)已知元素A、B形成的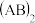 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为___________ 。
(5)F元素的简单阴离子结构示意图___________ 。电解D与F形成的化合物的水溶液在工业上有着重要应用,试写出其电解的总的化学反应方程式:___________ 。
(6)元素G位于周期表的___________ 区,其价电子的排布式为:___________ ,该元素可形成 、
、 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是___________ 。
(7)短周期元素M与元素E在周期表中的位置呈现对角线关系,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是___________ 化合物(填“离子”或“共价”)。推测M的最高价氧化物对应水化物___________ (填“能”或“不能”)与D的最高价氧化物对应水化物发生反应。
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子最外层电子排布式为 |
| F | 基态原子的最外层p轨道有2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 生活中使用最多的一种金属 |
(2)C、D、E三种元素的原子半径由大到小的顺序
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,其空间构型分别为:
(4)已知元素A、B形成的
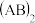 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为(5)F元素的简单阴离子结构示意图
(6)元素G位于周期表的
 、
、 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是(7)短周期元素M与元素E在周期表中的位置呈现对角线关系,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
您最近一年使用:0次
2022-03-03更新
|
652次组卷
|
2卷引用:天津市南开区南开中学2021-2022学年高二上学期期末检测化学试题
名校
解题方法
4 . 短周期元素W、X、Y和Z在元素周期表中的相对位置如表所示,这四种元素原子的最外层电子数之和为21。下列关系正确的是
| W | X | |||
| Y | Z |
A.氢化物沸点: | B.化合物熔点: |
C.氧化物对应水化物的酸性: | D.简单离子的半径: |
您最近一年使用:0次
名校
5 . 高铁酸钾(K2FeO4)为高效净水剂,紫色固体,易溶于水,微溶于KOH溶液,具有强氧化性,在酸性溶液中完全、快速产生O2,在碱性溶液中较稳定。某实验小组制备高铁酸钾并探究性质。
(1)制备K2FeO4 (夹持装置略)

①Fe元素在元素周期表中的位置为__ 。
②A为氯气发生装置,A中离子反应方程式是__ 。
③将除杂装置B补充完整并标明所用试剂__ 。
④C中得到紫色固体和溶液,C中发生的主要反应为__ (用化学方程式表示)。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2,为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
i.由方案1中溶液变红可知a中含有__ 离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能有__ 产生(用化学式表示)。
ii.方案Ⅱ可证明K2FeO4氧化了Cl-,用KOH溶液洗涤的目的是__ 。
②根据K2FeO4的制备实验得出:氧化性Cl2__ FeO (填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是__ 。
③资料表明,酸性溶液中的氧化性FeO >MnO
>MnO ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性FeO
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性FeO >MnO
>MnO ,若能,请说明理由;若不能,进一步设计实验方案,理由或方案:
,若能,请说明理由;若不能,进一步设计实验方案,理由或方案:__ 。
(1)制备K2FeO4 (夹持装置略)

①Fe元素在元素周期表中的位置为
②A为氯气发生装置,A中离子反应方程式是
③将除杂装置B补充完整并标明所用试剂
④C中得到紫色固体和溶液,C中发生的主要反应为
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2,为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
| 方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色 |
| 方案Ⅱ | 用KOH溶液充分洗涤 中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b,取少量b,滴加盐酸,有Cl2产生。 中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b,取少量b,滴加盐酸,有Cl2产生。 |
ii.方案Ⅱ可证明K2FeO4氧化了Cl-,用KOH溶液洗涤的目的是
②根据K2FeO4的制备实验得出:氧化性Cl2
 (填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和FeO 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是③资料表明,酸性溶液中的氧化性FeO
 >MnO
>MnO ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性FeO
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性FeO >MnO
>MnO ,若能,请说明理由;若不能,进一步设计实验方案,理由或方案:
,若能,请说明理由;若不能,进一步设计实验方案,理由或方案:
您最近一年使用:0次
名校
解题方法
6 . 一种重要的有机化工原料有机物X,下面是以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。Y是一种功能高分子材料。
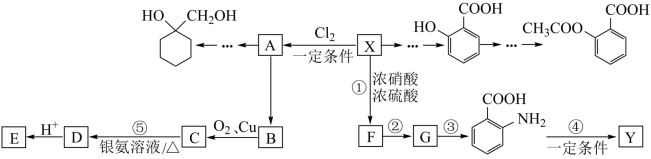
已知:①X为芳香烃,其相对分子质量为92
②烷基苯在高锰酸钾的作用下,侧链被氧化成羧基: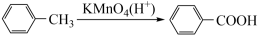
③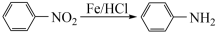 (苯胺,易被氧化)
(苯胺,易被氧化)
④R1-NH2+R2-COOH
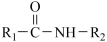 +H2O
+H2O
请根据本题所给信息与所学知识回答下列问题:
(1)X的分子式为___________ ,该分子最多有___________ 个原子共平面。
(2)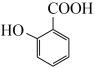 的名称为
的名称为___________ ,G中官能团名称为___________ 。
(3)反应③的反应类型是___________ :已知A为一氯代物,则E的结构简式是___________ 。
(4)反应⑤的化学方程式为___________ 。
(5)阿司匹林有多种同分异构体,满足下列条件的同分异构体有___________ 种:
①含有苯环;
②既不能发生水解反应,也不能发生银镜反应;
③1 mol该有机物能与2 mol NaHCO3完全反应。
(6)参照上述合成路线,结合所学知识,设计一条以A为原料制备 的合成路线(无机试剂任用)
的合成路线(无机试剂任用) _______ 。

已知:①X为芳香烃,其相对分子质量为92
②烷基苯在高锰酸钾的作用下,侧链被氧化成羧基:
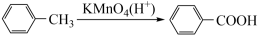
③
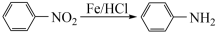 (苯胺,易被氧化)
(苯胺,易被氧化) ④R1-NH2+R2-COOH

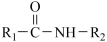 +H2O
+H2O请根据本题所给信息与所学知识回答下列问题:
(1)X的分子式为
(2)
 的名称为
的名称为(3)反应③的反应类型是
(4)反应⑤的化学方程式为
(5)阿司匹林有多种同分异构体,满足下列条件的同分异构体有
①含有苯环;
②既不能发生水解反应,也不能发生银镜反应;
③1 mol该有机物能与2 mol NaHCO3完全反应。
(6)参照上述合成路线,结合所学知识,设计一条以A为原料制备
 的合成路线(无机试剂任用)
的合成路线(无机试剂任用)
您最近一年使用:0次
名校
解题方法
7 . 有机物X是药物的中间体,它的一种合成路线如下。

已知:

(1)A无支链,A中含有的官能团名称是___ 。
(2)A连续氧化的步骤如下:

A转化为B的化学方程式是___ 。
(3)M为芳香化合物,其结构简式是___ 。
(4)M→N的化学方程式是___ ,反应类型是___ 。
(5)下列说法不正确的是___ 。
a.1molD与NaOH溶液反应时,最多消耗2molNaOH
b.E在一定条件下可生成高分子化合物
c.F能发生酯化反应和消去反应
(6)Q的结构简式是___ 。
(7)以乙烯为起始原料,选用必要的无机试剂合成A,写出合成路线___ (用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。

已知:


(1)A无支链,A中含有的官能团名称是
(2)A连续氧化的步骤如下:

A转化为B的化学方程式是
(3)M为芳香化合物,其结构简式是
(4)M→N的化学方程式是
(5)下列说法不正确的是
a.1molD与NaOH溶液反应时,最多消耗2molNaOH
b.E在一定条件下可生成高分子化合物

c.F能发生酯化反应和消去反应
(6)Q的结构简式是
(7)以乙烯为起始原料,选用必要的无机试剂合成A,写出合成路线
您最近一年使用:0次
2020-01-14更新
|
418次组卷
|
6卷引用:天津市南开中学2021届高三上学期第五次月考化学试卷
名校
解题方法
8 . X、Y、Z、E、T均为短周期元素,在周期表中的相对位置如图1。X是短周期中原子半径最大的元素; X、Y在同一周期,Y是常见的半导体材料; E的最高价氧化物对应水化物有强脱水性。
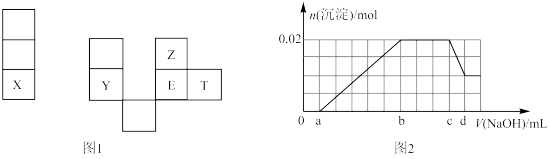
根据判断出的元素回答问题:
(1)T在元素周期表中的位置________________________ ;
(2)这几种元素的氢化物中,水溶液酸性最强的是_____________________ (填化学式);YZ2 的熔点 ______ EZ2 的熔点(填高于或低于);
(3)E2T2 的电子式______________________________ ;
(4)工业上制备单质X的化学反应方程式_______________________ ;
(5)已知1mol晶体Y在足量Z2中燃烧,恢复至室温,放出989.2 kJ热量,写出该反应的热化学方程式:_______________ ;
(6)某溶液中可能含有以下阳离子(忽略由水电离产生的H+、OH-):H+、NH 、K+、Mg2+、Al3+,现取100mL该溶液逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如上图2所示。
、K+、Mg2+、Al3+,现取100mL该溶液逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如上图2所示。
①在实验中,NaOH溶液滴至b~c段过程中发生的离子反应方程式为____________________________ ;NaOH溶液的浓度为_____ mol·L-1 (用字母c、d表示);
②原溶液中含有的Mg2+、Al3+、H+,其物质的量之比n(Mg2+):n(Al3+):n(H+)为_________ 。

根据判断出的元素回答问题:
(1)T在元素周期表中的位置
(2)这几种元素的氢化物中,水溶液酸性最强的是
(3)E2T2 的电子式
(4)工业上制备单质X的化学反应方程式
(5)已知1mol晶体Y在足量Z2中燃烧,恢复至室温,放出989.2 kJ热量,写出该反应的热化学方程式:
(6)某溶液中可能含有以下阳离子(忽略由水电离产生的H+、OH-):H+、NH
 、K+、Mg2+、Al3+,现取100mL该溶液逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如上图2所示。
、K+、Mg2+、Al3+,现取100mL该溶液逐滴滴加NaOH溶液,测得沉淀的物质的量与NaOH溶液的体积关系如上图2所示。①在实验中,NaOH溶液滴至b~c段过程中发生的离子反应方程式为
②原溶液中含有的Mg2+、Al3+、H+,其物质的量之比n(Mg2+):n(Al3+):n(H+)为
您最近一年使用:0次
2016-12-09更新
|
437次组卷
|
2卷引用:天津市南开中学2022-2023学年高三上学期统练三化学试题
名校
9 . I按要求填空,括号内为有机物的结构简式或分子式
(1)有机物甲(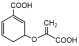 )中含氧官能团的名称是
)中含氧官能团的名称是________________
(2)有机物乙(分子式为C3H6O3)可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的乙为无色粘稠液体,易溶于水。乙的核磁共振氢谱如图 ,则乙的名称为
,则乙的名称为______________
(3)有机物丙(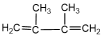 )的反式1,4-加成聚合反应产物的结构简式为
)的反式1,4-加成聚合反应产物的结构简式为______________
(4)已知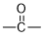 为平面结构,则有机物丁(
为平面结构,则有机物丁( )分子中最多有
)分子中最多有_____ 个原子在同一平面内
II化学式为C9H10O2的有机物有如下的转化关系:
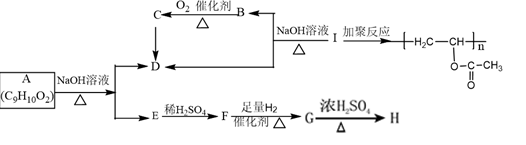
已知:① F与FeCl3溶液能发生显色反应
②从G到H的反应中,H只有一种结构且能使溴水褪色。
③羟基与双键碳原子相连接时,不稳定,易发生转化:
请回答下列问题:
(5)写出物质D的名称_______________
(6)B→C的反应类型:_____________________________ 。G→H反应类型:__________________
(7)A生成D和E的化学方程式:_______________________ 。
(8)有机物B与银氨溶液反应的离子方程式________________________ 。
(9)写出由苯酚合成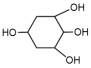 的合成路线流程图(无机试剂任选,要注明条件)
的合成路线流程图(无机试剂任选,要注明条件)_______
(1)有机物甲(
 )中含氧官能团的名称是
)中含氧官能团的名称是(2)有机物乙(分子式为C3H6O3)可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的乙为无色粘稠液体,易溶于水。乙的核磁共振氢谱如图
 ,则乙的名称为
,则乙的名称为(3)有机物丙(
 )的反式1,4-加成聚合反应产物的结构简式为
)的反式1,4-加成聚合反应产物的结构简式为(4)已知
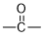 为平面结构,则有机物丁(
为平面结构,则有机物丁( )分子中最多有
)分子中最多有II化学式为C9H10O2的有机物有如下的转化关系:

已知:① F与FeCl3溶液能发生显色反应
②从G到H的反应中,H只有一种结构且能使溴水褪色。
③羟基与双键碳原子相连接时,不稳定,易发生转化:

请回答下列问题:
(5)写出物质D的名称
(6)B→C的反应类型:
(7)A生成D和E的化学方程式:
(8)有机物B与银氨溶液反应的离子方程式
(9)写出由苯酚合成
 的合成路线流程图(无机试剂任选,要注明条件)
的合成路线流程图(无机试剂任选,要注明条件)
您最近一年使用:0次
名校
解题方法
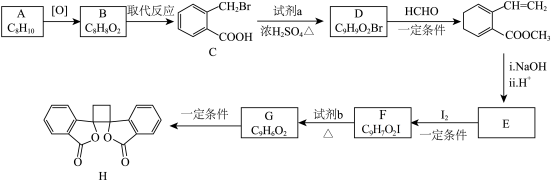
10 . 具有抗菌作用的白头翁素衍生物H的合成路线如下图所示:
已知:i.RCH2Br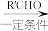 R﹣HC═CH﹣R′
R﹣HC═CH﹣R′
ii.R﹣HC═CH﹣R′

iii.R﹣HC═CH﹣R′

(以上R、R'、R''代表氢、烷基或芳基等)
(1)A属于芳香烃,其名称是_______________________ 。
(2)D的结构简式是_______________________________ 。
(3)由F生成G的反应类型是________________________________________ 。
(4)由E与I2在一定条件下反应生成F的化学方程式是_____________________ ;此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是_______________________________ 。
(5)下列说法正确的是___________ (选填字母序号)。
A. G存在顺反异构体
B. 由G生成H的反应是加成反应
C. 1 mol G最多可以与1 mol H2发生加成反应
D. 1 mol F或1 mol H与足量NaOH溶液反应,均消耗2 molNaOH
(6)以乙烯为起始原料,结合已知信息选用必要的无机试剂合成 写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。___________________

已知:i.RCH2Br
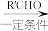 R﹣HC═CH﹣R′
R﹣HC═CH﹣R′ii.R﹣HC═CH﹣R′


iii.R﹣HC═CH﹣R′


(以上R、R'、R''代表氢、烷基或芳基等)
(1)A属于芳香烃,其名称是
(2)D的结构简式是
(3)由F生成G的反应类型是
(4)由E与I2在一定条件下反应生成F的化学方程式是
(5)下列说法正确的是
A. G存在顺反异构体
B. 由G生成H的反应是加成反应
C. 1 mol G最多可以与1 mol H2发生加成反应
D. 1 mol F或1 mol H与足量NaOH溶液反应,均消耗2 molNaOH
(6)以乙烯为起始原料,结合已知信息选用必要的无机试剂合成
 写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
您最近一年使用:0次
2019-02-14更新
|
884次组卷
|
8卷引用:天津市六校(天津中学、南开中学、实验中学等)2020届高三上学期期初检测化学试题
天津市六校(天津中学、南开中学、实验中学等)2020届高三上学期期初检测化学试题【校级联考】湖北省荆州中学、宜昌一中等“荆、荆、襄、宜四地七校考试联盟”2019届高三上学期期末考试理科综合化学试题【校级联考】“荆 、荆、襄、宜四地七校考试联盟”2019届高三下学期2月联考化学试题【全国百强校】江西省宜春市上高二中2019届高三下学期第七次月考理科综合化学试题河北省秦皇岛市六校2020届高三上学期期初检测联考化学试题湖北名师联盟(人教版)2019-2020学年高三上学期第二次月考精编仿真金卷化学试题2020届高三化学二轮冲刺新题专练——有机化学基础选做题专题4.2 有机化学基础(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升



