名校
解题方法
1 . 氮化锶 在工业上广泛用于生产荧光粉.锶与氮气在加热条件下可生成氮化锶,氮化锶遇水剧烈反应.某同学设计如下装置制备氮化锶(各装置盛装足量试剂),使用的氮气样品可能含有少量
在工业上广泛用于生产荧光粉.锶与氮气在加热条件下可生成氮化锶,氮化锶遇水剧烈反应.某同学设计如下装置制备氮化锶(各装置盛装足量试剂),使用的氮气样品可能含有少量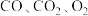 等气体杂质。
等气体杂质。
已知:醋酸二氨合亚铜 溶液能定量吸收
溶液能定量吸收 ,但易被
,但易被 氧化,失去吸收
氧化,失去吸收 能力;连苯三酚碱性溶液能定量吸收
能力;连苯三酚碱性溶液能定量吸收 。
。
Ⅰ.氮化锶的制取
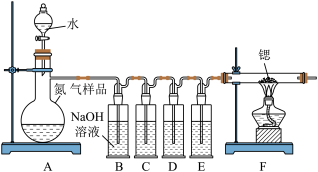
(1)装置C、D、E盛装的试剂分别是_____________ (填代号)。
甲.连苯三酚碱性溶液 乙.浓硫酸 丙.醋酸二氨合亚铜溶液
(2)该套装置设计存在缺陷,可能会导致产品变质,提出改进方案_____________ 。
Ⅱ.产品纯度的测定
称取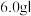 中所得产品,加入干燥的三颈烧瓶中,然后由仪器3加入蒸馏水,通入水蒸气,将产生的氨全部蒸出,用
中所得产品,加入干燥的三颈烧瓶中,然后由仪器3加入蒸馏水,通入水蒸气,将产生的氨全部蒸出,用 的盐酸标准溶液完全吸收(吸收液体积变化忽略不计)。从烧杯中量取
的盐酸标准溶液完全吸收(吸收液体积变化忽略不计)。从烧杯中量取 的吸收液,用
的吸收液,用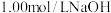 标准溶液滴定过剩的
标准溶液滴定过剩的 ,到终点时消耗
,到终点时消耗 溶液。(图中夹持装置略)
溶液。(图中夹持装置略)

(3)三颈烧瓶中发生反应的化学方程式为________________________________________ 。
(4)装置中长玻璃管的作用原理是_____________ ;仪器3的名称是_____________ 。
(5)用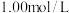 的
的 标准溶液滴定过剩的
标准溶液滴定过剩的 时所选指示剂为
时所选指示剂为_____________ ;如何判断滴定终点的到达?__________________________________________________ 。
(6)产品纯度为_____________ 。(保留三位有效数字)
(7)下列实验操作可能使氮化锶 测定结果偏低的是
测定结果偏低的是_____________ (填字母)。
a.滴定前碱式滴定管未排气泡,滴定后气泡消失
b.读数时,滴定前平视,滴定后俯视
c.滴定后,碱式滴定管尖嘴外还悬着一滴液体
 在工业上广泛用于生产荧光粉.锶与氮气在加热条件下可生成氮化锶,氮化锶遇水剧烈反应.某同学设计如下装置制备氮化锶(各装置盛装足量试剂),使用的氮气样品可能含有少量
在工业上广泛用于生产荧光粉.锶与氮气在加热条件下可生成氮化锶,氮化锶遇水剧烈反应.某同学设计如下装置制备氮化锶(各装置盛装足量试剂),使用的氮气样品可能含有少量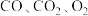 等气体杂质。
等气体杂质。已知:醋酸二氨合亚铜
 溶液能定量吸收
溶液能定量吸收 ,但易被
,但易被 氧化,失去吸收
氧化,失去吸收 能力;连苯三酚碱性溶液能定量吸收
能力;连苯三酚碱性溶液能定量吸收 。
。Ⅰ.氮化锶的制取

(1)装置C、D、E盛装的试剂分别是
甲.连苯三酚碱性溶液 乙.浓硫酸 丙.醋酸二氨合亚铜溶液
(2)该套装置设计存在缺陷,可能会导致产品变质,提出改进方案
Ⅱ.产品纯度的测定
称取
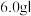 中所得产品,加入干燥的三颈烧瓶中,然后由仪器3加入蒸馏水,通入水蒸气,将产生的氨全部蒸出,用
中所得产品,加入干燥的三颈烧瓶中,然后由仪器3加入蒸馏水,通入水蒸气,将产生的氨全部蒸出,用 的盐酸标准溶液完全吸收(吸收液体积变化忽略不计)。从烧杯中量取
的盐酸标准溶液完全吸收(吸收液体积变化忽略不计)。从烧杯中量取 的吸收液,用
的吸收液,用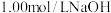 标准溶液滴定过剩的
标准溶液滴定过剩的 ,到终点时消耗
,到终点时消耗 溶液。(图中夹持装置略)
溶液。(图中夹持装置略)
(3)三颈烧瓶中发生反应的化学方程式为
(4)装置中长玻璃管的作用原理是
(5)用
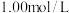 的
的 标准溶液滴定过剩的
标准溶液滴定过剩的 时所选指示剂为
时所选指示剂为(6)产品纯度为
(7)下列实验操作可能使氮化锶
 测定结果偏低的是
测定结果偏低的是a.滴定前碱式滴定管未排气泡,滴定后气泡消失
b.读数时,滴定前平视,滴定后俯视
c.滴定后,碱式滴定管尖嘴外还悬着一滴液体
您最近一年使用:0次
2 . 某化学小组欲测定一份长期放置的补铁药品(有效成分是琥珀酸亚铁,化学式为FeC4H4O4)是否已变质,实验如下:
Ⅰ.取补铁药样品10.00g,碾碎,溶于100.0mL稀盐酸中,过滤,滤液呈浅黄绿色;
Ⅱ.取少量滤液,滴加KSCN溶液,溶液变为浅红色,再滴入3滴H2O2溶液,溶液红色加深;
Ⅲ.准确量取I中滤液20.00mL,加入足量H2O2溶液,再加入足量NaOH溶液,过滤、洗涤、常温晾干,获得Fe(OH)3固体0.642g;
Ⅳ.再准确量取I中滤液20.00mL于大试管中,加入1.00g铜粉,用胶塞塞紧试管口,充分振荡后过滤,最后得到干燥的铜粉0.936g。
(1)I中琥珀酸亚铁与稀盐酸反应生成FeCl2和琥珀酸(分子式为C4H6O4),说明酸性:C4H6O4_______ HCl(填“>”或“<”)。
(2)用离子方程式解释II中实验现象产生的原因:_______ 、Fe3++3SCN-=Fe(SCN)3。
(3)IV中发生反应的离子方程式为_______ 。
(4)该补铁药中琥珀酸亚铁变质程度为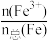 ×100%=
×100%=_______ (保留3位有效数字)。
(5)IV中溶液与铜粉反应时必须使用胶塞塞紧试管口,原因是_______ 。
Ⅰ.取补铁药样品10.00g,碾碎,溶于100.0mL稀盐酸中,过滤,滤液呈浅黄绿色;
Ⅱ.取少量滤液,滴加KSCN溶液,溶液变为浅红色,再滴入3滴H2O2溶液,溶液红色加深;
Ⅲ.准确量取I中滤液20.00mL,加入足量H2O2溶液,再加入足量NaOH溶液,过滤、洗涤、常温晾干,获得Fe(OH)3固体0.642g;
Ⅳ.再准确量取I中滤液20.00mL于大试管中,加入1.00g铜粉,用胶塞塞紧试管口,充分振荡后过滤,最后得到干燥的铜粉0.936g。
(1)I中琥珀酸亚铁与稀盐酸反应生成FeCl2和琥珀酸(分子式为C4H6O4),说明酸性:C4H6O4
(2)用离子方程式解释II中实验现象产生的原因:
(3)IV中发生反应的离子方程式为
(4)该补铁药中琥珀酸亚铁变质程度为
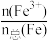 ×100%=
×100%=(5)IV中溶液与铜粉反应时必须使用胶塞塞紧试管口,原因是
您最近一年使用:0次
2023-08-26更新
|
169次组卷
|
5卷引用:山西省2023-2024学年高三上学期10月月考化学试题
名校
3 . 为探究某食品包装袋内一小包脱氧剂中的还原铁粉是否变质,分别取少量样品溶于盐酸,再进行下列实验,其中结论正确的是
| A.若滴加KSCN溶液,溶液变红,说明铁粉变质 |
| B.若滴加KSCN溶液,溶液未变红,说明铁粉未变质 |
| C.若依次滴加氯水、KSCN溶液,溶液变红,说明铁粉全部变质 |
| D.若滴加KSCN溶液,溶液未变红;再滴加氯水,溶液变红,说明铁粉部分变质 |
您最近一年使用:0次
2021-04-07更新
|
1031次组卷
|
16卷引用:山西省怀仁市2020-2021学年高一上学期期末考试化学试题
山西省怀仁市2020-2021学年高一上学期期末考试化学试题天津市和平区2017-2018学年高一上学期期末考试化学试题安徽省芜湖市第一中学2020-2021学年高一上学期第二次月考化学试题辽宁省沈阳市2020-2021学年高一上学期期末质量监测化学试题云南省曲靖市第二中学2020-2021学年高一上学期期末考试化学试题黑龙江省鹤岗市绥滨县第一中学2020-2021学年高一上学期期末考试化学(理)试题浙江省余姚中学2020-2021 学年高一上学期期中考试化学试题河北省石家庄精英中学2020-2021学年高二下学期期末考试化学试题(已下线)专题六 铁及其化合物(A卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)天津市静海区第一中学2021-2022学年高三上学期(9月)学生学业能力调研化学试题人教2019版必修第一册第三章 铁 金属材料复习与提高河南省洛阳市2021-2022学年高一上学期期末考试化学试题浙江省宁波市效实中学2022-2023学年高一上学期期中考试化学试题安徽省芜湖市2022-2023学年高一上学期期末教学质量统测化学试题9.2.1反应的合理选择(课中)-2019苏教版必修2课前课中课后河北师范大学附属中学2023-2024学年高一上学期12月月考化学试题
名校
4 . 由下列实验及现象,推出的相应结论正确的是( )
| 实验 | 现象 | 结论 |
| A.用铂丝蘸取某金属的盐溶液, 在酒精灯火焰上灼烧 | 火焰呈黄色 | 此盐溶液中含有 Na+,不含 K+ |
| B.①取少量绿矾样品,加水溶解, 滴加 KSCN 溶液 ②向溶液中通入空气 | ①溶液颜色无变化 ②溶液逐渐变红 | ①绿矾样品未变质 ②Fe2+易被空气氧化为 Fe3+ |
| C.①某溶液中加入 Ba(NO3)2 溶 液 ②再加入足量盐酸 | ①产生白色沉淀 ②仍有白色沉淀 | 原溶液中有 SO42﹣ |
| D.向碘水中加入等体积 CCl4, 振荡后静置 | 上层接近无色,下层显紫红色 | I2 在 CCl4 中的溶解度小于在水中 的溶解度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-12-26更新
|
234次组卷
|
3卷引用:【全国百强校】山西省太原市第五中学2018-2019学年高一上学期12月月考化学试题
5 . 根据下列实验操作与现象所得出的结论正确的是
| 选项 | 实验操作与现象 | 结论 |
| A | 将灼热后表面变黑的螺旋状铜丝伸入约 的乙醇中,铜丝能保持红热一段时间 的乙醇中,铜丝能保持红热一段时间 | 乙醇催化氧化反应是放热反应 |
| B | 取久置的 粉末,向其中滴加过量盐酸,产生无色气体 粉末,向其中滴加过量盐酸,产生无色气体 |  未变质 未变质 |
| C | 取少量医用酒精加入一小粒金属钠,产生无色气体 | 乙醇能与钠反应 |
| D | 将红热的铂丝伸入装有浓氨水的锥形瓶中的液面上方,瓶口出现少量红棕色气体 | 氨的氧化产物为 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 高铁酸钾(K2FeO4)是一种强氧化剂和环境友好型水处理剂,易分解,遇水和酸易变质。学习小组在实验室对高铁酸钾的制备和一些性质进行探究。
回答下列问题:
(1)高铁酸钾的制备。
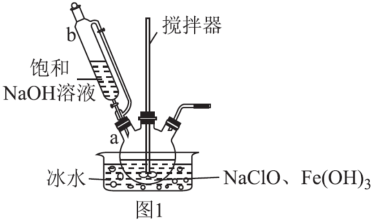
步骤一:制备Na2FeO4,装置如图1所示。将b中饱和NaOH溶液全部逐滴滴入a中,充分反应;
步骤二:由b向a中反应后液体中加入饱和KOH溶液;
步骤三:将a中所得浊液移出,分离提纯。
①仪器b的名称为___ ,其侧管的作用为___ 。
②步骤一中采用冰水浴冷却的目的为___ ;a中制备Na2FeO4反应的离子方程式为___ 。
③步骤二中,能得到K2FeO4悬浊液的原因为___ 。
④K2FeO4悬浊液经过滤、洗涤、提纯,可得产品。其中提纯所用的操作名称为___ 。
(2)K2FeO4遇水转化为Fe(OH)3,则其作水处理剂的优点为___ 。
(3)用图2所示装置检验K2FeO4受热分解的产物。
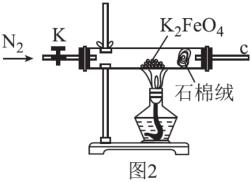
①检验分解的气体产物为O2的操作和现象为___ 。
②设计实验证明完全分解后的固体产物中不含Fe(Ⅱ)___ 。
回答下列问题:
(1)高铁酸钾的制备。
步骤一:制备Na2FeO4,装置如图1所示。将b中饱和NaOH溶液全部逐滴滴入a中,充分反应;

步骤二:由b向a中反应后液体中加入饱和KOH溶液;
步骤三:将a中所得浊液移出,分离提纯。
①仪器b的名称为
②步骤一中采用冰水浴冷却的目的为
③步骤二中,能得到K2FeO4悬浊液的原因为
④K2FeO4悬浊液经过滤、洗涤、提纯,可得产品。其中提纯所用的操作名称为
(2)K2FeO4遇水转化为Fe(OH)3,则其作水处理剂的优点为
(3)用图2所示装置检验K2FeO4受热分解的产物。

①检验分解的气体产物为O2的操作和现象为
②设计实验证明完全分解后的固体产物中不含Fe(Ⅱ)
您最近一年使用:0次
2021-08-28更新
|
551次组卷
|
4卷引用:山西省太原市第五十六中学2021-2022学年高三上学期第一次月考化学试题
山西省太原市第五十六中学2021-2022学年高三上学期第一次月考化学试题河南部分学校2022届新高三8月份摸底联考化学试题安徽省亳州市涡阳县育萃高级中学2021-2022学年高二上学期第一次月考化学试题(已下线)3.1.2 不同价态铁元素之间的转化-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)
7 . 化学上常用燃烧法确定有机物的组成。这种方法是在电炉里加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成。如图所列装置是用燃烧法确定有机物分子式常用的装置。
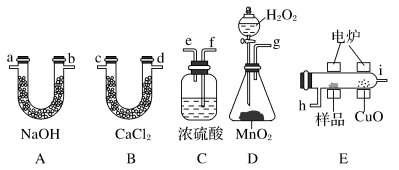
回答下列问题:
(1)产生的氧气按从左到右流向,所选装置各导管的连接顺序是__ 。
(2)C装置中浓H2SO4的作用是___ 。
(3)D装置中MnO2的作用是__ 。
(4)燃烧管中CuO的作用是___ 。
(5)若准确称取0.90g样品(只含C、H、O三种元素中的两种或三种),经充分燃烧后,A管质量增加1.32g,B管质量增加0.54g,则该有机物的最简式为___ 。
(6)要确定该有机物的分子式,还要___ 。

回答下列问题:
(1)产生的氧气按从左到右流向,所选装置各导管的连接顺序是
(2)C装置中浓H2SO4的作用是
(3)D装置中MnO2的作用是
(4)燃烧管中CuO的作用是
(5)若准确称取0.90g样品(只含C、H、O三种元素中的两种或三种),经充分燃烧后,A管质量增加1.32g,B管质量增加0.54g,则该有机物的最简式为
(6)要确定该有机物的分子式,还要
您最近一年使用:0次
2021-01-03更新
|
444次组卷
|
12卷引用:山西省朔州市怀仁县第一中学2018-2019学年高二下学期第二次月考化学试题
山西省朔州市怀仁县第一中学2018-2019学年高二下学期第二次月考化学试题(已下线)2011-2012年新疆乌鲁木齐市第八中学高一下学期期末考试化学卷2015-2016学年辽宁大连经济技术开发区得胜高中高二下期中化学试卷2018版化学(苏教版)高考总复习专题十二课时跟踪训练--认识有机化合物【全国百强校】辽宁省鞍山市第一中学2018-2019学年高二下学期开学考试化学试题3.2有机化合物结构的测定能力提升宁夏石嘴山市第三中学2019-2020学年高二10月月考化学试题天津市南开中学人教版高中化学选修5预习练习:第一章 第四节 研究有机化合物的一般步骤和方法 第2课时江西省南昌市新建区第二中学2020-2021学年高二上学期“新星计划”体验营10月考化学试题(已下线)1.4 研究有机化合物的一般步骤和方法(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版选修5)(已下线)1.2 研究有机化合物的一般方法(A级基础练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修3)(已下线)1.2.2 确定有机化合物的实验式与分子结构-2020-2021学年高二化学课时同步练(人教版2019选择性必修3)



