27. 科学家在利用碳水化合物消除污染气体和生成新能源方面取得重大成果。
(1)①甲醇是一种绿色可再生能源,在高效催化剂的作用下,CH
4可与NO
2反应,消除NO
2的污染,改善雾霾天气,发生的反应为:CH
4(g)+2NO
2(g)
⇌CO
2(g)+2H
2O(g)+N
2(g)
△H<0。该反应自发进行的条件为
_______(填高温、低温或任何条件)。在恒温恒容条件下,下列不能说明该反应达到平衡状态的是
_______(填序号)。
a.v
逆(NO
2)=v
正(H
2O)
b.混合气体的密度不再变化
c.混合气体的平均摩尔质量不再变化
d.单位时间内有4 mol C-H键断裂的同时有4 molO-H键形成
e.混合气体的压强不变
②如表是相同时间内处理NO
2的量与温度的关系,NO
2的处理量先增大后减小的原因是
_______。
| 温度/℃ | 100 | 200 | 300 | 400 | 500 |
| NO2的处理量/% | 39.3 | 70.4 | 85.6 | 75.7 | 50.5 |
(2)一定条件下,向2 L恒容密闭容器中通入4 mol CH
4、8 mol NO
2发生上述反应。测得反应过程中NO
2的体积分数在不同条件X下随着时间的变化如图1中曲线I、 曲线II所示:
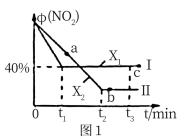
①若X表示温度,则X
1、X
2的相对大小是
_______,a、b、c三点对应的混合气体的平均相对分子质量的大小为
_______(用a、b、c表示)
②X
1条件下,在t
1~t
3 min内v(N
2)
_______(填“>”“<”或“=”)在t
2~ t
3 min内v(N
2),曲线I对应的反应的平衡常数K=
_______,(用分数表示)
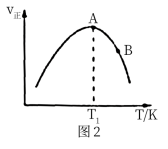
(3)欲研究在某催化剂作用下该反应的反应速率与温度的关系,在其他条件相同时,改变反应温度,测得经过相同时间时该反应的正反应速率如图2所示,A、B两点对应温度下正反应速率变化的原因可能是
_______。 A、B两点对应温度下该反应的活化能Ea(A)
_______Ea(B) (填“>”或“<”)。