1 . 氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示NaCl在水中溶解过程的微观状态示意图。___________ 。
a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.由上图可知,水分子在形成自由移动的Na+和Cl-中起到了至关重要的作用
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
(2)某同学用含钠元素的不同类别物质制备NaCl。化学反应方程式如下:
a.2Na + Cl2 2NaCl
2NaCl
b.NaOH + HCl = NaCl + H2O
c.Na2O + 2HCl = 2NaCl + H2O
d.___________。
① 反应d可为某物质与HCl反应来制得氯化钠,该物质的化学式为___________ 。
② 反应d也可为两种盐溶液相互反应获得氯化钠,该反应的化学方程式为___________ 。
③ 反应c中的原料Na2O的物质类别是碱性氧化物,请依据其类别通性,再列举2个能与Na2O反应的其他物质(用化学式表示)___________ 。
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO 等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
(3)①过滤操作中所用到的玻璃仪器有烧杯、漏斗和___________ 。
②用离子方程式表示加入过量Na2CO3溶液的作用Ca2++CO =CaCO3↓和
=CaCO3↓和___________ 。
③ 用离子方程式表示盐酸的作用H+ + OH-=H2O 和___________ 。
Ⅰ.实验室研究氯化钠的性质及制备
(1)下图表示NaCl在水中溶解过程的微观状态示意图。

a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.由上图可知,水分子在形成自由移动的Na+和Cl-中起到了至关重要的作用
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
(2)某同学用含钠元素的不同类别物质制备NaCl。化学反应方程式如下:
a.2Na + Cl2
 2NaCl
2NaCl b.NaOH + HCl = NaCl + H2O
c.Na2O + 2HCl = 2NaCl + H2O
d.___________。
① 反应d可为某物质与HCl反应来制得氯化钠,该物质的化学式为
② 反应d也可为两种盐溶液相互反应获得氯化钠,该反应的化学方程式为
③ 反应c中的原料Na2O的物质类别是碱性氧化物,请依据其类别通性,再列举2个能与Na2O反应的其他物质(用化学式表示)
Ⅱ.工业生产中氯化钠的制备
我国食盐的来源主要为海盐、湖盐、井矿盐。粗食盐中除了含泥沙等难溶性杂质外,还含有Ca2+、Mg2+、SO
 等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。
等可溶性杂质。为得到精制食盐,某同学设计如下除杂流程,向粗盐中依次加入:过量BaCl2溶液、过量Na2CO3溶液、过量NaOH溶液,然后过滤,再在滤液中加入适量盐酸后加热蒸发结晶得纯净的NaCl。(3)①过滤操作中所用到的玻璃仪器有烧杯、漏斗和
②用离子方程式表示加入过量Na2CO3溶液的作用Ca2++CO
 =CaCO3↓和
=CaCO3↓和③ 用离子方程式表示盐酸的作用H+ + OH-=H2O 和
您最近一年使用:0次
2 . Ⅰ.下面两个方法都可以用来制氯气:①MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O;②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。③4HCl+O2
MnCl2+Cl2↑+2H2O;②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。③4HCl+O2 2Cl2+2H2O(g),根据以上两个反应,回答下列问题:
2Cl2+2H2O(g),根据以上两个反应,回答下列问题:
(1)反应①的离子方程式为___________ 。
(2)浓盐酸在反应①中表现出来的性质是___________。
(3)若要制得相同质量的氯气,反应①②所消耗的HCl的质量之比为___________ 。
(4)由上述3个反应发生的条件可推知MnO2、KMnO4、O2三种物质氧化性由强到弱的顺序为___________ 。
Ⅱ.某同学欲利用浓盐酸、MnO2、Fe等试剂制取无水氯化铁、收集一定量的氯气并验证其某些性质,实验装置如图所示(制气装置省略)。___________ (填名称)。
(6)装置③中现象是___________ ,装置④中有一处错误,更正为___________ 。
(7)装置⑦是用于氯气的尾气处理,防止污染空气,发生反应的化学方程式为___________ 。
 MnCl2+Cl2↑+2H2O;②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。③4HCl+O2
MnCl2+Cl2↑+2H2O;②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。③4HCl+O2 2Cl2+2H2O(g),根据以上两个反应,回答下列问题:
2Cl2+2H2O(g),根据以上两个反应,回答下列问题:(1)反应①的离子方程式为
(2)浓盐酸在反应①中表现出来的性质是___________。
| A.只有还原性 | B.只有氧化性 | C.只有酸性 | D.既表还原性和又表酸性 |
(3)若要制得相同质量的氯气,反应①②所消耗的HCl的质量之比为
(4)由上述3个反应发生的条件可推知MnO2、KMnO4、O2三种物质氧化性由强到弱的顺序为
Ⅱ.某同学欲利用浓盐酸、MnO2、Fe等试剂制取无水氯化铁、收集一定量的氯气并验证其某些性质,实验装置如图所示(制气装置省略)。
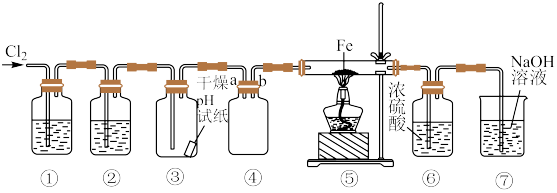
(6)装置③中现象是
(7)装置⑦是用于氯气的尾气处理,防止污染空气,发生反应的化学方程式为
您最近一年使用:0次
3 . A和B两支试管所盛的溶液中共含有K+、Ag+、Mg2+、Cl−、OH−、 六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:
六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:
(1)若向某试管中滴入稀盐酸产生沉淀,则该试管为___________ (填“A”或“B”)。
(2)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是___________ (填化学式)。
(3)若将试管A和试管B中的溶液按一定体积比混合后过滤,蒸干所得滤液可得到一种纯净物,该物质为___________ ( 写化学式),则混合过程中发生反应的离子方程式为Ag++Cl-=AgCl↓与___________ (不考虑Ag+与OH−的反应)。
(4)按如图所示操作,充分反应后:___________ 。
②结合Ⅰ、Ⅱ实验现象可知 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为___________ 。
(5)已知 可发生反应:
可发生反应:
①该反应中氧化剂是___________ (填化学式)。
②用双线桥法标出电子转移的数目和方向:___________ 。
 六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:
六种离子,向试管A的溶液中滴入酚酞溶液,溶液呈红色。请回答下列问题:(1)若向某试管中滴入稀盐酸产生沉淀,则该试管为
(2)若向试管B的溶液中加入合适的药品,过滤后可以得到相应的金属和仅含一种溶质的溶液,则加入的药品是
(3)若将试管A和试管B中的溶液按一定体积比混合后过滤,蒸干所得滤液可得到一种纯净物,该物质为
(4)按如图所示操作,充分反应后:
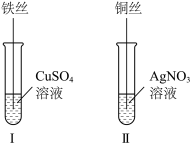
②结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(5)已知
 可发生反应:
可发生反应:
①该反应中氧化剂是
②用双线桥法标出电子转移的数目和方向:
您最近一年使用:0次
4 . 研究物质性质及物质转化具有重要的价值,根据所学知识回答下列问题:
(1)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示置换反应的是___________ (填字母)。
①下列应用或事实与胶体的性质有关系的是___________ 。
A.在 溶液中滴加
溶液中滴加 溶液出现红褐色沉淀
溶液出现红褐色沉淀
B.在河流入海处易形成三角洲
C.用石膏或盐卤点制豆腐
②提纯明胶的水溶液和 溶液装置是下列中的
溶液装置是下列中的___________ (填序号)。___________ (填化学式),若该反应生成标准状况下的气体为8.96L,则该反应中转移电子的数目为___________ 。
(4)中国古代著作中有“银针验毒”的记录,其原理为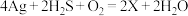 ,则X的化学式是
,则X的化学式是___________ ,其中 在该反应中
在该反应中___________ (填标号)。
A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(1)下图为离子反应、氧化还原反应和置换反应三者之间的关系,其中表示置换反应的是

①下列应用或事实与胶体的性质有关系的是
A.在
 溶液中滴加
溶液中滴加 溶液出现红褐色沉淀
溶液出现红褐色沉淀B.在河流入海处易形成三角洲
C.用石膏或盐卤点制豆腐
②提纯明胶的水溶液和
 溶液装置是下列中的
溶液装置是下列中的A. B.
B. 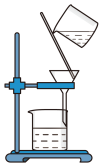 C.
C.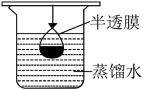
(4)中国古代著作中有“银针验毒”的记录,其原理为
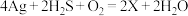 ,则X的化学式是
,则X的化学式是 在该反应中
在该反应中A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
您最近一年使用:0次
5 . 某温度下将氯气通入过量KOH溶液中,反应后得到KCl、KClO和KClO3的混合溶液,若所得溶液中ClO-和ClO 的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为
的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为
 的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为
的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为| A.3:7 | B.7:3 | C.1:1 | D.3:11 |
您最近一年使用:0次
6 . 下列反应的离子方程式或电离方程式正确的是
A.氧化铜与稀硫酸反应: |
B.向 NaHSO4溶液中滴加 Ba(OH)2溶液至SO 恰好沉淀完全: 恰好沉淀完全: |
C.盐酸和足量碳酸钠反应:  |
D.硫酸氢钠溶于水的电离方程式: |
您最近一年使用:0次
7 . 下列物质的分类正确的是
| 选项 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| A | Na2CO3 | H2SO4 | CaCl2 | MgO | CO2 |
| B | NaOH | HCl | NaCl | Na2O | NO |
| C | KOH | HNO3 | CaCO3 | CaO | Mn2O7 |
| D | NaOH | HCl | CuSO4 | Na2O2 | SO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 用NA表示阿伏加德罗常数的值,下列叙述中正确的是
| A.0.1molH2SO4溶于水电离出的离子数0.7NA |
B.1molCH (碳正离子)中含有电子数为10NA (碳正离子)中含有电子数为10NA |
| C.27g金属铝与足量的盐酸反应,铝失去电子数为3NA |
| D.标准状况下,23g乙醇的体积为11.2L |
您最近一年使用:0次
9 . 同温同压下,同质量的下列气体充入气球中,气球体积最大的是
| A.CO2 | B.H2 | C.Cl2 | D.CH4 |
您最近一年使用:0次
解题方法
10 . 下列关于钠及其化合物的说法正确的是
| A.过量的Na2O2投入滴有酚酞的水中,溶液最终呈红色 |
| B.钠着火后,可用泡沫灭火器灭火 |
| C.Na2CO3可用于治疗胃酸过多 |
| D.钠与硫酸铜溶液反应时,有蓝色沉淀生成同时产生气体 |
您最近一年使用:0次



