名校
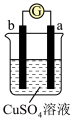
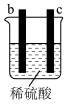
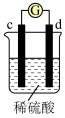
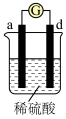
1 . 有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
由此可判断这四种金属的活动性顺序是
| 实验装置 |
|
|
| 部分实验现象 | a极质量减小,b极质量增加 | b极有气体产生,c极无变化 |
| 实验装置 |
|
|
| 部分实验现象 | d极溶解,c极有气体产生 | 电流计指示在导线中电流从a极流向d极 |
A. | B. |
C. | D. |
您最近一年使用:0次
2024-04-21更新
|
188次组卷
|
5卷引用:湖南省邵东市第一中学2022-2023学年高一上学期期末测试化学试题
湖南省邵东市第一中学2022-2023学年高一上学期期末测试化学试题宁夏石嘴山市第三中学2023-2024学年高一下学期3月月考化学试题河南省信阳高级中学2023-2024学年高一下学期4月月考化学试题(已下线)专题02 化学反应与能量变化-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)广西来宾市忻城县高级中学2023-2024学年高一下学期期中考试化学试卷
名校
解题方法
2 . 为测定 溶液的浓度,进行如下实验:用标准稀盐酸溶液进行滴定。
溶液的浓度,进行如下实验:用标准稀盐酸溶液进行滴定。
(1)配制
 盐酸标准溶液所需仪器除量筒、小烧杯、玻璃棒、胶头滴管外,还需要
盐酸标准溶液所需仪器除量筒、小烧杯、玻璃棒、胶头滴管外,还需要______ 。
(2)用______ 量取 待测
待测 溶液放入锥形瓶中,滴加2~3滴酚酞作指示剂,用标准盐酸溶液进行滴定。为减小实验误差,进行了三次实验,假设每次所取
溶液放入锥形瓶中,滴加2~3滴酚酞作指示剂,用标准盐酸溶液进行滴定。为减小实验误差,进行了三次实验,假设每次所取 溶液体积均为
溶液体积均为 ,三次实验结果如下:
,三次实验结果如下:
该 溶液的浓度约为
溶液的浓度约为______ 。
(3)滴定时边滴边摇动锥形瓶,眼睛______ 。判断到达滴定终点的实验现象是:滴加最后半滴标准液,溶液由______ ,且半分钟内不变色。
(4)下列操作会造成测定结果(待测 溶液浓度值)偏低的有
溶液浓度值)偏低的有______ 。
A.配制标准溶液定容时,加水超过刻度
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用标准稀盐酸溶液润洗
D.滴定到达终点时,俯视读出滴定管读数
E.摇动锥形瓶时有少量液体溅出瓶外
(5)中和滴定的装置和相似操作可用来做其它实验,如据反应 ,可以用碘水滴定
,可以用碘水滴定 溶液,应选
溶液,应选______ 作指示剂;据反应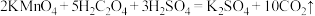
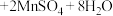 可以用酸性
可以用酸性 溶液滴定
溶液滴定 溶液,
溶液, 溶液应装在
溶液应装在______ 滴定管中(填写“酸式”或者“碱式”)。
 溶液的浓度,进行如下实验:用标准稀盐酸溶液进行滴定。
溶液的浓度,进行如下实验:用标准稀盐酸溶液进行滴定。(1)配制

 盐酸标准溶液所需仪器除量筒、小烧杯、玻璃棒、胶头滴管外,还需要
盐酸标准溶液所需仪器除量筒、小烧杯、玻璃棒、胶头滴管外,还需要(2)用
 待测
待测 溶液放入锥形瓶中,滴加2~3滴酚酞作指示剂,用标准盐酸溶液进行滴定。为减小实验误差,进行了三次实验,假设每次所取
溶液放入锥形瓶中,滴加2~3滴酚酞作指示剂,用标准盐酸溶液进行滴定。为减小实验误差,进行了三次实验,假设每次所取 溶液体积均为
溶液体积均为 ,三次实验结果如下:
,三次实验结果如下:| 实验次数 | 第一次 | 第二次 | 第三次 |
消耗盐酸溶液体积 | 19.00 | 23.00 | 23.04 |
 溶液的浓度约为
溶液的浓度约为(3)滴定时边滴边摇动锥形瓶,眼睛
(4)下列操作会造成测定结果(待测
 溶液浓度值)偏低的有
溶液浓度值)偏低的有A.配制标准溶液定容时,加水超过刻度
B.锥形瓶水洗后直接装待测液
C.酸式滴定管水洗后未用标准稀盐酸溶液润洗
D.滴定到达终点时,俯视读出滴定管读数
E.摇动锥形瓶时有少量液体溅出瓶外
(5)中和滴定的装置和相似操作可用来做其它实验,如据反应
 ,可以用碘水滴定
,可以用碘水滴定 溶液,应选
溶液,应选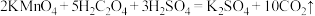
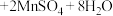 可以用酸性
可以用酸性 溶液滴定
溶液滴定 溶液,
溶液, 溶液应装在
溶液应装在
您最近一年使用:0次
解题方法
3 . 某离子反应涉及H2O、ClO-、 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
 、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是
、OH-、N2、Cl-等微粒,其中N2、ClO-的数目随时间变化的曲线如图所示,下列说法正确的是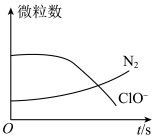
| A.该反应中Cl-为氧化产物 | B.消耗1mol还原剂微粒,转移6mol电子 |
C. 被ClO-氧化成N2 被ClO-氧化成N2 | D.该反应为非氧化还原反应 |
您最近一年使用:0次
2024-04-05更新
|
61次组卷
|
2卷引用:湖南省邵阳市新邵县第三中学2023-2024学年高一上学期期中考试化学试题
名校
4 . 氨能与 形成配合物
形成配合物 和
和 ,该反应在生产和生活中发挥着重要的作用。
,该反应在生产和生活中发挥着重要的作用。
(1)基态 原子价层电子的轨道表示式为
原子价层电子的轨道表示式为_______ , 中
中 与
与 间形成的化学键为
间形成的化学键为_______ 。
(2)将 置于
置于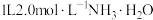 溶液中,通入
溶液中,通入 ,
, 转化为
转化为 的离子方程式为:
的离子方程式为:
_______ 
_______ 。反应1小时测得溶液中银的总浓度为 ,
, 的溶解速率为
的溶解速率为_______ 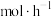 。
。
(3)氨与 形成配合物有助于
形成配合物有助于 溶解。常温下,向
溶解。常温下,向 饱和溶液(含足量
饱和溶液(含足量 固体)中滴加氨水,主要存在以下平衡:
固体)中滴加氨水,主要存在以下平衡:
(i)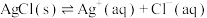
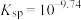
(ii)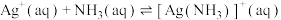
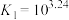
(iii)
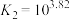
①下列有关说法中,正确的有_______ (填编号)。
A.加少量水稀释,平衡后溶液中 、
、 均减小
均减小
B.随 增大,反应ⅱ平衡正向移动,
增大,反应ⅱ平衡正向移动, 增大
增大
C.随 增大,
增大, 不变
不变
D.溶液中存在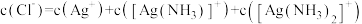
②反应

_______ (用 、
、 、
、 表示)。
表示)。
(4)向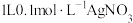 溶液中通入足量
溶液中通入足量 得到澄清溶液(设溶液体积不变),溶液中
得到澄清溶液(设溶液体积不变),溶液中 、
、 、
、 的物质的量分数
的物质的量分数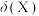 随
随 的变化如图所示。
的变化如图所示。
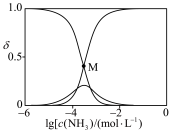
已知溶液中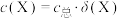 ,
, 。
。
① 点溶液中
点溶液中
_______  。
。
②计算 点溶液中
点溶液中 的转化率
的转化率________ (写出计算过程,已知 )。
)。
 形成配合物
形成配合物 和
和 ,该反应在生产和生活中发挥着重要的作用。
,该反应在生产和生活中发挥着重要的作用。(1)基态
 原子价层电子的轨道表示式为
原子价层电子的轨道表示式为 中
中 与
与 间形成的化学键为
间形成的化学键为(2)将
 置于
置于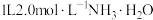 溶液中,通入
溶液中,通入 ,
, 转化为
转化为 的离子方程式为:
的离子方程式为:

 ,
, 的溶解速率为
的溶解速率为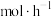 。
。(3)氨与
 形成配合物有助于
形成配合物有助于 溶解。常温下,向
溶解。常温下,向 饱和溶液(含足量
饱和溶液(含足量 固体)中滴加氨水,主要存在以下平衡:
固体)中滴加氨水,主要存在以下平衡:(i)
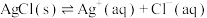
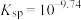
(ii)
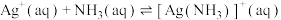
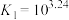
(iii)

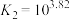
①下列有关说法中,正确的有
A.加少量水稀释,平衡后溶液中
 、
、 均减小
均减小B.随
 增大,反应ⅱ平衡正向移动,
增大,反应ⅱ平衡正向移动, 增大
增大C.随
 增大,
增大, 不变
不变D.溶液中存在
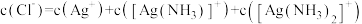
②反应


 、
、 、
、 表示)。
表示)。(4)向
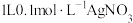 溶液中通入足量
溶液中通入足量 得到澄清溶液(设溶液体积不变),溶液中
得到澄清溶液(设溶液体积不变),溶液中 、
、 、
、 的物质的量分数
的物质的量分数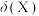 随
随 的变化如图所示。
的变化如图所示。
已知溶液中
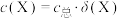 ,
, 。
。①
 点溶液中
点溶液中
 。
。②计算
 点溶液中
点溶液中 的转化率
的转化率 )。
)。
您最近一年使用:0次
2024-04-03更新
|
862次组卷
|
2卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期中测试化学试题
名校
解题方法
5 . 除去粗盐中的Ca2+、Mg2+、 及泥沙,可先将粗盐溶于水,然后进行下列操作:
及泥沙,可先将粗盐溶于水,然后进行下列操作:
①过滤②加过量的NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。正确的操作顺序是
 及泥沙,可先将粗盐溶于水,然后进行下列操作:
及泥沙,可先将粗盐溶于水,然后进行下列操作:①过滤②加过量的NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。正确的操作顺序是
| A.①④②⑤③ | B.④①②⑤③ | C.②④⑤①③ | D.⑤②④①③ |
您最近一年使用:0次
2024-03-30更新
|
187次组卷
|
64卷引用:湖南省岳阳市2022-2023学年高一上学期第一次月考化学试题
湖南省岳阳市2022-2023学年高一上学期第一次月考化学试题2015-2016学年陕西省城固一中高一上学期期中测试化学试卷山东省昌邑市第一中学2017-2018学年高一上学期期末模拟化学试题吉林省长春外国语学校2017-2018学年高一上学期期末考试化学(文)试题北京市首师附2019-2020学年第一学期期中考试高一化学试卷四川省自贡市田家炳中学2019-2020学年高一上学期期中考试化学试题天津市静海县第一中学2019-2020学年高一3月学生学业能力调研考试化学试题四川省江油中学2018-2019学年高一10月月考化学试题内蒙古北京八中乌兰察布分校2020-2021学年高一上学期第一次月考化学试题北京交通大学附属中学2020-2021学年高一上学期期中考试化学试题宁夏吴忠市吴忠中学2020-2021学年高一上学期期中考试化学试题四川省成都市实验外国语学校(西区)2020-2021学年高一上学期期中考试化学试题山东省日照市莒县2020-2021学年高一11月模块考试化学试题辽宁省抚顺县高级中学2019-2020学年高一下学期期中网课学习质量检测化学试题黑龙江省大庆实验中学2020-2021学年高一上学期第一次线上教学质量检测(1月)化学试题合肥市第十一中学2020-2021学年高一下学期第一次教学质量评估化学试题贵州省毕节市民族中学2020-2021学年高一上学期12月月考化学试题广东省中山市第二中学2020-2021学年高一下学期第一次段考化学试题黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高一4月月考化学试题湖北省黄冈市麻城市麻城二中2020-2021学年高一下学期期中考试化学试题山西省大同市天镇县实验中学2020-2021学年高一下学期期中考试化学试题河北省师范大学附属中学2020-2021学年高一第二学期期中考试化学试题(已下线)专题01 硫及其化合物【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)北京市大兴区2020-2021学年高一下学期期末考试化学试题吉林省白城市第一中学2020-2021学年高一下学期期中考试化学试题内蒙古集宁新世纪中学2020-2021学年高一上学期期中考试化学试题重庆铁路中学2020-2021学年高一下学期4月月考化学试题广东省2012年全国高中学生化学素质和实验能力竞赛初赛试题(B组)吉林省长春市2020-2021学年高一下学期期末联考化学试题(已下线)3.3.1 粗盐提纯 从海水中提取溴(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)宁夏中卫市第一中学2021-2022学年高一上学期第一次月考化学试题安徽省合肥市第六中学2021-2022学年高一上学期第一次月考化学试题浙江省绍兴市诸暨中学2021-2022学年高一上学期期中考试(实验班)化学试题甘肃省永昌县第一高级中学2020-2021学年高一上学期期中考试化学试题黑龙江省哈尔滨市第一六二中学2021-2022学年高一上学期期末考试化学试题安徽省蚌埠市2021-2022学年高一上学期期末学业水平测试化学试题云南省宣威市第三中学2021-2022学年高一下学期4月考试化学试题云南省昆明市云南师范大学附属中学2021-2022学年高一下学期期中考试化学试题山东省临沂市2021-2022学年高一下学期期中考试化学试题广东省深圳市福田区外国语高级中学2021-2022学年高一下学期期中考试(选择考)化学试题江苏省天一中学2021-2022学年高一下学期期中考试(文)化学试题北京市东直门中学2021—2022学年高一下学期6月月考化学试题四川省什邡中学2021-2022学年高一上学期第一次月考化学试题云南红河县第一中学2021-2022学年高一下学期期末考试化学试题云南省昆明北大博雅实验中学2020-2021学年高一下学期期中考试化学试题吉林省洮南市第一中学2021-2022学年高一下学期第一次月考化学试题云南省红河县第一中学2020-2021学年高一下学期期末考试化学试题黑龙江省双鸭山市第一中学2022-2023学年高一下学期4月月考(普通班)化学试题辽宁省鞍山市普通高中2022-2023学年高一下学期期中考试化学(A卷)试题广东省广州大同中学2022-2023学年高一下学期期中考试化学试题广东省江门市新会陈经纶中学2022-2023学年高一下学期期中考试(合格考)化学试题安徽省六安第二中学2022-2023学年高一下学期期中考试化学试题山西省阳泉市2022-2023学年高一下学期期末考试化学试题陕西省武功县普集高级中学2022-2023学年高一下学期3月月考化学试题广东省佛山市三水中学2022-2023学年高一下学期3月第一次统测化学试题黑龙江省哈尔滨市第四中学校2023-2024学年高一上学期11月月考化学试题 新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高一上学期10月第一次月考化学试卷河北省邯郸市永年区第二中学2023-2024学年高一上学期12月月考化学试题广东省深圳市光明中学2023-2024学年高一下学期3月第一次统测化学试题广东省江门市某校2023-2024学年高一下学期第一次质量检测化学试题安徽省蚌埠市固镇县汉兴学校、怀远县禹泽学校2023-2024学年高一上学期12月期末联考化学试题云南省昆明市禄劝彝族苗族自治县第一中学2023-2024学年高一下学期3月月考化学试题四川省华蓥中学2023-2024学年高一下学期4月月考化学试题广东省深圳市龙岗区平湖外国语学校2023-2024学年高一下学期期中考试化学试卷
6 . 2022年度诺贝尔化学奖授与了点击反应。K。B.Sharpless教授发现,在亚铜的催化下,末端炔烃可以高区域选择性地与叠氮化合物发生高效的点击反应,这一反应目前已经应用于生物化学等交叉领域。点击反应代表性示例如下:
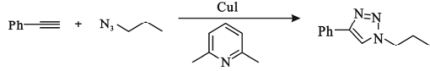 (Ph-:苯基)
(Ph-:苯基)
科学家以环己醇为原料,经过多步转化和点击反应合成化合物G,请按要求回答下面的问题。
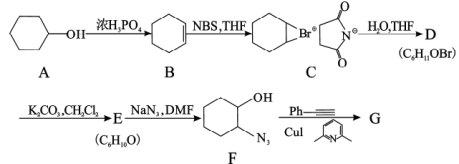
(1)有机物A转化为有机物B的反应类型为___________ ;浓硫酸也可用作该转化的催化剂,此处转化不使用浓硫酸作催化剂,其原因有___________ 。
(2)有机物C经水解反应开环后得到有机物D,有机物D的结构简式为___________ 。
(3)有机物E为双环化合物,其所含官能团的名称为___________ 。
(4)叠氮酸根( )的结构可表示为:
)的结构可表示为: ;其中心原子N的杂化类型为
;其中心原子N的杂化类型为___________ 。
(5)有机物F转化为有机物G的反应方程式为___________ 。
(6)满足下列条件的有机物A的同分异构体有___________ 种(不考虑立体异构)。
条件1:含一个五元环;
条件2:含有两个手性碳原子。
(7)根据点击反应信息和相关知识,设计以苯乙烯和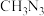 为原料合成
为原料合成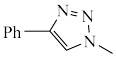 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)___________ 。
 (Ph-:苯基)
(Ph-:苯基)科学家以环己醇为原料,经过多步转化和点击反应合成化合物G,请按要求回答下面的问题。

(1)有机物A转化为有机物B的反应类型为
(2)有机物C经水解反应开环后得到有机物D,有机物D的结构简式为
(3)有机物E为双环化合物,其所含官能团的名称为
(4)叠氮酸根(
 )的结构可表示为:
)的结构可表示为: ;其中心原子N的杂化类型为
;其中心原子N的杂化类型为(5)有机物F转化为有机物G的反应方程式为
(6)满足下列条件的有机物A的同分异构体有
条件1:含一个五元环;
条件2:含有两个手性碳原子。
(7)根据点击反应信息和相关知识,设计以苯乙烯和
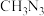 为原料合成
为原料合成 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)
您最近一年使用:0次
解题方法
7 . 研究碳、硫、氮的化合物间的反应,对实现“绿色环保”的目标具有重要的意义。
(1)现向一恒容密闭容器中充入 ,一段时间后对容器中的成分进行定量分析,其组分如下表:
,一段时间后对容器中的成分进行定量分析,其组分如下表:
上述物质之间发生反应的热化学方程式如下:
反应I: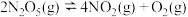
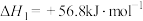
反应Ⅱ: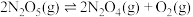
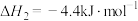
反应Ⅲ:


_______  ;该体系中
;该体系中_______ (填“吸收”或“放出”)_______ kJ能量。
(2)燃料不完全燃烧生成的炭黑小颗粒在催化剂存在下可将尾气中的NO还原为无害气体: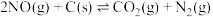
 ,该反应在恒温恒容条件下达到平衡后,下列有关叙述正确的是
,该反应在恒温恒容条件下达到平衡后,下列有关叙述正确的是_______ (填序号)。
①该方法使用的催化剂对反应体系中活化分子百分数没有影响
②若向体系中充入少量的NO气体,NO的平衡转化率不变
③当体系中压强不再变化时,反应达到平衡状态
④当体系中混合气体的密度不变时,反应达到平衡状态
(3)已知在气缸中还发生了如下反应:
反应Ⅳ:
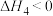
反应V: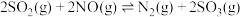
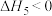
现向某密闭容器中均充入等物质的量的 和
和 ,在恒温恒容条件下测得气体的压强与时间的关系如图所示:
,在恒温恒容条件下测得气体的压强与时间的关系如图所示:
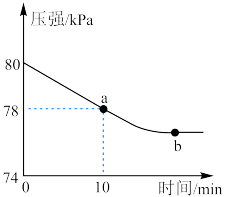
已知a点时 的转化率为50%,则:
的转化率为50%,则:
①a点时 的分压为
的分压为_______ kPa,0~10min内 的平均反应速率为
的平均反应速率为_______  。
。
②b点反应Ⅳ的平衡常数 的范围为
的范围为_______ ( 为用分压计算的平衡常数,分压=总压×物质的量分数)。
为用分压计算的平衡常数,分压=总压×物质的量分数)。
(1)现向一恒容密闭容器中充入
 ,一段时间后对容器中的成分进行定量分析,其组分如下表:
,一段时间后对容器中的成分进行定量分析,其组分如下表:| 气体组分 |  |  |  |  |
| 物质的量/mol | 0.2 | 0.5 | 0.6 | 0.4 |
反应I:
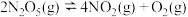
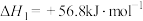
反应Ⅱ:
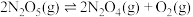
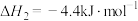
反应Ⅲ:



 ;该体系中
;该体系中(2)燃料不完全燃烧生成的炭黑小颗粒在催化剂存在下可将尾气中的NO还原为无害气体:
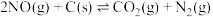
 ,该反应在恒温恒容条件下达到平衡后,下列有关叙述正确的是
,该反应在恒温恒容条件下达到平衡后,下列有关叙述正确的是①该方法使用的催化剂对反应体系中活化分子百分数没有影响
②若向体系中充入少量的NO气体,NO的平衡转化率不变
③当体系中压强不再变化时,反应达到平衡状态
④当体系中混合气体的密度不变时,反应达到平衡状态
(3)已知在气缸中还发生了如下反应:
反应Ⅳ:

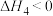
反应V:
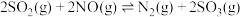
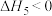
现向某密闭容器中均充入等物质的量的
 和
和 ,在恒温恒容条件下测得气体的压强与时间的关系如图所示:
,在恒温恒容条件下测得气体的压强与时间的关系如图所示:
已知a点时
 的转化率为50%,则:
的转化率为50%,则:①a点时
 的分压为
的分压为 的平均反应速率为
的平均反应速率为 。
。②b点反应Ⅳ的平衡常数
 的范围为
的范围为 为用分压计算的平衡常数,分压=总压×物质的量分数)。
为用分压计算的平衡常数,分压=总压×物质的量分数)。
您最近一年使用:0次
2024-03-18更新
|
41次组卷
|
2卷引用:湖南省岳阳市湘阴县知源高级中学等多校2023-2024学年高三上学期11月月考化学试题
名校
8 . 氢能是最具应用前景的绿色能源,下列反应是目前大规模制取氢气的方法之一: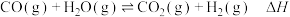
回答下列问题:
已知:①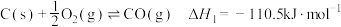 ;
;
②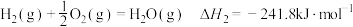 ;
;
③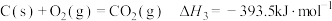 。
。
(1)
___________ 。
(2)实验发现,830℃时(其他条件相同),相同时间内,向上述体系中投入一定量的 可以提高
可以提高 的百分含量。做对比实验,结果如图所示:
的百分含量。做对比实验,结果如图所示:

分析无 、投入微米
、投入微米 、投入纳米
、投入纳米 ,
, 百分含量不同的原因是
百分含量不同的原因是___________ 。
(3)在 时,将
时,将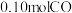 与
与 充入
充入 的恒容密闭容器中,反应达到平衡时,
的恒容密闭容器中,反应达到平衡时, 的物质的量分数
的物质的量分数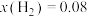 。
。
① 的平衡转化率
的平衡转化率
___________ %; 时,反应平衡常数
时,反应平衡常数
___________ (保留2位有效数字)。
②由 时上述实验数据计算得到
时上述实验数据计算得到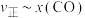 和
和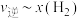 的关系如图1所示。若升高温度,反应重新达到平衡,则
的关系如图1所示。若升高温度,反应重新达到平衡,则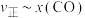 相应的点变为
相应的点变为___________ 、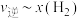 相应的点变为
相应的点变为___________ (填图中字母)。
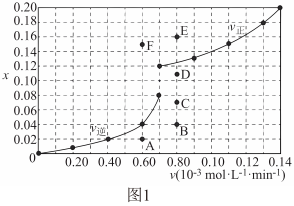
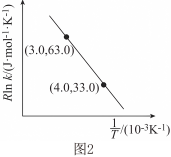
(4)反应 的Arrhenius经验公式的实验数据如图2中曲线所示,已知经验公式为
的Arrhenius经验公式的实验数据如图2中曲线所示,已知经验公式为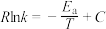 (其中
(其中 为活化能,
为活化能, 为速率常数,
为速率常数, 和
和 为常数)。该反应的活化能
为常数)。该反应的活化能
___________  。
。
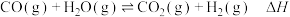
回答下列问题:
已知:①
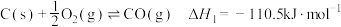 ;
;②
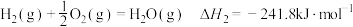 ;
;③
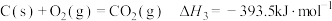 。
。(1)

(2)实验发现,830℃时(其他条件相同),相同时间内,向上述体系中投入一定量的
 可以提高
可以提高 的百分含量。做对比实验,结果如图所示:
的百分含量。做对比实验,结果如图所示:
分析无
 、投入微米
、投入微米 、投入纳米
、投入纳米 ,
, 百分含量不同的原因是
百分含量不同的原因是(3)在
 时,将
时,将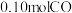 与
与 充入
充入 的恒容密闭容器中,反应达到平衡时,
的恒容密闭容器中,反应达到平衡时, 的物质的量分数
的物质的量分数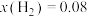 。
。①
 的平衡转化率
的平衡转化率
 时,反应平衡常数
时,反应平衡常数
②由
 时上述实验数据计算得到
时上述实验数据计算得到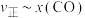 和
和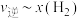 的关系如图1所示。若升高温度,反应重新达到平衡,则
的关系如图1所示。若升高温度,反应重新达到平衡,则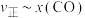 相应的点变为
相应的点变为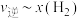 相应的点变为
相应的点变为
(4)反应
 的Arrhenius经验公式的实验数据如图2中曲线所示,已知经验公式为
的Arrhenius经验公式的实验数据如图2中曲线所示,已知经验公式为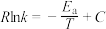 (其中
(其中 为活化能,
为活化能, 为速率常数,
为速率常数, 和
和 为常数)。该反应的活化能
为常数)。该反应的活化能
 。
。
您最近一年使用:0次
名校
9 . 探究铜和浓硫酸的反应,下列装置或操作错误的是
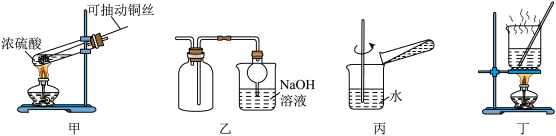
| A.上下移动装置甲中的铜丝体现绿色化学的思想 |
| B.装置乙可用于收集SO2气体 |
| C.将试管中的液体倒入装置丙中稀释,观察颜色可确定CuSO4的生成 |
| D.利用装置丁将硫酸铜溶液加热浓缩、冷却结晶,可析出CuSO4∙5H2O |
您最近一年使用:0次
2024-02-27更新
|
1102次组卷
|
15卷引用:湖南省长沙市明德中学2022-2023学年高一下学期5月月考化学试题
湖南省长沙市明德中学2022-2023学年高一下学期5月月考化学试题2016届山东省临沂市高三上学期期中考试化学试卷辽宁省本溪市2019-2020学年高一下学期寒假验收考试化学试题(已下线)第15讲 硫及其化合物(精讲)——2021年高考化学一轮复习讲练测人教版2019必修第二册 第五章 第一节 第2课时 硫酸 硫酸根离子的检验广东省东莞市第五高级中学2020-2021学年高一下学期期中考试化学试题广东省汕头市东方中学2020-2021学年高一下学期期中考试化学试题河北省邢台市名校联盟2022-2023学年高一下学期3月月考化学试题(已下线)山东省青岛市2023届高三下学期一模化学试题变式题(选择题6-10)四川省成都市郫都区2022-2023学年高一下学期4月期中化学试题第五章 化工生产中的重要非金属元素(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)(已下线)专题突破卷04?非金属及其化合物?-2024年高考化学一轮复习考点通关卷(新教材新高考)(已下线)考点巩固卷04 非金属及其化合物(4大考点60题)?-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)第五章 化工生产中的重要非金属元素【单元测试A卷】江西省宜春市丰城市第九中学2023-2024学年高一下学期期中考试化学试题
名校
解题方法
10 . 甲烷化反应即为氢气和碳氧化物反应生成甲烷,有利于实现碳循环利用。已知涉及的反应如下:
反应Ⅰ: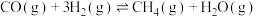 ∆H1<0
∆H1<0
反应Ⅱ: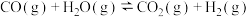 ∆H2<0
∆H2<0
在360℃时,在固定容积的容器中进行上述反应,平衡时CO和H2的转化率及CH4和 CO2的产率随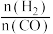 变化的情况如图所示。若按
变化的情况如图所示。若按  向恒容容器内投料,初始压强为 p₀[已知:①CH,的选择性=
向恒容容器内投料,初始压强为 p₀[已知:①CH,的选择性= 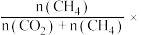 100%;②平衡常数用分压表示,分压=总压×物质的量分数]。 下列说法错误的是
100%;②平衡常数用分压表示,分压=总压×物质的量分数]。 下列说法错误的是

反应Ⅰ:
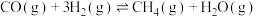 ∆H1<0
∆H1<0反应Ⅱ:
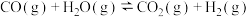 ∆H2<0
∆H2<0在360℃时,在固定容积的容器中进行上述反应,平衡时CO和H2的转化率及CH4和 CO2的产率随
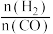 变化的情况如图所示。若按
变化的情况如图所示。若按  向恒容容器内投料,初始压强为 p₀[已知:①CH,的选择性=
向恒容容器内投料,初始压强为 p₀[已知:①CH,的选择性= 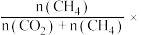 100%;②平衡常数用分压表示,分压=总压×物质的量分数]。 下列说法错误的是
100%;②平衡常数用分压表示,分压=总压×物质的量分数]。 下列说法错误的是
A.图中表示CO转化率变化的曲线是 b, 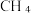 产率变化的曲线是c 产率变化的曲线是c |
B.点 C 通过改变温度达到点 A,则 A、B、C 三点温度由大到小为  |
C.若两个反应达到平衡时总压为  ,CO的平衡转化率为a,则 CH₄的选择性 ,CO的平衡转化率为a,则 CH₄的选择性 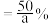 |
D.若两个反应达到平衡时总压为 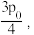 CO的平衡转化率为a,则反应Ⅰ的 CO的平衡转化率为a,则反应Ⅰ的  |
您最近一年使用:0次