解题方法
1 . 某可逆反应在体积为5L的密闭容器中进行,0~3min内各物质的物质的量的变化情况如图所示(A、B、C均为气体)。_______ 。
(2)在2min末,A的浓度为______ ;反应开始至2min时,B的平均反应速率为______ 。
(3)2min时,正反应速率______ 逆反应速率(填“>”“<”或“=”)。
(4)能说明该反应已达到平衡状态的是______ (填字母)。
a.v(A)=2v(B) b.c(A):c(B):c(C)=2:1:2
c.v逆(A)=2v正(B) d.容器内各组分浓度保持不变
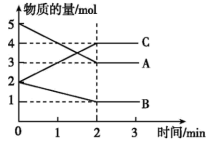
(2)在2min末,A的浓度为
(3)2min时,正反应速率
(4)能说明该反应已达到平衡状态的是
a.v(A)=2v(B) b.c(A):c(B):c(C)=2:1:2
c.v逆(A)=2v正(B) d.容器内各组分浓度保持不变
您最近一年使用:0次
解题方法
2 . 化合物C是一种医药中间体,可通过以下方法合成:_______ 和_______ (每空1分)。
(2)B的结构简式为_______ ,A→B的反应类型为_______ 。
(3)写出B→C的化学反应方程式_______ 。
(4)C分子中有_______ 种不同化学环境的氢原子。
(5)D是A的一种同分异构体。D的苯环上的一氯代物有2种,D能发生水解反应且能发生银镜反应,写出符合条件的D的结构简式:_______ 。
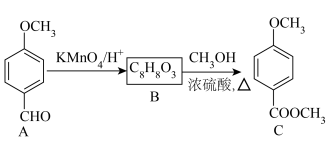
(2)B的结构简式为
(3)写出B→C的化学反应方程式
(4)C分子中有
(5)D是A的一种同分异构体。D的苯环上的一氯代物有2种,D能发生水解反应且能发生银镜反应,写出符合条件的D的结构简式:
您最近一年使用:0次
3 . 氯及其化合物既是重要化工原料,又是高效、广谱消毒剂。_______ ,利用装置Ⅰ制备 ,发生反应的化学方程式为
,发生反应的化学方程式为_______ 。
(2)若要利用装置Ⅱ收集纯净的 ,则需要先将装置Ⅰ中产生的气体依次通过盛装
,则需要先将装置Ⅰ中产生的气体依次通过盛装_______ (填试剂名称)、浓硫酸的洗气瓶除杂;收集 时,气体从集气瓶的
时,气体从集气瓶的_______ (选“m”或“n”)导管口进入。
(3)制得的 按照装置Ⅲ中箭头方向通入。
按照装置Ⅲ中箭头方向通入。
①若试剂X为水,则可制得氯水。证明氯水中含有 的操作及现象为
的操作及现象为_______ 。
②若试剂X为 ,则可制得
,则可制得 的
的 溶液(
溶液( 可溶于
可溶于 ,但不与
,但不与 反应)。取稀盐酸、新制氯水、
反应)。取稀盐酸、新制氯水、 的
的 溶液,分别滴在三张红色纸条上,可观察到的实验现象是
溶液,分别滴在三张红色纸条上,可观察到的实验现象是_______ ,证明氯水中的_______ (填化学式)具有漂白作用。
③若试剂X为1mol/L KBr溶液,则可以观察到溶液逐渐变为棕红色,溶液中发生反应的离子方程式为_______ 。
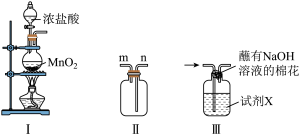
 ,发生反应的化学方程式为
,发生反应的化学方程式为(2)若要利用装置Ⅱ收集纯净的
 ,则需要先将装置Ⅰ中产生的气体依次通过盛装
,则需要先将装置Ⅰ中产生的气体依次通过盛装 时,气体从集气瓶的
时,气体从集气瓶的(3)制得的
 按照装置Ⅲ中箭头方向通入。
按照装置Ⅲ中箭头方向通入。①若试剂X为水,则可制得氯水。证明氯水中含有
 的操作及现象为
的操作及现象为②若试剂X为
 ,则可制得
,则可制得 的
的 溶液(
溶液( 可溶于
可溶于 ,但不与
,但不与 反应)。取稀盐酸、新制氯水、
反应)。取稀盐酸、新制氯水、 的
的 溶液,分别滴在三张红色纸条上,可观察到的实验现象是
溶液,分别滴在三张红色纸条上,可观察到的实验现象是③若试剂X为1mol/L KBr溶液,则可以观察到溶液逐渐变为棕红色,溶液中发生反应的离子方程式为
您最近一年使用:0次
4 . 下图为铁及其化合物的“价-类”二维图。_______ 和化学式②_______ 。
(2)参考“价-类”二维图,预测 的性质:
的性质:
可供选择的试剂:① ②KI溶液 ③NaOH溶液 ④
②KI溶液 ③NaOH溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液
Ⅰ.从化合价角度分析。 中的Fe元素的化合价为
中的Fe元素的化合价为_______ ,可能与上述试剂中的_______ (填字母)发生氧化还原反应。
Ⅱ.从物质类别角度分析。 属于盐,可能与上述试剂中的
属于盐,可能与上述试剂中的_______ (填字母)发生复分解反应。
(3)某工厂用) 溶液腐蚀镀有铜的绝缘板生产印刷电路,写出该过程的化学反应方程式并用双线桥标出电子转移的方向和数目
溶液腐蚀镀有铜的绝缘板生产印刷电路,写出该过程的化学反应方程式并用双线桥标出电子转移的方向和数目_______ 。
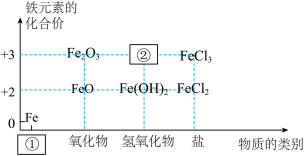
(2)参考“价-类”二维图,预测
 的性质:
的性质:可供选择的试剂:①
 ②KI溶液 ③NaOH溶液 ④
②KI溶液 ③NaOH溶液 ④ 溶液 ⑤
溶液 ⑤ 溶液
溶液Ⅰ.从化合价角度分析。
 中的Fe元素的化合价为
中的Fe元素的化合价为Ⅱ.从物质类别角度分析。
 属于盐,可能与上述试剂中的
属于盐,可能与上述试剂中的(3)某工厂用)
 溶液腐蚀镀有铜的绝缘板生产印刷电路,写出该过程的化学反应方程式并用双线桥标出电子转移的方向和数目
溶液腐蚀镀有铜的绝缘板生产印刷电路,写出该过程的化学反应方程式并用双线桥标出电子转移的方向和数目
您最近一年使用:0次
5 .  气体与足量
气体与足量 溶液完全反应后,再加入
溶液完全反应后,再加入 溶液,发生如下化学反应:
溶液,发生如下化学反应:
①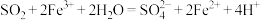 ;
;
② ,
,
下列有关说法正确的是
 气体与足量
气体与足量 溶液完全反应后,再加入
溶液完全反应后,再加入 溶液,发生如下化学反应:
溶液,发生如下化学反应:①
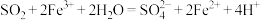 ;
;②
 ,
,下列有关说法正确的是
A.氧化性: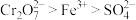 |
B.若有6.72L 参加反应,则最终消耗0.2mol 参加反应,则最终消耗0.2mol |
C.反应②中,每有1mol  参加反应,转移电子的数目为 参加反应,转移电子的数目为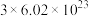 |
D.由上述反应原理推断: 不能将 不能将 氧化成 氧化成 |
您最近一年使用:0次
6 . 用 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是
 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是A.0.2mol/L  溶液中,含有的 溶液中,含有的 数目为0.4 数目为0.4 |
B.标准状况下,22.4L  含有的分子数目为 含有的分子数目为 |
C.1mol  所含质子数为11 所含质子数为11 |
D.22g  中含有的氧原子数为2 中含有的氧原子数为2 |
您最近一年使用:0次
7 . 某无色澄清溶液中,含有表中的四种离子:
分别取该溶液10mL进行如下实验:
已知:①该溶液中各离子的物质的量浓度相同;②淀粉溶液遇 变蓝;③忽略水自身的电离。
变蓝;③忽略水自身的电离。
回答下列问题:
(1)实验室用 和浓盐酸制备氯气,该反应的化学方程式为
和浓盐酸制备氯气,该反应的化学方程式为_______ ,每转移 ,生成
,生成_______ L(换算成标准状况下) 。
。
(2)配制90mL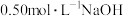 溶液需要
溶液需要_______ gNaOH固体,若定容时仰视刻度线,则会导致所配溶液的物质的量浓度_______ (填“偏大”“偏小”或“不变”)。
(3)实验I中通入氯气发生反应的离子方程式为_______ ;实验II中的白色沉淀为_______ (填化学式)。
(4)该溶液中存在的阳离子有_______ ;各离子的物质的量浓度均为_______  。
。
| 阳离子 |  、 、 、 、 、 、 |
| 阴离子 |  、 、 、 、 、 、 |
| 序号 | 实验内容 | 实验结果 |
| I | 向该溶液中通入少量氯气,然后加入淀粉溶液 | 溶液变蓝 |
| II | 向该溶液中加入 溶液(NaOH溶液过量) 溶液(NaOH溶液过量) | 产生1.45g白色沉淀 |
 变蓝;③忽略水自身的电离。
变蓝;③忽略水自身的电离。回答下列问题:
(1)实验室用
 和浓盐酸制备氯气,该反应的化学方程式为
和浓盐酸制备氯气,该反应的化学方程式为 ,生成
,生成 。
。(2)配制90mL
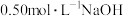 溶液需要
溶液需要(3)实验I中通入氯气发生反应的离子方程式为
(4)该溶液中存在的阳离子有
 。
。
您最近一年使用:0次
8 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.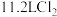 中含有的分子数为 中含有的分子数为 |
B.常温常压下,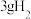 中含有的原子总数为 中含有的原子总数为 |
C.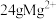 中含有的核外电子数为 中含有的核外电子数为 |
D. 稀盐酸中含有的 稀盐酸中含有的 数为 数为 |
您最近一年使用:0次
9 . 在电解饱和食盐水的过程中,当阴阳两极共收集到224mL气体(标准状况)时,理论上可得到氢氧化钠
| A.0.4g | B.0.8g | C.0.01g | D.0.02g |
您最近一年使用:0次
10 . 现有pH=2的醋酸溶液甲和pH=2的盐酸乙,请根据下列操作完成问题:
(1)取10mL的甲溶液,加入等体积的水,醋酸的电离平衡_______ (填“向左”“向右”或“不”)移动;另取10mL的甲溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),待固体溶解完后,溶液中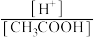 的比值将
的比值将_______ (填“增大”“减小”或“无法确定”)。
(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为:pH(甲)_______ pH(乙)(填“大于”“小于”或“等于”,下同)。
(3)25℃时,取25mL的甲溶液,加入等体积pH=12的NaOH溶液,反应后溶液中:pH_______ 7;[Na+]_______ [CH3COO﹣]。
(1)取10mL的甲溶液,加入等体积的水,醋酸的电离平衡
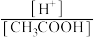 的比值将
的比值将(2)相同条件下,取等体积的甲、乙两溶液,各稀释100倍。稀释后的溶液,其pH大小关系为:pH(甲)
(3)25℃时,取25mL的甲溶液,加入等体积pH=12的NaOH溶液,反应后溶液中:pH
您最近一年使用:0次



