名校
1 . 化合物M是一种医药中间体,实验室中M的一种合成路线如下:
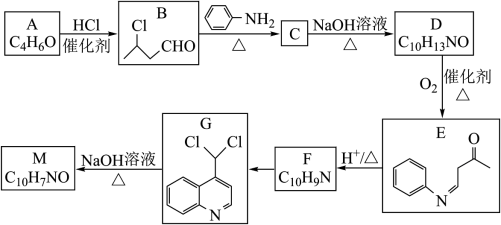
已知:
①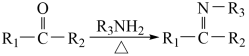
②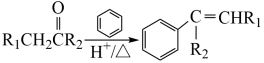
③一个碳原子连接两个—OH不稳定,易自动脱水
回答下列问题:
(1)A中官能团的名称为_______ ;B的化学名称为_______ 。
(2)D的结构简式为(并标出手性碳原子)_______ 。
(3)由F生成G所需试剂和条件为_______ 。
(4)由G生成M的化学方程式为_______ 。
(5)Q为D的同分异构体,同时满足下列条件的Q的所有结构简式有_______ 种(不含立体异构)。
①苯环上连有5个取代基;
②既含-NH2,又能与银氨溶液发生银镜反应。
(6)参照上述合成路线和信息,以2-丙醇和苯为原料(无机试剂任选),设计制备 的合成路线
的合成路线_______ 。

已知:
①

②

③一个碳原子连接两个—OH不稳定,易自动脱水
回答下列问题:
(1)A中官能团的名称为
(2)D的结构简式为(并标出手性碳原子)
(3)由F生成G所需试剂和条件为
(4)由G生成M的化学方程式为
(5)Q为D的同分异构体,同时满足下列条件的Q的所有结构简式有
①苯环上连有5个取代基;
②既含-NH2,又能与银氨溶液发生银镜反应。
(6)参照上述合成路线和信息,以2-丙醇和苯为原料(无机试剂任选),设计制备
 的合成路线
的合成路线
您最近一年使用:0次
2021-05-27更新
|
288次组卷
|
12卷引用:新疆昌吉州2022届高三第二次诊断性测试理科综合化学试题
新疆昌吉州2022届高三第二次诊断性测试理科综合化学试题河北省张家口市2021届高三第二次模拟考试化学试题河北省承德市2021届高三下学期第二次模拟考试化学试题(已下线)2021年高考化学押题预测卷(河北卷)(02)(含考试版、答题卡、参考答案、全解全析)(已下线)押山东卷第19题 有机化学基础综合题-备战2021年高考化学临考题号押题(山东卷)(已下线)押全国卷理综第36题 有机化学基础-备战2021年高考化学临考题号押题重庆市长寿中学2021届高三5月考前模拟化学试题四川省内江市第六中学2021-2022学年高三上学期第四次月考化学试题陕西省西安市铁一中滨河高级中学2021-2022学年高三上学期第三次模拟考试理综化学试题河南省温县第一高级中学2021-2022学年高三下学期开学考试理科综合化学试题北京市顺义区2022届高三上学期开学考试化学试题北京顺义区联合体2020-2021学年高三上学期开学初考试化学模拟试题
2 . 以物质a和乙二醇为原料合成有机物d的一种合成路线如图,下列说法错误的是
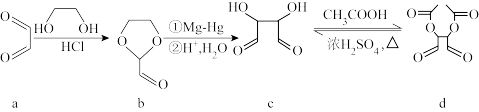

| A.a、b、c、d均能发生银镜反应 |
| B.a、c、d互为同系物 |
| C.a分子中不存在手性碳原子 |
| D.a、c均易溶于水 |
您最近一年使用:0次
2022-01-20更新
|
282次组卷
|
4卷引用:新疆昌吉州2021-2022学年高三上学期第二次高考质量检测化学试题
新疆昌吉州2021-2022学年高三上学期第二次高考质量检测化学试题广东省清远市2021-2022学年高三上学期期末教学质量检测化学试题(已下线)3.5.1 有机合成的主要任务-2021-2022学年高二化学课后培优练(人教版2019选择性必修3)(已下线)2022年重庆高考真题化学试题变式题(选择题6-10)
3 . 化合物Ⅷ是一种常用的解热镇痛药,一种以丙酸为基础原料合成化合物Ⅷ的合成路线如下:
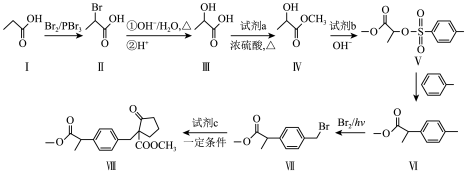
已知:RCH2COOCH3+R’CH2Br
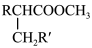 +HBr
+HBr
(1)有机物Ⅱ中含氧官能团名称为_______ 。
(2)V→Ⅵ的反应类型为_______ 。
(3)试剂b的分子式为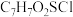 ,写出试剂b的结构简式:
,写出试剂b的结构简式:_______ 。
(4)在一定条件下,化合物Ⅶ和试剂c反应时,除生成Ⅷ外,还有 生成,写出反应Ⅶ→Ⅷ的化学方程式:
生成,写出反应Ⅶ→Ⅷ的化学方程式:_______ 。
(5)Ⅸ是Ⅶ的同分异构体,符合下列条件的Ⅸ有_______ 种,其中核磁共振氢谱图中有4组吸收峰,且峰面积之比为6∶3∶2∶2的结构简式为_______ (任写一种)。
①分子中含有苯环且苯环上有4个取代基。
②在碱性溶液中可发生水解,水解产物酸化后得到有机物甲和有机物乙,甲能与 溶液发生显色反应,
溶液发生显色反应, 乙最多能消耗
乙最多能消耗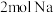 。
。
(6)请设计以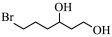 、
、 为原料制备
为原料制备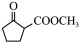 的合成路线流程图
的合成路线流程图_______ (无机试剂和有机溶剂任用)。

已知:RCH2COOCH3+R’CH2Br

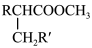 +HBr
+HBr(1)有机物Ⅱ中含氧官能团名称为
(2)V→Ⅵ的反应类型为
(3)试剂b的分子式为
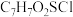 ,写出试剂b的结构简式:
,写出试剂b的结构简式:(4)在一定条件下,化合物Ⅶ和试剂c反应时,除生成Ⅷ外,还有
 生成,写出反应Ⅶ→Ⅷ的化学方程式:
生成,写出反应Ⅶ→Ⅷ的化学方程式:(5)Ⅸ是Ⅶ的同分异构体,符合下列条件的Ⅸ有
①分子中含有苯环且苯环上有4个取代基。
②在碱性溶液中可发生水解,水解产物酸化后得到有机物甲和有机物乙,甲能与
 溶液发生显色反应,
溶液发生显色反应, 乙最多能消耗
乙最多能消耗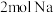 。
。(6)请设计以
 、
、 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图
您最近一年使用:0次
2022-01-27更新
|
207次组卷
|
4卷引用:新疆昌吉州2021-2022学年高三上学期第二次高考质量检测化学试题
20-21高三上·广东·期末
名校
解题方法
4 . 化合物G是一种药物合成中间体,其合成路线如图:

已知:R1CH2COOCH2CH3+R2COOCH2CH3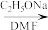
 +CH3CH2OH
+CH3CH2OH
(1)化合物A的名称是__ 。
(2)反应②和⑤的反应类型分别是__ 、__ 。
(3)写出C到D的反应方程式__ 。
(4)E的分子式__ 。
(5)F中官能团的名称是__ 。
(6)X是G的同分异构体,X具有五元碳环结构,其核磁共振氢谱显示四组峰,且峰面积之比为6:2:1:1。写出两种符合要求的X的结构简式___ 。
(7)设计由乙酸乙酯和1,4-二溴丁烷制备 的合成路线
的合成路线___ (无机试剂任选)。

已知:R1CH2COOCH2CH3+R2COOCH2CH3
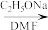
 +CH3CH2OH
+CH3CH2OH(1)化合物A的名称是
(2)反应②和⑤的反应类型分别是
(3)写出C到D的反应方程式
(4)E的分子式
(5)F中官能团的名称是
(6)X是G的同分异构体,X具有五元碳环结构,其核磁共振氢谱显示四组峰,且峰面积之比为6:2:1:1。写出两种符合要求的X的结构简式
(7)设计由乙酸乙酯和1,4-二溴丁烷制备
 的合成路线
的合成路线
您最近一年使用:0次
2020-03-02更新
|
1026次组卷
|
7卷引用:新疆昌吉州第二中学2020-2021学年高二下学期第一次月考化学(A)试题
名校
解题方法
5 . 苯并环己酮是合成萘(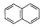 )或萘的取代物的中间体。由苯并环己酮合成1-乙基萘的一种路线如下图所示:
)或萘的取代物的中间体。由苯并环己酮合成1-乙基萘的一种路线如下图所示:
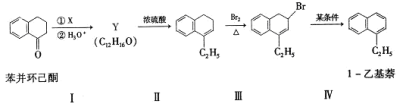
已知:
回答下列问题:
(1)萘的分子式为_______ ;苯并环己酮所含官能团是_______ (填名称)。
(2)Y的结构简式为_________ 。
(3)步骤Ⅲ的反应属于_________ (填反应类型)。
(4)步骤Ⅳ反应的化学方程式为____________ (标明反应条件)。
(5)苯并环己酮用强氧化剂氧化可生成邻苯二甲酸。邻苯二甲酸和乙二醇经缩聚反应生成的高分子化合物的结构简式是________ 。
(6)1-乙基萘的同分异构体中,属于萘的取代物的有_______ 种(不含1-乙基萘)。W也是1 -乙基萘的同分异构体,它是含一种官能团的苯的取代物,核磁共振氢谱显示W有三种不同化学环境的氢原子,且个数比为1:1:2,W的结构简式为_________ 。
(7)仍以苯并环己酮为原料,上述合成路线中,只要改变其中一个步骤的反应条件和试剂,便可合成萘。完成该步骤:__________ (表示方法示例:A  B)。
B)。
 )或萘的取代物的中间体。由苯并环己酮合成1-乙基萘的一种路线如下图所示:
)或萘的取代物的中间体。由苯并环己酮合成1-乙基萘的一种路线如下图所示:
已知:

回答下列问题:
(1)萘的分子式为
(2)Y的结构简式为
(3)步骤Ⅲ的反应属于
(4)步骤Ⅳ反应的化学方程式为
(5)苯并环己酮用强氧化剂氧化可生成邻苯二甲酸。邻苯二甲酸和乙二醇经缩聚反应生成的高分子化合物的结构简式是
(6)1-乙基萘的同分异构体中,属于萘的取代物的有
(7)仍以苯并环己酮为原料,上述合成路线中,只要改变其中一个步骤的反应条件和试剂,便可合成萘。完成该步骤:
 B)。
B)。
您最近一年使用:0次
2017-04-12更新
|
460次组卷
|
6卷引用:新疆昌吉市第九中学2021届高三上学期开学考试化学试题
解题方法
6 . 绿色化学的核心就是利用化学原理和技术手段从源头上减少或消除工业生产对环境的污染。下列做法不符合“绿色化学”理念的是
| A.尽可能采用对人类和环境无毒无害的合成路线 |
| B.用可降解塑料生产包装盒或快餐盒 |
| C.制备硝酸铜不用Cu和浓硝酸反应,应用Cu和稀硝酸反应 |
D.用反应2CH2=CH2 + O2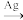 2 2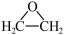 制备环氧乙烷 制备环氧乙烷 |
您最近一年使用:0次
名校
7 . Ⅰ.已知: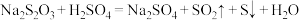 ,某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
,某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
(1)Na2S2O3中S的化合价为 _______ 价
(2)该实验①、②可探究温度对反应速率的影响,因此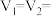
_______ ,V3=_______
(3)若实验①、③探究硫酸浓度对反应速率的影响,V4=_______ ,V5=_______ 。
Ⅱ.在1 L恒容密闭容器中充入一定量CH3OH发生反应:2CH3OH(g)=CH3OCH3(g)+H2O(g) △H,测得CH3OH的浓度与温度的关系如图所示:
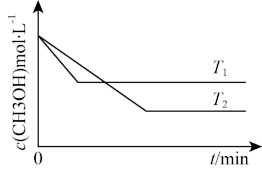
(4)△H_______ (填“>”“<”或“=”)0
(5)在T1时达到平衡后,再向容器中充入少量甲醇蒸气,CH3OH的平衡转化率_______ (填“增大”“减小”或“不变”)。
(6)工业上,利用水煤气合成CH3OH的反应表示如下:2H2(g)+CO(g) CH3OH(g) △H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。
CH3OH(g) △H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。
①从反应开始恰好平衡状态时,H2的平均反应速率v(H2)为_______ mol/(L·min)。
②在温度不变条件下,上述反应达到平衡后再向容器中充入0.01 mol H2和0.05 mol CH3OH(g)时,平衡_______ (填“向左移动”、“向右移动”或“不移动”)。
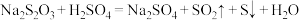 ,某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
,某同学探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:| 实验序号 | 反应温度/ |  溶液 溶液 | 稀 |  | ||
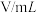 | 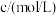 |  | 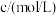 |  | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 |  | 0.10 |  | 0.50 |  |
| ③ | 20 |  | 0.10 | 4.0 | 0.50 | 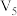 |
(2)该实验①、②可探究温度对反应速率的影响,因此
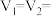
(3)若实验①、③探究硫酸浓度对反应速率的影响,V4=
Ⅱ.在1 L恒容密闭容器中充入一定量CH3OH发生反应:2CH3OH(g)=CH3OCH3(g)+H2O(g) △H,测得CH3OH的浓度与温度的关系如图所示:

(4)△H
(5)在T1时达到平衡后,再向容器中充入少量甲醇蒸气,CH3OH的平衡转化率
(6)工业上,利用水煤气合成CH3OH的反应表示如下:2H2(g)+CO(g)
 CH3OH(g) △H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。
CH3OH(g) △H=-91.0 kJ·mol-1,向1 L的恒容密容器中加入0.1 mol H2和0.05 mol CO在一定温度下发生上述反应,10 min后反应达到平衡状态,测得放出的热量为3.64 kJ。①从反应开始恰好平衡状态时,H2的平均反应速率v(H2)为
②在温度不变条件下,上述反应达到平衡后再向容器中充入0.01 mol H2和0.05 mol CH3OH(g)时,平衡
您最近一年使用:0次
解题方法
8 . 现有A、B、C三种烃,其球棍模型如下图:___________ (填对应的字母)。
(2)在120℃、101kPa条件下,将以上三种烃和足量O2混合点燃,完全燃烧后恢复到相同条件,测得有些气体在反应前后气体总体积没有发生变化,满足条件的气体是___________ (填对应的字母)。
(3)工业上合成一氯乙烷,应选___________ 为原料(填对应的字母)。
(4)要除去C中混有的B可以采用的方法是___________。
(5)烃D是B的一种同系物,其密度是相同条件下B的2倍,则烃D的同分异构体有___________ 种。(不包括D本身,且不考虑立体异构)
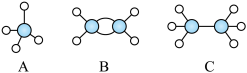
(2)在120℃、101kPa条件下,将以上三种烃和足量O2混合点燃,完全燃烧后恢复到相同条件,测得有些气体在反应前后气体总体积没有发生变化,满足条件的气体是
(3)工业上合成一氯乙烷,应选
(4)要除去C中混有的B可以采用的方法是___________。
| A.将气体通过酸性高锰酸钾溶液 |
| B.将气体通过溴水 |
| C.一定条件下,向混合气体中通入H2 |
| D.将气体通过NaOH溶液 |
您最近一年使用:0次
名校
9 . “绿水青山就是金山银山”,运用化学反应原理研究碳、氮、硫的单质及其化合物的反应对缓解环境污染、能源危机具有重要意义。甲醇是一种可再生能源,具有广泛的开发和应用前景:工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)  CH3OH(g) ΔH1=-116kJ•mol-1。
CH3OH(g) ΔH1=-116kJ•mol-1。
(1)下列关于该反应说法正确的是
(2)一定条件下向2 L的密闭容器中充入1molCO和2molH2发生反应:CO(g)+2H2(g)  CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示:
CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示:
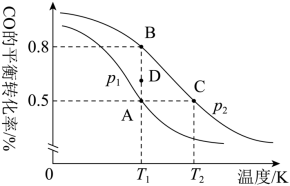
①A、B、C三点平衡常数KA、KB、KC的中最小的为是_______ 。
A.KA B. KB C.KC
②压强p1_______ p2(填“>”“<”或“=”),则B点的Kp=_______ (Kp为以分压表示的平衡常数;分压=总压×物质的量分数)
A.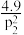 B.
B.  C.
C. 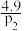 D.
D. 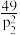
③在T1和p1条件下,由D点到A点过程中,正、逆反应速率之间的关系:v正_______ v逆(填“>”“<”或“=”)。
(3)已知可逆反应CO+H2O(g) CO2+H2,
CO2+H2,
①830 K,若起始时:c(CO)=2 mol/L,c(H2O)=3 mol/L,平衡时CO的转化率为60%,水蒸气的转化率为_______ ;K值为_______ 。
②830 K,若只将起始时c(H2O)改为6 mol/L,则水蒸气的转化率为_______ 。
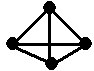
(4)已知N4分子结构如图,断裂1 mol N≡N键吸收942kJ热量,生成1 mol N-N键释放167 kJ热量根据以上信息和数据,下列热化学方程式正确的是
 CH3OH(g) ΔH1=-116kJ•mol-1。
CH3OH(g) ΔH1=-116kJ•mol-1。(1)下列关于该反应说法正确的是
| A.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 |
| B.若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大 |
| C.升高温度,化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数 |
| D.若加入催化剂,不影响反应活化能但能增大单位体积内活化分子百分数,从而增大化学反应速率 |
 CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示:
CH3OH(g),CO的平衡转化率与温度、压强的关系如图所示:
①A、B、C三点平衡常数KA、KB、KC的中最小的为是
A.KA B. KB C.KC
②压强p1
A.
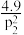 B.
B.  C.
C. 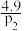 D.
D. 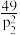
③在T1和p1条件下,由D点到A点过程中,正、逆反应速率之间的关系:v正
(3)已知可逆反应CO+H2O(g)
 CO2+H2,
CO2+H2,①830 K,若起始时:c(CO)=2 mol/L,c(H2O)=3 mol/L,平衡时CO的转化率为60%,水蒸气的转化率为
②830 K,若只将起始时c(H2O)改为6 mol/L,则水蒸气的转化率为
(4)已知N4分子结构如图,断裂1 mol N≡N键吸收942kJ热量,生成1 mol N-N键释放167 kJ热量根据以上信息和数据,下列热化学方程式正确的是

| A.2N2=N4 △H =-882 kJ·mol-1 |
| B.N2 (g)=0.5N4 (g) △H=+441 kJ |
| C.N2 (g)=0.5N4 (g) △H=-441 kJ·mol-1 |
| D.2N2(g)=N4(g) △H=+882 kJ·mol-1 |
您最近一年使用:0次
解题方法
10 . 已知某物质X能发生如图转化(四种物质均含元素R),回答下列问题:
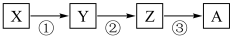
I.已知X是一种能使湿润的红色石蕊试纸变蓝的气体,与A化合生成一种正盐,则:
(1)X的电子式为______ ,写出X与Z在催化剂作用下生成两种无毒物质的化学方程式________ 。
(2)在含 离子的溶液中,
离子的溶液中,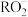 离子可转化为RO,写出
离子可转化为RO,写出 和
和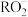 离子在酸性水溶液中反应的离子方程式
离子在酸性水溶液中反应的离子方程式___________ 。
II.若X的产量是衡量一个国家石油化工水平的标志,且Y与A在浓硫酸作用下生成一种具有香味的物质B,则:
(3)X的分子式为___________ ,①的反应类型是___________ ,工业上以X为为原料可以合成一种生活中最常见的有机高分子材料,其反应的化学方程式为___________ 。
(4)实验室利用Y与A制备B,写出化学反应方程式:___________ 。

I.已知X是一种能使湿润的红色石蕊试纸变蓝的气体,与A化合生成一种正盐,则:
(1)X的电子式为
(2)在含
 离子的溶液中,
离子的溶液中,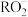 离子可转化为RO,写出
离子可转化为RO,写出 和
和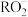 离子在酸性水溶液中反应的离子方程式
离子在酸性水溶液中反应的离子方程式II.若X的产量是衡量一个国家石油化工水平的标志,且Y与A在浓硫酸作用下生成一种具有香味的物质B,则:
(3)X的分子式为
(4)实验室利用Y与A制备B,写出化学反应方程式:
您最近一年使用:0次



