1 . 下图为氯及其化合物的“价类二维图”,下列说法错误的是

| A.c可用于自来水杀菌消毒 |
B.e的化学式为 |
C.d见光易分解,反应方程式为 |
| D.a分别与g、h、f在一定条件下反应都可生成b |
您最近一年使用:0次
解题方法
2 . 含钠化合物在工业生产和日常生活中应用广泛。
(1)钠元素的氧化物中属于碱性氧化物的是___________ (写化学式)。
(2)实验室需使用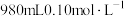 的
的 溶液。
溶液。
①需用托盘天平称量 固体的质量是
固体的质量是___________ 。
②某同学配制 溶液的过程如下图所示:
溶液的过程如下图所示:___________ (填标号)。
③下列操作可导致所配溶液的浓度偏高的是___________ (填标号)。
A.容量瓶内原来存有少量的水
B.定容时液面超过刻度线,用胶头滴管吸出
C. 固体溶解后立即转移到容量瓶中
固体溶解后立即转移到容量瓶中
D.定容时俯视刻度线
(3)市场上销售的“苏打水”是一种非常受欢迎的饮品,其溶质是 而不是
而不是 。
。
①写出 的电离方程式
的电离方程式___________ 。
②“苏打水”会因储藏温度过高而分解产生少量 ,使口感发涩。写出一种除去“苏打水”中少量
,使口感发涩。写出一种除去“苏打水”中少量 ,改善口感的方法
,改善口感的方法___________ (用离子方程式表示)。
(4)给游泳池中的水消毒时,若将84消毒液与双氧水混用,可导致泳池内藻类快速生长,池水变绿,其主要原因是 与
与 反应产生
反应产生 ,促进藻类生长。该反应说明氧化性:
,促进藻类生长。该反应说明氧化性:
___________  (填“>”或“<”);当生成
(填“>”或“<”);当生成 时,转移电子数为
时,转移电子数为___________ 。
(1)钠元素的氧化物中属于碱性氧化物的是
(2)实验室需使用
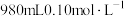 的
的 溶液。
溶液。①需用托盘天平称量
 固体的质量是
固体的质量是②某同学配制
 溶液的过程如下图所示:
溶液的过程如下图所示: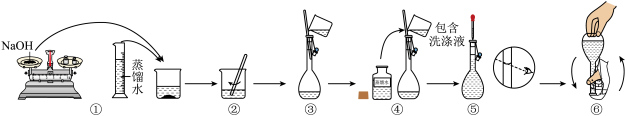
③下列操作可导致所配溶液的浓度偏高的是
A.容量瓶内原来存有少量的水
B.定容时液面超过刻度线,用胶头滴管吸出
C.
 固体溶解后立即转移到容量瓶中
固体溶解后立即转移到容量瓶中D.定容时俯视刻度线
(3)市场上销售的“苏打水”是一种非常受欢迎的饮品,其溶质是
 而不是
而不是 。
。①写出
 的电离方程式
的电离方程式②“苏打水”会因储藏温度过高而分解产生少量
 ,使口感发涩。写出一种除去“苏打水”中少量
,使口感发涩。写出一种除去“苏打水”中少量 ,改善口感的方法
,改善口感的方法(4)给游泳池中的水消毒时,若将84消毒液与双氧水混用,可导致泳池内藻类快速生长,池水变绿,其主要原因是
 与
与 反应产生
反应产生 ,促进藻类生长。该反应说明氧化性:
,促进藻类生长。该反应说明氧化性:
 (填“>”或“<”);当生成
(填“>”或“<”);当生成 时,转移电子数为
时,转移电子数为
您最近一年使用:0次
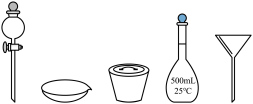
3 . 某小组设计实验测定菠菜中铁元素的含量。已知:菠菜中铁元素主要以草酸亚铁( )的形式存在,草酸亚铁难溶于水;草酸是一种二元有机弱酸,具有还原性。
)的形式存在,草酸亚铁难溶于水;草酸是一种二元有机弱酸,具有还原性。
I.菠菜的预处理___________ (从下图中选择,写名称)。___________ 。
(3)检验“滤液”中是否含有 的试剂是
的试剂是___________ (写名称)。
(4)“滤液”中加入 的作用是
的作用是___________ (用离子方程式表示)。
Ⅱ.比色法测定菠菜中铁元素的含量
(5)利用色度传感器测得不同浓度 标准液的吸收率如下图:
标准液的吸收率如下图: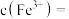
___________  ,该菠菜中铁元素的含量为
,该菠菜中铁元素的含量为___________  。
。
 )的形式存在,草酸亚铁难溶于水;草酸是一种二元有机弱酸,具有还原性。
)的形式存在,草酸亚铁难溶于水;草酸是一种二元有机弱酸,具有还原性。I.菠菜的预处理

(3)检验“滤液”中是否含有
 的试剂是
的试剂是(4)“滤液”中加入
 的作用是
的作用是Ⅱ.比色法测定菠菜中铁元素的含量
(5)利用色度传感器测得不同浓度
 标准液的吸收率如下图:
标准液的吸收率如下图: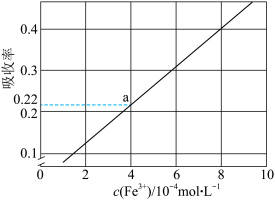
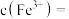
 ,该菠菜中铁元素的含量为
,该菠菜中铁元素的含量为 。
。
您最近一年使用:0次
4 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.常温常压下,23g 中含有的分子总数为 中含有的分子总数为 |
B.  溶液中含有的 溶液中含有的 数小于 数小于 |
C.1L 的亚硫酸溶液中含有的 的亚硫酸溶液中含有的 数为 数为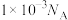 |
D.氢氧燃料电池工作时,正极消耗11.2L气体(标况下),电路中转移电子数为 |
您最近一年使用:0次
5 . 下列事实能证明ROH是弱碱的是
A. 溶液呈酸性 溶液呈酸性 |
| B.ROH溶液的导电能力小于盐酸 |
C.室温下, ROH溶液pH约为11 ROH溶液pH约为11 |
D.ROH溶液与 溶液反应生成白色沉淀 溶液反应生成白色沉淀 |
您最近一年使用:0次
6 . 劳动创造幸福生活。下列对劳动项目的原理解释正确的是
| 选项 | 劳动项目 | 化学原理 |
| A. | 使用明矾作净水剂 | 明矾具有强氧化性,能杀菌消毒 |
| B. | 为防止地下钢管被腐蚀,将钢管与直流电源负极相连 | 采用了牺牲阳极法进行防护 |
| C. | 用纯碱溶液洗涤餐具上的油脂 | 油脂在碱性条件下易水解 |
| D. | 工业合成氨反应温度控制在700K左右 | 温度越高氨的平衡产率越大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
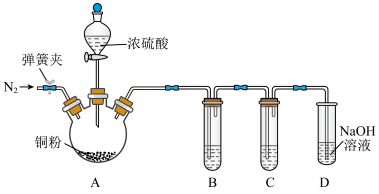
7 . 某研究小组用下列装置(夹持和加热装置已略去)研究不同价态硫元素之间的转化。 ,一段时间后关闭弹簧夹;
,一段时间后关闭弹簧夹;
②滴加浓硫酸,加热三颈烧瓶。
(1)通入 的目的为
的目的为___________ 。
(2)三颈烧瓶中产生大量气体,甲同学猜测三颈烧瓶中的反应实现了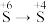 的转化,提出在试管B中盛放品红溶液,出现
的转化,提出在试管B中盛放品红溶液,出现___________ 现象即可证明猜测正确。
(3)甲同学又提出把三颈烧瓶中的金属铜换成活性炭,也能实现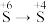 的转化,写出反应的化学方程式
的转化,写出反应的化学方程式___________ 。
(4)为了实现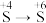 的转化,乙同学在试管C中盛放新制氯水,观察到氯水褪色,反应的离子方程式为
的转化,乙同学在试管C中盛放新制氯水,观察到氯水褪色,反应的离子方程式为___________ ,设计实验证明实现了该转化___________ 。实验中可以代替新制氯水的试剂有___________ (填标号)。
A.FeCl3溶液 B.滴有酚酞的NaOH溶液
C.淀粉—KI溶液 D.酸性KMnO4溶液
(5)丙同学提出利用该装置可同时实现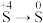 与
与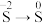 的转化,则试管C中盛放的试剂为
的转化,则试管C中盛放的试剂为___________ (写化学式)溶液。
 ,一段时间后关闭弹簧夹;
,一段时间后关闭弹簧夹;②滴加浓硫酸,加热三颈烧瓶。
(1)通入
 的目的为
的目的为(2)三颈烧瓶中产生大量气体,甲同学猜测三颈烧瓶中的反应实现了
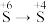 的转化,提出在试管B中盛放品红溶液,出现
的转化,提出在试管B中盛放品红溶液,出现(3)甲同学又提出把三颈烧瓶中的金属铜换成活性炭,也能实现
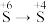 的转化,写出反应的化学方程式
的转化,写出反应的化学方程式(4)为了实现
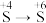 的转化,乙同学在试管C中盛放新制氯水,观察到氯水褪色,反应的离子方程式为
的转化,乙同学在试管C中盛放新制氯水,观察到氯水褪色,反应的离子方程式为A.FeCl3溶液 B.滴有酚酞的NaOH溶液
C.淀粉—KI溶液 D.酸性KMnO4溶液
(5)丙同学提出利用该装置可同时实现
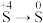 与
与 的转化,则试管C中盛放的试剂为
的转化,则试管C中盛放的试剂为
您最近一年使用:0次
解题方法
8 . 氮是生物体的重要组成元素,也是维持高等动植物生命活动的必需元素,研究氮的循环和转化对生产和生活有重要的价值。
Ⅰ.细菌可以促使铁、氮两种元素发生氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。___________ (填标号)。
a. b.
b. c.
c.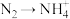 d.
d.
(2)硝化和反硝化过程均为氧化还原反应,反硝化过程中,含氮物质发生___________ (填“氧化”或“还原”)反应。
(3)写出氨态氮与亚硝态氮在氨氧化细菌的作用下转化为氮气的离子方程式___________ 。
(4)土壤中的铁循环可用于水体脱氮。土壤中的铁循环脱除水体中硝态氮和氨态氮的原理分别为:① ②
②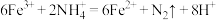 。若转移的电子数相等,则反应①②中生成
。若转移的电子数相等,则反应①②中生成 的物质的量之比为
的物质的量之比为___________ 。
Ⅱ.某实验小组用过量的氨气和氯气在常温下制备 。
。___________ 。
(6)利用装置B制取所需氯气,写出反应的离子方程式___________ 。
(7)为了使氨气和氯气在D中充分混合,各接口合理的连接顺序为___________ (提示:①氨气和氯气形成逆向流动更有利于两者充分混合。②用小写字母和箭头表示,箭头方向与气流方向一致)。
________ ___________。
___________。
Ⅰ.细菌可以促使铁、氮两种元素发生氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如下图所示。

a.
 b.
b. c.
c.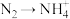 d.
d.
(2)硝化和反硝化过程均为氧化还原反应,反硝化过程中,含氮物质发生
(3)写出氨态氮与亚硝态氮在氨氧化细菌的作用下转化为氮气的离子方程式
(4)土壤中的铁循环可用于水体脱氮。土壤中的铁循环脱除水体中硝态氮和氨态氮的原理分别为:①
 ②
②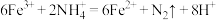 。若转移的电子数相等,则反应①②中生成
。若转移的电子数相等,则反应①②中生成 的物质的量之比为
的物质的量之比为Ⅱ.某实验小组用过量的氨气和氯气在常温下制备
 。
。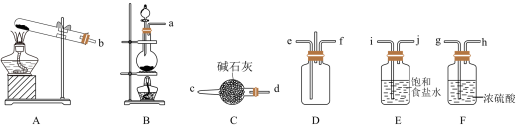
(6)利用装置B制取所需氯气,写出反应的离子方程式
(7)为了使氨气和氯气在D中充分混合,各接口合理的连接顺序为
________
 ___________。
___________。
您最近一年使用:0次
解题方法
9 . 某化学实验小组以草木灰为原料制取 晶体,制取流程如下图所示。
晶体,制取流程如下图所示。 、
、 、
、 和不溶于水的杂质。
和不溶于水的杂质。
② 的溶解度随温度的升高而增大,且增幅较大。
的溶解度随温度的升高而增大,且增幅较大。
下列说法错误的是
 晶体,制取流程如下图所示。
晶体,制取流程如下图所示。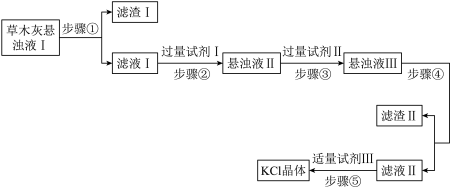
 、
、 、
、 和不溶于水的杂质。
和不溶于水的杂质。②
 的溶解度随温度的升高而增大,且增幅较大。
的溶解度随温度的升高而增大,且增幅较大。下列说法错误的是
| A.步骤①和步骤④的操作均为过滤 |
B.过量试剂I是 溶液,其作用是除去 溶液,其作用是除去 、 、 |
C.过量试剂Ⅱ是 溶液,其作用是除去过量 溶液,其作用是除去过量 |
| D.步骤⑤的操作是蒸发浓缩、冷却结晶 |
您最近一年使用:0次
10 . 常温下,将含有酚酞的 溶液平均分成两份,分别逐滴滴加稀硫酸和硫酸钠溶液,测得混合溶液的导电能力随时间变化的曲线如图所示。下列说法不正确的是
溶液平均分成两份,分别逐滴滴加稀硫酸和硫酸钠溶液,测得混合溶液的导电能力随时间变化的曲线如图所示。下列说法不正确的是
 溶液平均分成两份,分别逐滴滴加稀硫酸和硫酸钠溶液,测得混合溶液的导电能力随时间变化的曲线如图所示。下列说法不正确的是
溶液平均分成两份,分别逐滴滴加稀硫酸和硫酸钠溶液,测得混合溶液的导电能力随时间变化的曲线如图所示。下列说法不正确的是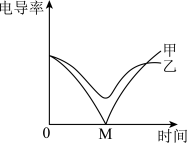
| A.甲曲线对应氢氧化钡与稀硫酸的反应 |
| B.甲曲线上的M点代表两种溶液恰好完全反应 |
| C.乙曲线导电能力减弱的过程中,溶液由红色变为无色 |
D.乙曲线对应的反应过程中 、 、 浓度均减小 浓度均减小 |
您最近一年使用:0次



