解题方法
1 . 铁是人体必需的微量元素之一,补铁剂中的Fe2+在空气中很容易被氧化为Fe3+,影响铁元素在人体中的吸收利用。某实验小组进行如图所示的对照实验,验证补铁剂和维生素C一起服用的科学性。
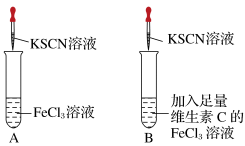
[实验操作]第一步:在A、B两支试管中加入对比试剂;第二步:振荡;第三步:滴加KSCN溶液。
[实验现象]
(1)A试管中溶液变___________ 色,B试管中无明显现象。
[实验结论]
(2)维生素C具有___________ (填“氧化性”或“还原性”),能防止Fe2+被氧化为Fe3+,所以补铁剂和维生素C一起服用具有科学依据。
[生活应用]
(3)某品牌泡腾片的主要成分为维生素C和NaHCO3,放入水中立即产生大量气泡(CO2)使口感更好,说明维生素C具有___________ (填“酸性”或“碱性”)。
(4)为防止烹调时蔬菜中维生素C的损失,烹调蔬菜应注意___________ (写一条即可)。

[实验操作]第一步:在A、B两支试管中加入对比试剂;第二步:振荡;第三步:滴加KSCN溶液。
[实验现象]
(1)A试管中溶液变
[实验结论]
(2)维生素C具有
[生活应用]
(3)某品牌泡腾片的主要成分为维生素C和NaHCO3,放入水中立即产生大量气泡(CO2)使口感更好,说明维生素C具有
(4)为防止烹调时蔬菜中维生素C的损失,烹调蔬菜应注意
您最近一年使用:0次
2 . I. 甲小组的同学用如图装置制备干燥纯净的Cl2,并进行性质实验。

(1)装置A中制取氯气,三种玻璃仪器的名称分别是酒精灯、________ 和________ ,反应的化学方程式为________ 。该反应中盐酸体现了________ (填字母)。
a.氧化性 b.还原性 c. 酸性 d. 碱性
(2)装置B的作用是________ 。
(3)装置C中盛放的是________ ,目的是除去水蒸气。
(4)装置D可以用作不同的用途。
a. 若装置D用于收集Cl2,请将图中装置D的导气管补充完整。________
b. 若装置D中放入湿润的蓝色石蕊试纸,可以看到的现象是________ 。
II. 乙小组的同学用如图所示装置制取氯水并进行相关实验。
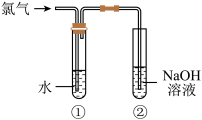
实验进行一段时间后,取少量试管①中的溶液,检验其中有Cl-的方法是_______ 。
III. 甲、乙两个小组的同学都用到了NaOH溶液,目的是________ ,反应的离子方程式为________ 。

(1)装置A中制取氯气,三种玻璃仪器的名称分别是酒精灯、
a.氧化性 b.还原性 c. 酸性 d. 碱性
(2)装置B的作用是
(3)装置C中盛放的是
(4)装置D可以用作不同的用途。
a. 若装置D用于收集Cl2,请将图中装置D的导气管补充完整。
b. 若装置D中放入湿润的蓝色石蕊试纸,可以看到的现象是
II. 乙小组的同学用如图所示装置制取氯水并进行相关实验。

实验进行一段时间后,取少量试管①中的溶液,检验其中有Cl-的方法是
III. 甲、乙两个小组的同学都用到了NaOH溶液,目的是
您最近一年使用:0次
名校
解题方法
3 . 物质的性质与元素的金属性或非金属性密切相关,能根据元素的金属性或非金属性判断下列结论正确的是
①原子半径:Al>Cl>S
②氢化物稳定性:HF>H2S>PH3
③离子的还原性: >
> >
>
④单质的氧化性:Cl2>S>Si
⑤酸性: >
>
⑥碱性: >
> >
>
①原子半径:Al>Cl>S
②氢化物稳定性:HF>H2S>PH3
③离子的还原性:
 >
> >
>
④单质的氧化性:Cl2>S>Si
⑤酸性:
 >
>
⑥碱性:
 >
> >
>
| A.①④⑤ | B.③⑥ | C.②④⑥ | D.①③④ |
您最近一年使用:0次
2020-09-06更新
|
181次组卷
|
2卷引用:人教版(2019)高一必修第一册第四章 物质结构 元素周期律 第二节 元素周期律 课时1 元素性质的周期性变化规律
4 . 下表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
(1)表中元素,化学性质最不活泼的是________ ,只有负价而无正价的是________ ,氧化性最强的单质是_______ ,还原性最强的单质是________ 。
(2)最高价氧化物的水化物中碱性最强的是________ ,酸性最强的是________ ,呈两性的是________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(1)表中元素,化学性质最不活泼的是
(2)最高价氧化物的水化物中碱性最强的是
您最近一年使用:0次
5 . 某化学课题小组将二氧化硫的制备与多个性质实验进行了一体化设计,实验装置如图所示。下列说法不正确的是
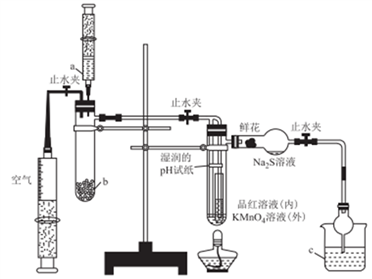

| A.a、b、c中依次盛装70%硫酸.Na2SO3固体、NaOH溶液 |
| B.实验时,湿润的pH试纸、鲜花、品红溶液、KMnO4溶液均褪色,Na2S溶液出现淡黄色沉淀 |
| C.此设计可证明SO2水溶液的酸性,SO2的氧化性、还原性、漂白性 |
| D.点燃酒精灯加热,可证明SO2使品红溶液褪色具有可逆性,使KMnO4溶液褪色不具有可逆性 |
您最近一年使用:0次
2018-04-27更新
|
1793次组卷
|
10卷引用:人教版2019必修第二册 第五章 本章达标检测
人教版2019必修第二册 第五章 本章达标检测湖南省益阳市2018届高三4月调研考试理综化学试题湖南省浏阳市第一中学2018届高三上学期入学测试化学试题(已下线)第15讲 硫及其化合物(精练)-2021年高考化学一轮复习讲练测(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)上海交通大学附属中学2022-2023学年高一上学期期末考试化学试题上海交通大学附属中学2022-2023学年高一上学期期末考试化学试题湖南省衡阳市第八中学2023-2024学年高一下学期开学考试化学试题江苏省常州市田家炳2高级中学023-2024学年高一上学期12月阶段性调研化学学科试卷
解题方法
6 . 某研究性学习小组的同学拟分析某市空气的质量情况,测定该市空气中 的含量并制定下列研究方案:
的含量并制定下列研究方案:
Ⅰ.资料表明, 具有较强的还原性,能与酸性
具有较强的还原性,能与酸性 溶液(紫红色,其还原产物
溶液(紫红色,其还原产物 在水溶液中接近无色)发生反应:
在水溶液中接近无色)发生反应:
Ⅱ.设计实验方案
方案一:利用 使品红溶液褪色作定性分析。其原理为;
使品红溶液褪色作定性分析。其原理为;___________ ;
方案二:利用 的还原性,使
的还原性,使 和已知浓度及体积的酸性
和已知浓度及体积的酸性 溶液反应进行定量分析。
溶液反应进行定量分析。
Ⅲ.选择分析地点:某工业区、某公园、某居民小区、某商业区、某交通枢纽。
Ⅳ选择分析时间:晴天、风速较小时;晴天、风速较大时;雨前;雨后。
V.对测定的结果进行初步分析并向相关单位提出建议。请你参与该研究性学习小组的活动并发表你的见解:
(1)该小组的同学拟用下列装置通过方案二定量分析空气中 的含量:
的含量:
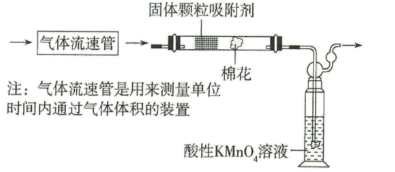
当看到实验的现象为时___________ ,应停止通空气。
(2)下图是该小组同学根据实验测得的县城不同地区空气中 的含量:
的含量:

①工厂区、交通枢纽 含量明显高于其他地区的原因是;
含量明显高于其他地区的原因是;___________ 。
②请你向当地有关部门提出一条减少工厂区 排放的建议:
排放的建议:___________ 。
(3)下表是该小组同学测得的不同天气情况下的县城空气中 的平均含量。请你分析雨后或风速较大时
的平均含量。请你分析雨后或风速较大时 平均含量较低的原因:
平均含量较低的原因:
①___________ ;
②___________ 。
 的含量并制定下列研究方案:
的含量并制定下列研究方案:Ⅰ.资料表明,
 具有较强的还原性,能与酸性
具有较强的还原性,能与酸性 溶液(紫红色,其还原产物
溶液(紫红色,其还原产物 在水溶液中接近无色)发生反应:
在水溶液中接近无色)发生反应:
Ⅱ.设计实验方案
方案一:利用
 使品红溶液褪色作定性分析。其原理为;
使品红溶液褪色作定性分析。其原理为;方案二:利用
 的还原性,使
的还原性,使 和已知浓度及体积的酸性
和已知浓度及体积的酸性 溶液反应进行定量分析。
溶液反应进行定量分析。Ⅲ.选择分析地点:某工业区、某公园、某居民小区、某商业区、某交通枢纽。
Ⅳ选择分析时间:晴天、风速较小时;晴天、风速较大时;雨前;雨后。
V.对测定的结果进行初步分析并向相关单位提出建议。请你参与该研究性学习小组的活动并发表你的见解:
(1)该小组的同学拟用下列装置通过方案二定量分析空气中
 的含量:
的含量:
当看到实验的现象为时
(2)下图是该小组同学根据实验测得的县城不同地区空气中
 的含量:
的含量:
①工厂区、交通枢纽
 含量明显高于其他地区的原因是;
含量明显高于其他地区的原因是;②请你向当地有关部门提出一条减少工厂区
 排放的建议:
排放的建议:(3)下表是该小组同学测得的不同天气情况下的县城空气中
 的平均含量。请你分析雨后或风速较大时
的平均含量。请你分析雨后或风速较大时 平均含量较低的原因:
平均含量较低的原因:①
②
| 天气情况 | 平均风速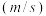 | 空气中 平均含量 平均含量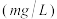 |
| 雨前 | 2.0 | 0.03 |
| 雨后 | 2.2 | 0.01 |
| 晴 | 2.3 | 0.015 |
| 晴 | 0.9 | 0.03 |
您最近一年使用:0次
名校
7 . 某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如图实验:

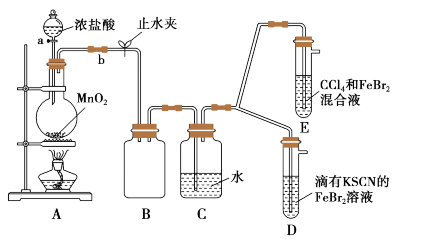
(1)①装置A中发生反应的离子方程式是__ 。
②整套实验装置存在一处明显的不足,请指出__ 。
(2)用改正后的装置进行实验,实验过程如下:
(3)因忙于观察和记录,没有及时停止反应,E中发生了新的变化 。
E装置中:CCl4层先由无色变为橙色,后颜色逐渐加深,直至变成红色。
为探究上述实验现象的本质,小组同学查得资料如下:
用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生。请结合上述资料用两步方程式 (离子或化学方程式不限定)解释产生白色沉淀原因__ 、__ 。


(1)①装置A中发生反应的离子方程式是
②整套实验装置存在一处明显的不足,请指出
(2)用改正后的装置进行实验,实验过程如下:
| 实验操作 | 实验现象 | 结论 |
| 打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后关闭活塞a,点燃酒精灯。 | D装置中:溶液变红 E装置中:水层溶液变黄,振荡后,下层CCl4层无明显变化。 | Cl2、Br2、Fe3+的氧化性由 |
E装置中:CCl4层先由无色变为橙色,后颜色逐渐加深,直至变成红色。
为探究上述实验现象的本质,小组同学查得资料如下:
| i.Cl2和Br2反应生成BrCl,BrCl呈红色,沸点约5℃,它与水能反应,且该反应为非氧化还原反应。 ii.AgClO、AgBrO均可溶于水。 iii.溴化银为淡黄色沉淀 |
您最近一年使用:0次
22-23高一上·全国·课时练习
解题方法
8 . 金属性与非金属性比较
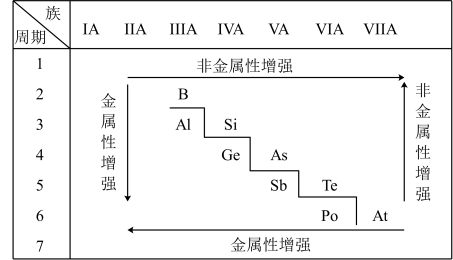
金属性强弱判断依据
(1)元素周期表位置
①同周期从左到右,金属性_________ 。
②同主族从上到下,金属性_________ 。
(2)单质及化合物相关性质
①金属单质与水或酸反应越_________ ,元素金属性_________ 。
②___________________________ 的碱性越强,元素金属性_________ 。
③离子的氧化性_________ ,对应金属元素的金属性_________ 。
(3)金属活动顺序表

非金属性强弱判断依据
(4)元素周期表位置
①同周期从左到右,非金属性________ 。
②同主族从上到下,非金属性________ 。
(5)单质及化合物相关性质
①单质越易跟H2化合,生成的氢化物也就越____ ,氢化物的还原性____ ,其非金属性也就____ 。
②最高价氧化物对应水化物的____ 越强,其非金属性越____ 。
③非金属单质间的置换反应,非金属____ 的单质能置换出非金属性____ 的单质,如卤素。
④元素的原子对应阴离子的还原性越强,元素的非金属性就_______ ,如卤素。
⑤与同一可变价金属反应,金属元素在该产物中价态越高,该非金属元素的非金属性_______ 。如S、Cl元素。

金属性强弱判断依据
(1)元素周期表位置
①同周期从左到右,金属性
②同主族从上到下,金属性
(2)单质及化合物相关性质
①金属单质与水或酸反应越
②
③离子的氧化性
(3)金属活动顺序表

非金属性强弱判断依据
(4)元素周期表位置
①同周期从左到右,非金属性
②同主族从上到下,非金属性
(5)单质及化合物相关性质
①单质越易跟H2化合,生成的氢化物也就越
②最高价氧化物对应水化物的
③非金属单质间的置换反应,非金属
④元素的原子对应阴离子的还原性越强,元素的非金属性就
⑤与同一可变价金属反应,金属元素在该产物中价态越高,该非金属元素的非金属性
您最近一年使用:0次
解题方法
9 . 回忆氮及其化合物的相关知识,完成下列各题。
(1)氮气的性质是_______
(2)下列气体中,可溶于水的无色气体是_______ ;易液化,遇挥发性酸时冒白烟,而且适宜用作制冷剂的是_______ 。
A. B.NO C.
B.NO C. D.
D.
(3)氨的喷泉实验体现了氨的哪些性质? _______
(4)在实验室里,下列试剂须储存在棕色试剂瓶中的是_______
(5)下列环境问题中,与二氧化氮的排放无关的是_______
(1)氮气的性质是_______
| A.只有氧化性 | B.只有还原性 |
| C.既有氧化性,又有还原性 | D.既没有氧化性,又没有还原性 |
A.
 B.NO C.
B.NO C. D.
D.
(3)氨的喷泉实验体现了氨的哪些性质? _______
| A.还原性 | B.极易溶于水 |
| C.与水反应生成碱性物质 | D.氨气比空气轻 |
| A.浓硝酸 | B.浓盐酸 | C.浓硫酸 | D.氯化钠 |
| A.酸雨 | B.光化学烟雾 | C.白色污染 | D.雾霾 |
您最近一年使用:0次
22-23高一上·全国·课时练习
10 . 元素周期律
(1)内容:元素的性质随着原子序数的递增而呈__________ 变化。
(2)实质:元素性质的周期性变化是元素原子的________________________ 的必然结果。
(3)同周期从左到右的结构与性质的递变性
(1)内容:元素的性质随着原子序数的递增而呈
(2)实质:元素性质的周期性变化是元素原子的
(3)同周期从左到右的结构与性质的递变性
| 原子结构 | 核电荷数 | |
| 电子层数 | ||
| 原子半径 | ||
| 性质 | 化合价 | |
| 元素的金属性和非金属性 | ||
| 离子的氧化性、还原性 | ||
| 气态氢化物的稳定性、还原性 | ||
| 最高价氧化物对应的水化物的酸碱性 |
您最近一年使用:0次



