1 . 化学物质在体育领域有广泛用途。下列说法错误 的是
| A.涤纶可作为制作运动服的材料 |
| B.纤维素可以为运动员提供能量 |
| C.木糖醇可用作运动饮料的甜味剂 |
| D.“复方氯乙烷气雾剂”可用于运动中急性损伤的镇痛 |
您最近一年使用:0次
2022-07-04更新
|
8870次组卷
|
17卷引用:2022年海南省高考真题化学试题
2022年海南省高考真题化学试题(已下线)2022年海南省高考真题变式题1-14(已下线)专题05 元素及其化合物-2022年高考真题模拟题分项汇编(已下线)考点43 合成高分子-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第35讲 生命中的基础有机化学物质 合成有机高分子(练)-2023年高考化学一轮复习讲练测(全国通用)福建省厦门集美中学2022-2023学年高三上学期10月月考化学试题(已下线)热点情景汇编-专题二 科学、技术、社会、环境中的化学(已下线)专题01 物质的组成与分类 传统文化-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题卷17 有机代表物的性质用途分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)查补易混易错02 有机化合物部分-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)(已下线)专题01 化学与STSE(已下线)专题01 化学与STSE(已下线)第10练 几种营养物质的综合考查 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)吉林省长春外国语学校2022-2023学年高二下学期6月月考化学试题吉林省长春市公主岭一中,榆树实验,九台一中,农安2022-2023学年高一下学期7月期末化学试题(已下线)考点38 合成高分子(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)河北省石家庄市第二中学2022-2023学年高三下学期2月月考化学试题
真题
2 . 镁化合物具有广泛用途,请回答有关镁的下列问题:
(1)单质镁在空气中燃烧的主要产物是白色的__ ,还生成少量的__ (填化学式)。
(2)CH3MgCl是一种重要的有机合成剂,其中镁的化合价是___ ,该化合物水解的化学方程式为___ 。
(3)如图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。
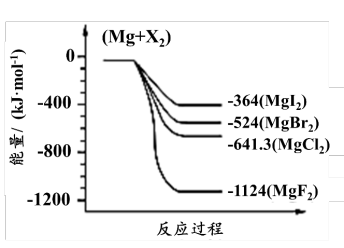
下列选项中正确的是__ (填序号)。
①MgI2中Mg2+与I-间的作用力小于MgF2中Mg2+与F-间的作用力
②Mg与F2的反应是放热反应
③MgBr2与Cl2反应的△H<0
④化合物的热稳定性顺序为MgI2>MgBr2>MgCl2>MgF2
⑤MgF2(s)+Br2(l)=MgBr2(s)+F2(g)△H=+600kJ·mol-1
(1)单质镁在空气中燃烧的主要产物是白色的
(2)CH3MgCl是一种重要的有机合成剂,其中镁的化合价是
(3)如图是金属镁和卤素反应的能量变化图(反应物和产物均为298K时的稳定状态)。

下列选项中正确的是
①MgI2中Mg2+与I-间的作用力小于MgF2中Mg2+与F-间的作用力
②Mg与F2的反应是放热反应
③MgBr2与Cl2反应的△H<0
④化合物的热稳定性顺序为MgI2>MgBr2>MgCl2>MgF2
⑤MgF2(s)+Br2(l)=MgBr2(s)+F2(g)△H=+600kJ·mol-1
您最近一年使用:0次
真题
3 . 锂是最轻的活泼金属,其单质及其化合物有广泛的用途。回答下列问题:
(1)用碳酸锂和_______ 反应可制备氯化锂,工业上可由电解LiCl-KCl的熔融混合物生产金属锂,阴极上的电极反应式为__________ 。
(2)不可使用二氧化碳灭火器扑灭因金属锂引起的火灾,其原因是__________ 。
(3)硬脂酸锂是锂肥皂的主要成分,可作为高温润滑油和油脂的稠化剂。鉴别硬脂酸锂与硬脂酸钠、硬脂酸钾可采用的实验方法和现象分别是__________ 。
(4)LiPF6易溶于有机溶剂,常用作锂离子电池的电解质。LiPF6受热易分解,其热分解产物为PF5和__________ 。
(1)用碳酸锂和
(2)不可使用二氧化碳灭火器扑灭因金属锂引起的火灾,其原因是
(3)硬脂酸锂是锂肥皂的主要成分,可作为高温润滑油和油脂的稠化剂。鉴别硬脂酸锂与硬脂酸钠、硬脂酸钾可采用的实验方法和现象分别是
(4)LiPF6易溶于有机溶剂,常用作锂离子电池的电解质。LiPF6受热易分解,其热分解产物为PF5和
您最近一年使用:0次
真题
解题方法
4 . 19-Ⅰ
下列叙述正确的有_______ 。
A.某元素原子核外电子总数是最外层电子数的5倍,则其最高正价为+7
B.钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能
C.高氯酸的酸性与氧化性均大于次氯酸的酸性和氧化性
D.邻羟基苯甲醛的熔点低于对羟基苯甲醛的熔点
19-Ⅱ
ⅣA族元素及其化合物在材料等方面有重要用途。回答下列问题:
(1)碳的一种单质的结构如图(a)所示。该单质的晶体类型为___________ ,原子间存在的共价键类型有________ ,碳原子的杂化轨道类型为__________________ 。

(2)SiCl4分子的中心原子的价层电子对数为__________ ,分子的立体构型为________ ,属于________ 分子(填“极性”或“非极性”)。
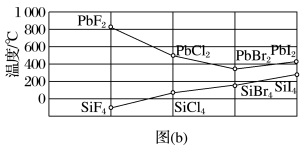
(3)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图(b)所示。
①SiX4的沸点依F、Cl、Br、I次序升高的原因是_________________ 。
②结合SiX4的沸点和PbX2的熔点的变化规律,可推断:依F、Cl、Br、I次序,PbX2中的化学键的离子性_______ 、共价性_________ 。(填“增强”“不变”或“减弱”)
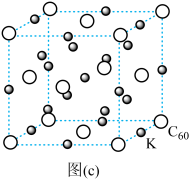
(4)碳的另一种单质C60可以与钾形成低温超导化合物,晶体结构如图(c)所示。K位于立方体的棱上和立方体的内部,此化合物的化学式为_______________ ;其晶胞参数为1.4 nm,晶体密度为_______ g·cm-3。
下列叙述正确的有
A.某元素原子核外电子总数是最外层电子数的5倍,则其最高正价为+7
B.钠元素的第一、第二电离能分别小于镁元素的第一、第二电离能
C.高氯酸的酸性与氧化性均大于次氯酸的酸性和氧化性
D.邻羟基苯甲醛的熔点低于对羟基苯甲醛的熔点
19-Ⅱ
ⅣA族元素及其化合物在材料等方面有重要用途。回答下列问题:
(1)碳的一种单质的结构如图(a)所示。该单质的晶体类型为



(2)SiCl4分子的中心原子的价层电子对数为
(3)四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图(b)所示。
①SiX4的沸点依F、Cl、Br、I次序升高的原因是
②结合SiX4的沸点和PbX2的熔点的变化规律,可推断:依F、Cl、Br、I次序,PbX2中的化学键的离子性
(4)碳的另一种单质C60可以与钾形成低温超导化合物,晶体结构如图(c)所示。K位于立方体的棱上和立方体的内部,此化合物的化学式为
您最近一年使用:0次
2017-08-08更新
|
3798次组卷
|
2卷引用:2017年全国普通高等学校招生统一考试化学(海南卷精编版)2
5 . 铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如CuSO4溶液常用作电解液、电镀液等。请回答以下问题:
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为_______ ;
(2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是_______ ;
(3) 的立体构型是
的立体构型是_______ ,其中S原子的杂化轨道类型是_______ ;
(4)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为_______ ;一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为_______ ;该晶体中,原子之间的作用力是_______ ;
(5)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF2的结构相似,该晶体储氢后的化学式应为___ 。
(1)CuSO4可由金属铜与浓硫酸反应制备,该反应的化学方程式为
(2)CuSO4粉末常用来检验一些有机物中的微量水分,其原因是
(3)
 的立体构型是
的立体构型是(4)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子最外层电子排布式为
(5)上述晶体具有储氢功能,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构为CaF2的结构相似,该晶体储氢后的化学式应为
您最近一年使用:0次
2016-12-09更新
|
758次组卷
|
3卷引用:2011年普通高等学校招生全国统一考试化学(海南卷)
2011年普通高等学校招生全国统一考试化学(海南卷)(已下线)2011-2012学年四川省雅安中学高二12月月考化学试卷河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:3.3 金属晶体



