1 . 聚氨酯类高分子材料PU用途广泛,其合成反应为:
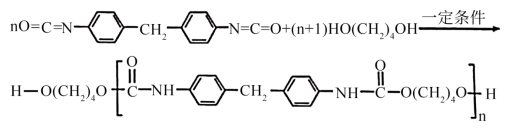
下列说法不正确的是

下列说法不正确的是
| A.HO(CH2)4OH的沸点高于CH3CH2CH2CH3 |
| B.高分子材料PU在强酸、强碱中能稳定存在 |
| C.合成PU的两种单体的核磁共振氢谱中均有3个吸收峰 |
| D.以1,3-丁二烯为原料,可合成HO(CH2)4OH |
您最近一年使用:0次
2021-07-26更新
|
552次组卷
|
17卷引用:第3章 有机合成及其应用 合成高分子化合物——C挑战区 模拟高考(鲁科版选修5)
第3章 有机合成及其应用 合成高分子化合物——C挑战区 模拟高考(鲁科版选修5)【全国区级联考】北京市西城区2018届高三二模化学试题(已下线)【全国区级联考】北京市西城区2018届高三二模理综化学试题(已下线)北京市西城高三化学二模试题福建2020届高三化学总复习专题训练——有机化学基础练习第五章 进入合成有机高分子化合物的时代—— C 挑战区 模拟高考(人教版选修5)北京市中国人民大学附属中学 2020届高三下学期第三次模拟化学试题(已下线)考点43 合成高分子-备战2023年高考化学一轮复习考点帮(全国通用)北京市第十中学2022-2023学年高三上学期等级考适应性练习(三模)化学试题第五章 合成高分子(B卷·能力提升练)-2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修3)【全国百强校】辽宁省沈阳市东北育才学校2017-2018学年高二下学期第二阶段考试化学试题浙江省宁波市咸祥中学2019-2020学年高二下学期期中考试化学试题(已下线)【浙江新东方】高中化学20210513-005【2021】【高二下】(鲁科版2019)选3第3章 C高考挑战区内蒙古赤峰市2020-2021学年高二下学期期末考试化学(A)试题重庆实验中学2020-2021学年高二下学期第二阶段测试化学试题河南省南阳市第一中学校2022-2023学年高二下学期5月月考化学试题
名校
解题方法
2 . 钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Ti的基态原子价电子排布式为________________ 。
②Fe的基态原子共有________ 种不同能级的电子。
(2)制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KCl+2CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由大到小的顺序是____________________ (用元素符号表示)。
②COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为________ ,中心原子的杂化方式为________ 。
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为6.9×10-2nm和7.8×10-2nm。则熔点:NiO________ (填“>”、“<”或“=”)FeO。
(4)Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。
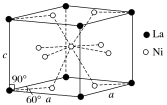
①该晶体的化学式为________________ 。
②已知该晶胞的摩尔质量为Mg·mol-1,密度为dg·cm-3。设NA为阿伏加德罗常数的值,则该晶胞的体积是________ cm3(用含M、d、NA的代数式表示)。
③该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较稳定。已知:a=511pm,c=397pm;标准状况下氢气的密度为8.98×10-5g·cm-3;储氢能力= 。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为
。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为________ 。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Ti的基态原子价电子排布式为
②Fe的基态原子共有
(2)制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KCl+2CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由大到小的顺序是
②COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为6.9×10-2nm和7.8×10-2nm。则熔点:NiO
(4)Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。

①该晶体的化学式为
②已知该晶胞的摩尔质量为Mg·mol-1,密度为dg·cm-3。设NA为阿伏加德罗常数的值,则该晶胞的体积是
③该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较稳定。已知:a=511pm,c=397pm;标准状况下氢气的密度为8.98×10-5g·cm-3;储氢能力=
 。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为
。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为
您最近一年使用:0次
2020-11-12更新
|
346次组卷
|
13卷引用:苏教版2017届高三单元精练检测十一化学试题
苏教版2017届高三单元精练检测十一化学试题2016届河北省晋州一中高三上学期期末理综化学试卷2016届安徽省安庆一中高三热身考试理综化学试卷2016届湖北省襄阳五中高三5月模拟三理综化学试卷2017届安徽省黄山市屯溪一中高三上月考二化学卷四川省内江市2017届高三第五次模拟考试理综化学试题陕西省师范大学附属中学2017届高三下学期第十一次模考理综化学试题湖北省孝感市八校2018届高三上学期期末考试理综化学试题(已下线)2018年6月1日 押高考化学第35题(2)——《每日一题》2018年高三化学四轮复习(已下线)解密21 物质的结构与性质(教师版)——备战2018年高考化学之高频考点解密(已下线)2019年5月31日《每日一题》四轮复习—— 押高考化学第35题(2)四川省成都附属实验中学2021届高三上学期11月月考理科综合化学试题(已下线)第三单元 物质的聚集状态性质与物质性质(能力提升)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)
3 . 硫及其化合物有许多用途,相关物质的物理常数如下表所示:
回答下列问题:
(1)根据价层电子对互斥理论, 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是__________ 。
(2)气态三氧化硫以单分子形式存在,其分子的立体构型为__________ 形,其中共价键的类型有__________ 种;固体三氧化硫中存在如图所示的三聚分子,该分子中 原子的杂化轨道类型为
原子的杂化轨道类型为__________ 。

 |  |  |  |  |  | |
| 熔点/℃ | -85.5 | 115.2 | >600 | -75.5 | 16.8 | 10.3 |
| 沸点/℃ | -60.3 | 444.6 | (分解) | -10.0 | 45.0 | 337.0 |
回答下列问题:
(1)根据价层电子对互斥理论,
 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是(2)气态三氧化硫以单分子形式存在,其分子的立体构型为
 原子的杂化轨道类型为
原子的杂化轨道类型为
您最近一年使用:0次
解题方法
4 . 现有四种短周期元素的有关信息如表所示:
则甲、乙、丙、丁四种元素的原子序数从大到小的排列顺序为
| 元素 | 结构特点及在周期表中的位置 | 单质及化合物的部分性质与用途 |
| 甲 | 在元素周期表中,主族序数等于周期序数 | 工业上用电解法冶炼金属 |
| 乙 | 原子最外层电子数是次外层电子数的一半 | 氧化物是工业制普通玻璃的主要原料 |
| 丙 | 原子最外层电子数是最内层电子数的2倍 | 单质存在多种同素异形体 |
| 丁 | 元素能形成两种不同的阴离子 | 丁的一种单质与 溶液反应生成丁的另一种单质 溶液反应生成丁的另一种单质 |
| A.甲、乙、丙、丁 |
| B.丁、甲、乙、丙 |
| C.丙、丁、甲、乙 |
| D.乙、甲、丁、丙 |
您最近一年使用:0次
5 . 现四种短周期元素的有关信息如表所示:
则甲、乙、丙、丁四种元素的原子序数从大到小的排列顺序为( )。
| 元素 | 结构特点及在周期表中的位置 | 单质及化合物的部分性质与用途 |
| 甲 | 在元素周期表中,主族序数等于周期序数 | 工业上用电解法冶炼该金属 |
| 乙 | 原子最外层电子数是次外层电子数的一半 | 氧化物是工业制普通玻璃的主要原料 |
| 丙 | 原子最外层电子数是最内层电子数的2倍 | 单质存在多种同素异形体 |
| 丁 | 元素能形成两种不同的单质 | 丁的一种单质与 溶液反应生成丁的另一种单质 溶液反应生成丁的另一种单质 |
| A.甲、乙、丙、丁 | B.丁、甲、乙、丙 |
| C.丙、丁、甲、乙 | D.乙、甲、丁、丙 |
您最近一年使用:0次
真题
名校
6 . 绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:______________ 、_______________ 。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。

①仪器B的名称是____________________ 。
②将下列实验操作步骤正确排序___________________ (填标号);重复上述操作步骤,直至A恒重,记为m3 g。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=________________ (列式表示)。若实验时按a、d次序操作,则使x__________ (填“偏大”“偏小”或“无影响”)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。
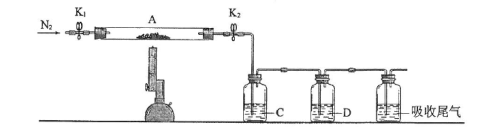
①C、D中的溶液依次为_________ (填标号)。C、D中有气泡冒出,并可观察到的现象分别为_______________ 。
a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 e.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式_____________________ 。
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为 m2 g。按下图连接好装置进行实验。

①仪器B的名称是
②将下列实验操作步骤正确排序
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

①C、D中的溶液依次为
a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 e.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式
您最近一年使用:0次
2017-08-08更新
|
9219次组卷
|
30卷引用:百所名校联考-金属及其化合物
百所名校联考-金属及其化合物2017年全国普通高等学校招生统一考试理综化学(新课标Ⅲ卷精编版)江西省上高二中2018届高三上学期第三次月考化学试题(已下线)《考前20天终极攻略》-5月27日 综合实验设计、探究和评价(已下线)解密18 物质的制备、实验方案的设计与评价——备战2018年高考化学之高频考点解密吉林省延边市第二中学2020届高三入学考试化学试题2020届高考化学二轮复习大题精准训练——定量分析化学实验中物质含量的测定2020届高考化学二轮复习大题精准训练——化学实验方案的设计及评价河北省衡水中学2020届高三四月份质量监测理综化学试题湖南省长沙市长郡中学2020届高三4月份教学质量监测理综化学试题(已下线)广东省深圳中学2020届高三3月份教学质量监测卷理综化学试题河北省石家庄市第二中学2020届高中毕业班二月份网络教学质量监测卷理科综合化学部分河南省郑州市第一中学2020年高中毕业班教学质量监测卷理科综合化学试题2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分贵州省贵阳市第一中学2020届高三教学质量监测理科综合化学试题湖南省长沙市雅礼中学2020届高三5月高考化学模拟试卷(已下线)专题讲座(三)“铁三角”综合实验题解题策略(精讲)——2021年高考化学一轮复习讲练测福建省福州市第二中学2021届高三上学期第一次月考化学试题云南省保山第九中学2021届高三上学期开学考试化学试题云南省玉溪师范学院附属中学2021-2022学年高三 上学期期末考试化学试题(已下线)【教材实验热点】04 Fe(OH)2与Fe(OH)3胶体的制备云南省普洱市第一中学2021-2022学年高三下学期3月份考试理综化学试题(已下线)专题26 定量测定类综合性实验题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型31 Fe2+、Fe3+的检验与性质探究安徽省六安市第一中学2017-2018学年高二上学期开学考试化学试题四川省双流中学2017-2018学年高二上学期开学考试化学试题安徽省黄山市屯溪第一中学2019-2020学年高二上学期入学摸底考试化学试题山东济南市历城第二中学2020-2021学年高二上学期开学考试化学试题高一必修第一册(鲁科2019)第3章 第2节 硫的转化 高考帮(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第一节 硫及其化合物
7 . Ⅰ.X、Y、Z、M、N为短周期的五种主族元素,其中X、Z同主族,Y、Z同周期,M与X、Y既不同族,也不同周期。X原子最外层电子数是核外电子层数的三倍,Y的最高化合价与其最低化合价
的代数和等于6。N是短周期主族元素中原子半径最大的非金属元素。
(1)请写出M的元素符号:____________ ,Z的原子结构示意图:_____________ 。M与X两元素可形成两种液态化合物,其化学式分别为________________________ 。
(2)请写出N元素在周期表中的位置:___________________________ ;与N同族的短周期元素L,其最高价氧化物的电子式为_______________________ 。
(3)Y与Z相比,非金属性较强的元素是__________ (填元素符号),可以证明该结论的实验事实是_________________________________________________________________ 。
Ⅱ.下列转化关系中,X、Y是生活中用途广泛的两种金属单质,A、B是氧化物,A为红棕色固体,C、D、E是中学常见的三种化合物。请根据转化关系回答下列问题。
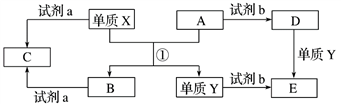
(1)请写出反应①的化学方程式:_____________________________________ 。
(2)由D到E的离子方程式:__________________ 。
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式:__________________________________________________________________ 。
(4)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制取高效净水剂Y(OH)SO4,已知还原产物为NO,则该反应的化学方程式是______________________________ 。
的代数和等于6。N是短周期主族元素中原子半径最大的非金属元素。
(1)请写出M的元素符号:
(2)请写出N元素在周期表中的位置:
(3)Y与Z相比,非金属性较强的元素是
Ⅱ.下列转化关系中,X、Y是生活中用途广泛的两种金属单质,A、B是氧化物,A为红棕色固体,C、D、E是中学常见的三种化合物。请根据转化关系回答下列问题。

(1)请写出反应①的化学方程式:
(2)由D到E的离子方程式:
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式:
(4)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制取高效净水剂Y(OH)SO4,已知还原产物为NO,则该反应的化学方程式是
您最近一年使用:0次
名校
解题方法
8 . A、B、C、D、E、W为六种前四周期元素,它们的原子序数依次增大. A 与 D 同主族,可形成 DA 型离子化合物,B与C同周期且相邻,C与E同主族,E2-与 Ar 原子具有相同的电子层结构,W 的合金用量最大、用途最广.请回答下列问题:
(1)D 在元素周期表中的位置___________ .
(2)A 分别与 C、E 形成最简单化合物中沸点较高的是________ (填化学式),原因是____________ .
(3)A、C、D三种元素形成的物质中含有的化学键类型______ ,灼热的碳能与 B 的最高价氧化物对应水化物的浓溶液反应,化学反应方程式为_____________ .
(4)向盛有A2C2 溶液的试管中加入几滴酸化的WEC4 溶液,溶液变成棕黄色,发生反应的离子方程式为____________ ;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成,产生气泡的原因是_______ ;生成沉淀的原因是____________ (用平衡移动原理解释).
(1)D 在元素周期表中的位置
(2)A 分别与 C、E 形成最简单化合物中沸点较高的是
(3)A、C、D三种元素形成的物质中含有的化学键类型
(4)向盛有A2C2 溶液的试管中加入几滴酸化的WEC4 溶液,溶液变成棕黄色,发生反应的离子方程式为
您最近一年使用:0次
2017-02-17更新
|
460次组卷
|
6卷引用:苏教版2017届高三单元精练检测五化学试题
2011·江西·二模
9 . 已知X、Y和Z三种元素的原子序数之和等于48。X的一种1∶1型氢化物分子中既有σ键又有π键。Z是金属元素,Z的单质和化合物有广泛的用途。已知Z的核电荷数小于28,且次外层有2个未成对电子。工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐)。M有显著的“压电性能”,应用于超声波的发生装置。经X射线分析,M晶体的最小重复单元为正方体(如图),边长为4.03×10-10 m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占。
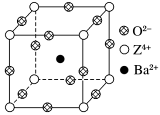
(1) Y在周期表中位于______________ ;Z4+的核外电子排布式为___________________ 。
(2)X的该种氢化物分子构型为________ ,X在该氢化物中以_______ 方式杂化。X和Y形成的化合物的熔点应该_______ (填“高于”或“低于”)X的氢化物的熔点。
(3)①制备M的化学方程式是_____________ 。
②在M晶体中,若将Z4+置于正方体的体心,Ba2+置于正方体的顶点,则O2-处于正方体的________ 。
③在M晶体中,Z4+的氧配位数为________ 。
④已知O2-半径为1.40×10-10 m,则Z4+半径为____ m。

(1) Y在周期表中位于
(2)X的该种氢化物分子构型为
(3)①制备M的化学方程式是
②在M晶体中,若将Z4+置于正方体的体心,Ba2+置于正方体的顶点,则O2-处于正方体的
③在M晶体中,Z4+的氧配位数为
④已知O2-半径为1.40×10-10 m,则Z4+半径为
您最近一年使用:0次
2016-12-09更新
|
1125次组卷
|
5卷引用:苏教版2017届高三单元精练检测十一化学试题
苏教版2017届高三单元精练检测十一化学试题(已下线)2011届江西省重点中学协作体高三第二次联考(理综)化学部分山东省章丘市第四中学2019届高三上学期第二次质量检测理综化学试题黑龙江省齐齐哈尔市第八中学2017-2018学年高二6月月考化学试题新疆奎屯市第一高级中学2018-2019学年高二下学期第一次月考化学试题



