1 . 二糖
(1)物理性质和存在
①蔗糖为___________ 晶体,___________ 溶于水,是自然界中分布最广的一种___________ ,存在于大多数植物体中,在___________ 和___________ 中含量最丰富。
②麦芽糖有甜味但不及蔗糖,主要存在于发芽的___________ 和___________ 中,可制___________ 。
③乳糖主要存在于哺乳动物的___________ 中,经发酵产生___________ 。
(2)化学性质
①C12H22O11(蔗糖)+H2O C6H12O6
C6H12O6_______ +C6H12O6________
②C12H22O11(麦芽糖)+H2O 2C6H12O6
2C6H12O6________
③实验探究——糖类的还原性
由此可见,蔗糖和麦芽糖互为同分异构体。
(1)物理性质和存在
①蔗糖为
②麦芽糖有甜味但不及蔗糖,主要存在于发芽的
③乳糖主要存在于哺乳动物的
(2)化学性质
①C12H22O11(蔗糖)+H2O
 C6H12O6
C6H12O6②C12H22O11(麦芽糖)+H2O
 2C6H12O6
2C6H12O6③实验探究——糖类的还原性
| 实验步骤 | 实验现象 | 实验结论 |
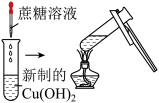 | 试管内无明显现象 | 蔗糖分子中无 |
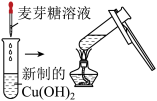 | 试管内产生砖红色沉淀 |
由此可见,蔗糖和麦芽糖互为同分异构体。
您最近一年使用:0次
2 . 金属元素的原子结构决定了金属元素的性质、在自然界中的存在形式及冶炼方法。
(1)金属的冶炼一般有下列方法:
a.焦炭法
b.水煤气(氢气和一氧化碳)法
c.活泼金属置换法
d.电解法
请从上述四种方法中选择相应的字母填入表中空格:
写出Al与Cr2O3反应的化学方程式:__________ 。
(2)铜在地壳中的含量远低于铝,但人类利用铜的历史远早于铝,这与古代发生的森林大火有一定的关系,因为人类在大火之后的灰烬中会发现红色发亮的物质。现在人们认识到,这种物质就是孔雀石[主要成分为Cu2(OH)2CO3,热稳定性差]在大火中转化而生成的铜,写出大火中与铜元素有关的三个化学方程式:______ 。
(1)金属的冶炼一般有下列方法:
a.焦炭法
b.水煤气(氢气和一氧化碳)法
c.活泼金属置换法
d.电解法
请从上述四种方法中选择相应的字母填入表中空格:
高炉炼铁 | 湿法炼铜 | 铝热法炼铬 | 工业上冶炼铝 |
(2)铜在地壳中的含量远低于铝,但人类利用铜的历史远早于铝,这与古代发生的森林大火有一定的关系,因为人类在大火之后的灰烬中会发现红色发亮的物质。现在人们认识到,这种物质就是孔雀石[主要成分为Cu2(OH)2CO3,热稳定性差]在大火中转化而生成的铜,写出大火中与铜元素有关的三个化学方程式:
您最近一年使用:0次
3 . CH4和Cl2发生取代反应的产物中,CH3Cl的含量最多。(_____)
您最近一年使用:0次
2022-03-02更新
|
230次组卷
|
2卷引用:课前-7.1.2 烷烃的性质-人教2019必修第二册
4 . 酸雨的危害及防治
(1)酸雨的危害
①直接______ 农作物,破坏森林和草原,使土壤、湖泊_____ 。
②加速建筑物、桥梁、工业设备、运输工具和电缆的_____ 。
③导致地下水中重金属元素含量增加,污染水源,危害人体健康。
(2)酸雨的防治
①消除_______ ,改变能源结构,开发利用清洁能源,如太阳能、风能、氢能等。
②对_________ 的排放加以控制,如燃料脱硫处理,废气中二氧化硫回收利用、控制汽车尾气排放等。
③健全法律法规,严格规定污染物的排放标准,提高环境保护意识。
(1)酸雨的危害
①直接
②加速建筑物、桥梁、工业设备、运输工具和电缆的
③导致地下水中重金属元素含量增加,污染水源,危害人体健康。
(2)酸雨的防治
①消除
②对
③健全法律法规,严格规定污染物的排放标准,提高环境保护意识。
您最近一年使用:0次
5 . I.燃煤的烟气中含有SO2,为治理雾霾天气,工厂采用多种方法实现烟气脱硫。
(1)“湿式吸收法”利用吸收剂与SO2发生反应从而脱硫,下列试剂中适合用作该法吸收剂的是____ (填字母序号)。
II.某工厂利用工业废碱渣(主要成分为Na2CO3)来吸收燃煤烟气中含有的SO2,还可以得到亚硫酸钠粗品。其流程如图:____ 。
(3)要提高SO2吸收效率的可行措施有____ (填数字序号)。
①加快烟气的通入速率
②将吸收液Na2CO3溶液进行雾化
③在高温条件下吸收
④适当增加Na2CO3的浓度
(4)上述流程中,加入NaOH后,发生的化学方程式是____ 。
(5)亚硫酸钠粗品中含有少量Na2SO4,原因是____ ,设计实验证明亚硫酸钠粗品含有少量Na2SO4的方案是:在一支试管中,加入少量亚硫酸钠粗品,用适量蒸馏水溶解,____ ,出现白色沉淀,则证明含有Na2SO4。
(6)已知有VL(已换算成标准状况)烟气(SO2),通入足量H2O2吸收,再加足量BaCl2溶液充分反应后(不考虑气中其他成分的反应),过滤、洗涤、干燥、称量得到Wg沉淀。烟气中SO2的含量(体积分数)的计算式是____ 。
(1)“湿式吸收法”利用吸收剂与SO2发生反应从而脱硫,下列试剂中适合用作该法吸收剂的是
| A.石灰乳 | B.Na2SO3溶液 | C.NaOH溶液 | D.CaCl2溶液 |
II.某工厂利用工业废碱渣(主要成分为Na2CO3)来吸收燃煤烟气中含有的SO2,还可以得到亚硫酸钠粗品。其流程如图:
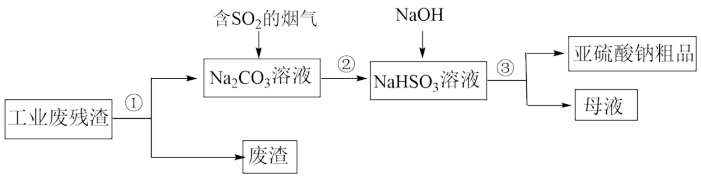
(3)要提高SO2吸收效率的可行措施有
①加快烟气的通入速率
②将吸收液Na2CO3溶液进行雾化
③在高温条件下吸收
④适当增加Na2CO3的浓度
(4)上述流程中,加入NaOH后,发生的化学方程式是
(5)亚硫酸钠粗品中含有少量Na2SO4,原因是
(6)已知有VL(已换算成标准状况)烟气(SO2),通入足量H2O2吸收,再加足量BaCl2溶液充分反应后(不考虑气中其他成分的反应),过滤、洗涤、干燥、称量得到Wg沉淀。烟气中SO2的含量(体积分数)的计算式是
您最近一年使用:0次
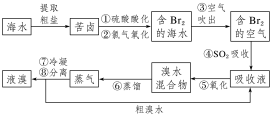
6 . 海水中化学资源的开发利用
(1)海水中溶解和悬浮着大量的____ 和____ 。海水中含量最多的____ 两种元素,加上Cl、Na、Mg、S、Ca、K、Br、C、Sr、B、F元素,其总含量超过99%,其他元素为____ 。虽然海水中元素的种类很多,总储量____ ,但许多元素的富集程度却____ 。
(2)海水制盐从海水中制得的氯化钠,可以食用,同时也是生产烧碱、纯碱、钠、氯气、盐酸等的化工原料。
①氯碱工业:电解饱和食盐水,可生产氢氧化钠、氢气和氯气。
化学反应方程式:______ 。
②制钠和氯气:______ 。
③制盐酸:________ 。
④制漂白剂(84消毒液):_______ 。
⑤制纯碱:__________ ;_________ 。
(3)海水提溴
①海水提溴的方法(吹出法)
②氧化、吸收环节主要离子方程式:2Br-+Cl2=Br2+2Cl-、SO2+Br2+2H2O=4H++SO +2Br-。
+2Br-。
(1)海水中溶解和悬浮着大量的
(2)海水制盐从海水中制得的氯化钠,可以食用,同时也是生产烧碱、纯碱、钠、氯气、盐酸等的化工原料。
①氯碱工业:电解饱和食盐水,可生产氢氧化钠、氢气和氯气。
化学反应方程式:
②制钠和氯气:
③制盐酸:
④制漂白剂(84消毒液):
⑤制纯碱:
(3)海水提溴
①海水提溴的方法(吹出法)
| 工艺流程 |
| |
基本操作 | 浓缩 | 海水晒盐和海水淡化的过程中副产物Br-得到浓缩 |
氧化 | 向浓缩的海水中通入Cl2,将Br-氧化成Br2 | |
吹出 | 利用溴的挥发性,通入热空气和水蒸气,吹出溴蒸气 | |
吸收 | 吹出的溴蒸气用SO2吸收 | |
蒸馏 | 再用Cl2将HBr氧化得到产品溴后蒸馏分离 | |
②氧化、吸收环节主要离子方程式:2Br-+Cl2=Br2+2Cl-、SO2+Br2+2H2O=4H++SO
 +2Br-。
+2Br-。
您最近一年使用:0次
7 . 石油裂解
定义:在石油化工生产中,常以_______ 为原料,采用比裂化更高的温度(700~800 ℃,有时甚至高达1 000 ℃以上),使石油分馏产品中相对分子质量较大的烃分解成_______ 等小分子烃的加工过程。
目的:获得_______ 等有机化工原料。其中,石油的裂解气中,_______ 的含量比较高。
定义:在石油化工生产中,常以
目的:获得
您最近一年使用:0次
8 . 同分异构体之间最简式、相对分子质量、各元素的百分含量、熔沸点一定都相同吗____ ?
您最近一年使用:0次
9 . 合成氨反应的限度
(1)合成氨反应的特点
(2)影响因素
①外界条件:_______ 温度、_______ 压强,有利于化学平衡向合成氨的方向移动。
②投料比:温度压强一定时, 、
、 的体积比为
的体积比为_______ 时平衡混合物中氨的百分含量最高。
(1)合成氨反应的特点
| 合成氨反应 | ——可逆性:反应为 |
| ——体积变化:正反应是气体体积 | |
——焓变:  | |
——常温下自发性: , , |
(2)影响因素
①外界条件:
②投料比:温度压强一定时,
 、
、 的体积比为
的体积比为
您最近一年使用:0次
10 . 海水中含量最多的两种元素为Na元素和Cl元素。(____)
您最近一年使用:0次