1 . 某化学小组拟设计实验探究 与钙盐溶液的反应情况。
与钙盐溶液的反应情况。
【文献资料】① 是难溶于水、易溶于盐酸的白色固体:②实验室用
是难溶于水、易溶于盐酸的白色固体:②实验室用 粉末和70%硫酸反应制备
粉末和70%硫酸反应制备 ;③浓硫酸与水混合时放出大量的热,产生大量“酸雾”。
;③浓硫酸与水混合时放出大量的热,产生大量“酸雾”。
【设计实验】
实验Ⅰ:探究二氧化硫与氯化钙溶液反应。___________ (填代号)。
(2)D装置作用是___________ (用离子方程式表示)。
(3)连接装置进行实验,发现C装置中产生白色沉淀。
①甲同学对白色沉淀成分提出如下假设:
假设1:白色固体是 ;
;
假设2:白色固体是 ;
;
假设3:白色固体是 和
和 。
。
②乙同学设计实验证明白色沉淀是 ,他的实验方案是
,他的实验方案是___________ 。
③丙同学认为C中生成硫酸钙的原因是装置内 氧化了
氧化了 。
。
排除装置内 干扰采取的措施是:在启动B中反应之前,
干扰采取的措施是:在启动B中反应之前,___________ (填实验步骤)
重新实验,C中无明显现象,所以 和
和 溶液不反应。
溶液不反应。
实验Ⅱ:探究 和
和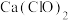 溶液反应。
溶液反应。
丁同学仅将上述实验C装置中氯化钙溶液换成漂白精溶液,进行实验时产生了大量白色沉淀。
(4)化学反应有两种情况。
①若 过量,则发生反应为
过量,则发生反应为
②若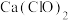 过量,则发生反应为
过量,则发生反应为___________ 。
(5)为了探究C中 是否过量,戊同学取少量c中上层清液于试管中,加入下列物质可以达到实验目的的是
是否过量,戊同学取少量c中上层清液于试管中,加入下列物质可以达到实验目的的是___________ (填字母)。
a.品红溶液 b. 溶液 c.紫色石蕊溶液
溶液 c.紫色石蕊溶液
 与钙盐溶液的反应情况。
与钙盐溶液的反应情况。【文献资料】①
 是难溶于水、易溶于盐酸的白色固体:②实验室用
是难溶于水、易溶于盐酸的白色固体:②实验室用 粉末和70%硫酸反应制备
粉末和70%硫酸反应制备 ;③浓硫酸与水混合时放出大量的热,产生大量“酸雾”。
;③浓硫酸与水混合时放出大量的热,产生大量“酸雾”。【设计实验】
实验Ⅰ:探究二氧化硫与氯化钙溶液反应。
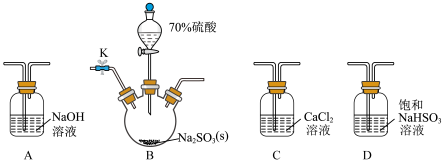
(2)D装置作用是
(3)连接装置进行实验,发现C装置中产生白色沉淀。
①甲同学对白色沉淀成分提出如下假设:
假设1:白色固体是
 ;
;假设2:白色固体是
 ;
;假设3:白色固体是
 和
和 。
。②乙同学设计实验证明白色沉淀是
 ,他的实验方案是
,他的实验方案是③丙同学认为C中生成硫酸钙的原因是装置内
 氧化了
氧化了 。
。排除装置内
 干扰采取的措施是:在启动B中反应之前,
干扰采取的措施是:在启动B中反应之前,重新实验,C中无明显现象,所以
 和
和 溶液不反应。
溶液不反应。实验Ⅱ:探究
 和
和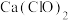 溶液反应。
溶液反应。丁同学仅将上述实验C装置中氯化钙溶液换成漂白精溶液,进行实验时产生了大量白色沉淀。
(4)化学反应有两种情况。
①若
 过量,则发生反应为
过量,则发生反应为
②若
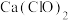 过量,则发生反应为
过量,则发生反应为(5)为了探究C中
 是否过量,戊同学取少量c中上层清液于试管中,加入下列物质可以达到实验目的的是
是否过量,戊同学取少量c中上层清液于试管中,加入下列物质可以达到实验目的的是a.品红溶液 b.
 溶液 c.紫色石蕊溶液
溶液 c.紫色石蕊溶液
您最近一年使用:0次
2 . 科学探究要实事求是、严谨细致。某化学兴趣小组设计实验进行有关氯化物的探究实验,回答下列问题:
Ⅰ.FeCl3在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了以Fe粉和Cl2为原料制备无水FeCl3的实验方案,装置示意图如下:___________ 。
(2)装置A中设计g管的作用是___________ 。
(3)装置A中发生反应的离子方程式为___________ 。
Ⅱ.利用惰性电极电解0.1mol/LFeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
实验数据如表所示:
(4)由实验1、2现象可以得出结论:增大pH,___________ 优先于___________ 放电;
Ⅲ.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol/L硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量X”是___________ ;
②为了探究浓度对氯化铵水解平衡的影响,实验6可与实验___________ 作对照实验;
③实验目的ii是___________ ;
④氯化铵在生产生活中有很多实用的用途,请写出一种应用:___________ 。
Ⅰ.FeCl3在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了以Fe粉和Cl2为原料制备无水FeCl3的实验方案,装置示意图如下:
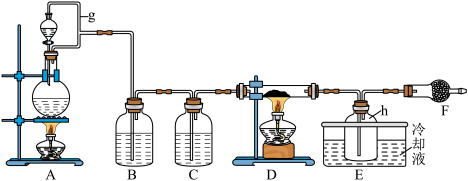
(2)装置A中设计g管的作用是
(3)装置A中发生反应的离子方程式为
Ⅱ.利用惰性电极电解0.1mol/LFeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
实验数据如表所示:
| 实验编号 | 电压/V | pH | 阳极现象 | 阴极现象 |
| 1 | 1.5 | 1.00 | 无气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
| 2 | 1.5 | 5.52 | 无气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
| 3 | 3.0 | 5.52 | 少量气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
| 4 | 4.5 | 5.52 | 大量气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
(4)由实验1、2现象可以得出结论:增大pH,
Ⅲ.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
| 实验编号 | c(NH4Cl)/mol·L-1 | 温度/℃ | 待测物理量X | 实验目的 |
| 5 | 0.5 | 30 | a | ___________ |
| 6 | 1.5 | i | b | 探究浓度对氯化铵水解平衡的影响 |
| 7 | 1.5 | 35 | c | ii |
| 8 | 2.0 | 40 | d | 探究温度、浓度同时对氯化铵化解平衡的影响 |
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol/L硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量X”是
②为了探究浓度对氯化铵水解平衡的影响,实验6可与实验
③实验目的ii是
④氯化铵在生产生活中有很多实用的用途,请写出一种应用:
您最近一年使用:0次
名校
解题方法
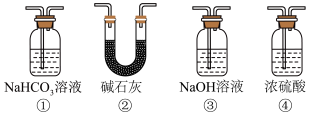
3 . 化学兴趣小组为研究 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。

(1)装置I中仪器c的名称是___________ 。
(2)实验结束后,同学们在装置Ⅲ中观察到 的红色褪去,但并未观察到“a无明显变化”这一预期现象。为达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加下图中的
的红色褪去,但并未观察到“a无明显变化”这一预期现象。为达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加下图中的___________ (填序号)装置。
(3)若产生的 足量,装置Ⅳ中的实验现象是
足量,装置Ⅳ中的实验现象是___________ 。
(4)写出装置V中发生反应的离子方程式___________ 。
(5)将制得的氯气通入如图装置可制备无水 ,已知
,已知 在
在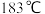 升华,遇潮湿空气立即产生大量白雾。
升华,遇潮湿空气立即产生大量白雾。

①实验开始时应先___________ (填“通入氯气”或“点燃酒精灯”)。
②用粗短导管连接A、B的目的是___________ 。C中碱石灰的作用是___________ 。
③若制备氯气时消耗 为
为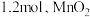 和铝粉均足量,所得产品
和铝粉均足量,所得产品 经纯化后测得质量为
经纯化后测得质量为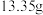 ,则该实验中
,则该实验中 的产率为
的产率为___________ ( )。
)。
(6)若将 通入热的烧碱溶液中,可以得到
通入热的烧碱溶液中,可以得到 和
和 的混合液。当混合液中
的混合液。当混合液中 和
和 的个数比为
的个数比为 时,混合液中
时,混合液中 和
和 的个数比为
的个数比为___________ 。
 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
(1)装置I中仪器c的名称是
(2)实验结束后,同学们在装置Ⅲ中观察到
 的红色褪去,但并未观察到“a无明显变化”这一预期现象。为达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加下图中的
的红色褪去,但并未观察到“a无明显变化”这一预期现象。为达到这一实验目的,你认为还需在装置Ⅱ与Ⅲ之间添加下图中的
(3)若产生的
 足量,装置Ⅳ中的实验现象是
足量,装置Ⅳ中的实验现象是(4)写出装置V中发生反应的离子方程式
(5)将制得的氯气通入如图装置可制备无水
 ,已知
,已知 在
在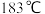 升华,遇潮湿空气立即产生大量白雾。
升华,遇潮湿空气立即产生大量白雾。
①实验开始时应先
②用粗短导管连接A、B的目的是
③若制备氯气时消耗
 为
为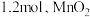 和铝粉均足量,所得产品
和铝粉均足量,所得产品 经纯化后测得质量为
经纯化后测得质量为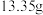 ,则该实验中
,则该实验中 的产率为
的产率为 )。
)。(6)若将
 通入热的烧碱溶液中,可以得到
通入热的烧碱溶液中,可以得到 和
和 的混合液。当混合液中
的混合液。当混合液中 和
和 的个数比为
的个数比为 时,混合液中
时,混合液中 和
和 的个数比为
的个数比为
您最近一年使用:0次
4 . NaCl是一种化工原料,可以制备多种物质,如下图所示。回答下列问题:
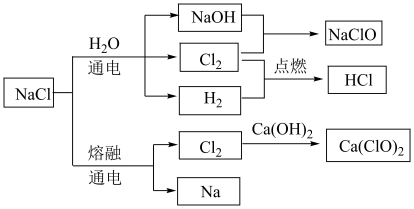
(1)蘸取NaCl溶液在酒精灯上灼烧,可观察到火焰呈________________ 色。
(2)氯化钠溶液通电后,发生反应的化学反应方程式为________________ 。
(3)Cl2与Ca(OH)2溶液发生反应的化学反应方程式为________________ 。
(4)如图表示NaCl固体在水中溶解过程的微观状态示意图,下列说法中,正确的是________ 。

a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.进入水中,NaCl固体形成能够自由移动的水合钠离子和水合氯离子
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
d.加热至熔融状态的NaCl也可以解离出自由移动的Na+和Cl-
(5)某小组同学为探究Cl2的性质并制备氯水,用如图所示装置进行实验。部分夹持装置已略去,其中a为干燥的有色布条,b为湿润的有色布条。
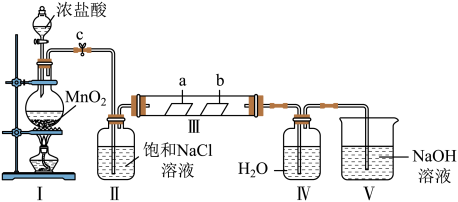
①加入药品前,应进行的实验操作是________________ 。
②实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,可采取的方法是________________ 。
③装置V中NaOH溶液的作用是________________ 。
④用强光照射氯水,并用传感器进行数据采集,获得相关变化曲线如下图。图中纵坐标可表示的物理量是_____ 。
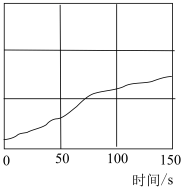
a.氯离子浓度 b.溶液中氯气的含量
c.pH d.氧气体积分数

(1)蘸取NaCl溶液在酒精灯上灼烧,可观察到火焰呈
(2)氯化钠溶液通电后,发生反应的化学反应方程式为
(3)Cl2与Ca(OH)2溶液发生反应的化学反应方程式为
(4)如图表示NaCl固体在水中溶解过程的微观状态示意图,下列说法中,正确的是

a.干燥的NaCl固体不导电,是由于其中不存在Na+和Cl-
b.进入水中,NaCl固体形成能够自由移动的水合钠离子和水合氯离子
c.NaCl溶液能导电,是由于在电流作用下,其可解离出自由移动的Na+和Cl-
d.加热至熔融状态的NaCl也可以解离出自由移动的Na+和Cl-
(5)某小组同学为探究Cl2的性质并制备氯水,用如图所示装置进行实验。部分夹持装置已略去,其中a为干燥的有色布条,b为湿润的有色布条。

①加入药品前,应进行的实验操作是
②实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,可采取的方法是
③装置V中NaOH溶液的作用是
④用强光照射氯水,并用传感器进行数据采集,获得相关变化曲线如下图。图中纵坐标可表示的物理量是

a.氯离子浓度 b.溶液中氯气的含量
c.pH d.氧气体积分数
您最近一年使用:0次
名校
5 . 利用下列装置和试剂进行实验,设计合理且能达到实验目的的是
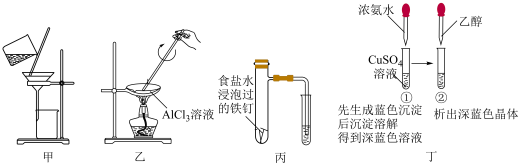
A.甲装置可分离 胶体和 胶体和 溶液 溶液 |
B.乙装置可制备无水 固体 固体 |
| C.丙装置可探究铁的析氢腐蚀 |
D.丁装置中现象可证明与 结合能力: 结合能力: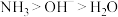 |
您最近一年使用:0次
6 . 舍勒制备氯气的方法至今还在实验室使用。某个合作学习小组用下图所示实验装置制取 Cl2并验证其性质。(已知:FeCl3的熔点 306℃、沸点 316℃)
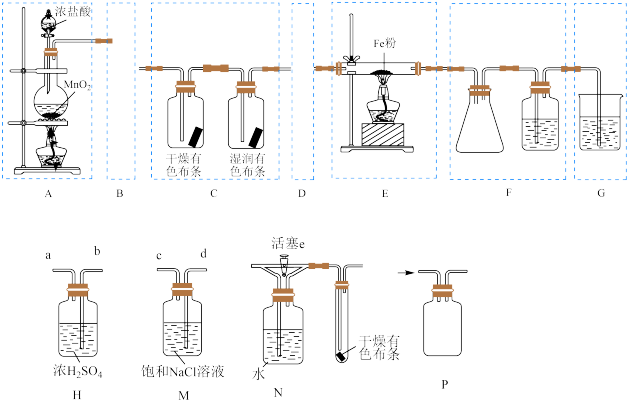
请回答下列问题。
(1)写出装置 A 的反应化学方程式___________ 。
(2)框 B 内装置的作用是净化氯气,把装置 H、M 连接后放入框 B 内,则其连接顺序是___________ (请填写小写字母)。
(3)框 D 装置的作用是收集氯气,请在答卷中按所示气流方向,将集气瓶 P 内的两个玻璃导管补充画完整___________ 。
(4)实验结束后,取锥形瓶中的少量固体于试管中,加足量蒸馏水,充分振荡使固体完全溶解,加入几滴KSCN 溶液后,再加入足量锌粉,充分振荡后静置。请描述上述实验过程中,试管中溶液的颜色变化___________ 。
(5)装置 G 可选用试剂___________ (填标号),并写出相应的离子方程式___________ 。
①KI ②NaCl ③NaOH ④H2SO4
(6)该合作学习小组完成上述实验验后,另一学习小组保留装置 A 和 B,且用装置 N 来替代装置 C,欲达到相同实验目的,请简述使用装置 N 进行实验的操作和现象___________ 。

请回答下列问题。
(1)写出装置 A 的反应化学方程式
(2)框 B 内装置的作用是净化氯气,把装置 H、M 连接后放入框 B 内,则其连接顺序是
(3)框 D 装置的作用是收集氯气,请在答卷中按所示气流方向,将集气瓶 P 内的两个玻璃导管补充画完整
(4)实验结束后,取锥形瓶中的少量固体于试管中,加足量蒸馏水,充分振荡使固体完全溶解,加入几滴KSCN 溶液后,再加入足量锌粉,充分振荡后静置。请描述上述实验过程中,试管中溶液的颜色变化
(5)装置 G 可选用试剂
①KI ②NaCl ③NaOH ④H2SO4
(6)该合作学习小组完成上述实验验后,另一学习小组保留装置 A 和 B,且用装置 N 来替代装置 C,欲达到相同实验目的,请简述使用装置 N 进行实验的操作和现象
您最近一年使用:0次
名校
7 . 下列实验装置或操作能达到实验目的的是
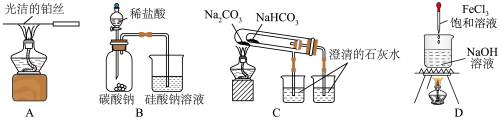
| A.用图A装置观察KCl的焰色试验现象 |
| B.用图B装置证明非金属性强弱:Cl>C>Si |
C.用图C装置比较 和 和 的热稳定性 的热稳定性 |
| D.用图D装置制备氢氧化铁胶体 |
您最近一年使用:0次
名校
8 . 科学探究要实事求是、严谨细致。某化学兴趣小组设计实验进行有关氯化物的探究实验,回答下列问题:
Ⅰ. 在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水
在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水 。经查阅资料得知:无水
。经查阅资料得知:无水 在空气中易潮解,加热易升华。他们设计了以Fe粉和
在空气中易潮解,加热易升华。他们设计了以Fe粉和 为原料制备无水
为原料制备无水 的实验方案,装置示意图如下:
的实验方案,装置示意图如下:
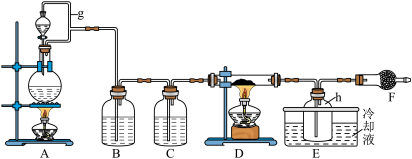
(1)仪器F的名称是___________ 。
(2)装置A中设计g管的作用是___________ 。
(3)装置A中发生反应的离子方程式为___________ 。
Ⅱ.利用惰性电极电解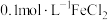 溶液,探究外界条件对电极反应(离子放电顺序)的影响。
溶液,探究外界条件对电极反应(离子放电顺序)的影响。
(4)实验数据如表所示:
①由实验1、2现象可以得出结论:增大pH,___________ 优先于___________ 放电;
②若由实验2、3、4现象可以得出结论:___________ 。
Ⅲ.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、 硝酸银溶液、蒸馏水和各种浓度的
硝酸银溶液、蒸馏水和各种浓度的 溶液。
溶液。
①实验中,“待测物理量X”是___________ ;
②为了探究浓度对氯化铵水解平衡的影响,实验6可与实验___________ 作对照实验;
③实验目的ⅱ是___________ ;
④上述表格中,b___________ d(填“>”、“<”或“=”)。
⑤氯化铵在生产生活中有很多实用的用途,请写出一种应用:___________ 。
Ⅰ.
 在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水
在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水 。经查阅资料得知:无水
。经查阅资料得知:无水 在空气中易潮解,加热易升华。他们设计了以Fe粉和
在空气中易潮解,加热易升华。他们设计了以Fe粉和 为原料制备无水
为原料制备无水 的实验方案,装置示意图如下:
的实验方案,装置示意图如下:
(1)仪器F的名称是
(2)装置A中设计g管的作用是
(3)装置A中发生反应的离子方程式为
Ⅱ.利用惰性电极电解
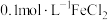 溶液,探究外界条件对电极反应(离子放电顺序)的影响。
溶液,探究外界条件对电极反应(离子放电顺序)的影响。(4)实验数据如表所示:
| 实验编号 | 电压/V | pH | 阳极现象 | 阴极现象 |
| 1 | 1.5 | 1.00 | 无气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
| 2 | 1.5 | 5.52 | 无气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
| 3 | 3.0 | 5.52 | 少量气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
| 4 | 4.5 | 5.52 | 大量气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
②若由实验2、3、4现象可以得出结论:
Ⅲ.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
| 实验编号 |  | 温度/℃ | 待测物理量X | 实验目的 |
| 5 | 0.5 | 30 | a | ___________ |
| 6 | 1.5 | ⅰ | b | 探究浓度对氯化铵水解平衡的影响 |
| 7 | 1.5 | 35 | c | ⅱ |
| 8 | 2.0 | 40 | d | 探究温度、浓度同时对氯化铵化解平衡的影响 |
 硝酸银溶液、蒸馏水和各种浓度的
硝酸银溶液、蒸馏水和各种浓度的 溶液。
溶液。①实验中,“待测物理量X”是
②为了探究浓度对氯化铵水解平衡的影响,实验6可与实验
③实验目的ⅱ是
④上述表格中,b
⑤氯化铵在生产生活中有很多实用的用途,请写出一种应用:
您最近一年使用:0次
2023-09-28更新
|
246次组卷
|
2卷引用:广东省部分学校(南粤名校联考)2023-2024学年高三上学期9月联考化学试题
名校
解题方法
9 . 某校化学兴趣小组为研究 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
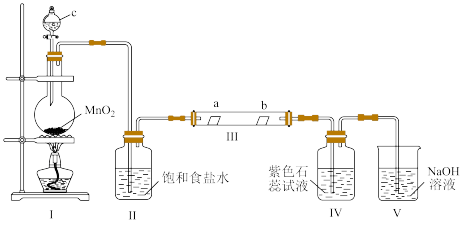
(1)装置Ⅰ中仪器c的名称是_______ ,实验室以二氧化锰和浓盐酸制备氯气的离子方程式,为_______ 。
(2)装置Ⅱ的作用是_______ 。
(3)若产生 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象_______ 。
(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是井未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的_______ 装置(填序号)。
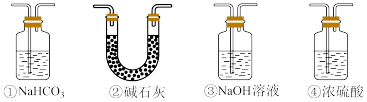
(5)实验结束后,欲回收利用装置Ⅰ中未反应完的 ,除了玻璃棒还需要的玻璃仪器有
,除了玻璃棒还需要的玻璃仪器有_______ 。
(6)常温下装置Ⅴ反生反应的离子方程式为_______ 。
(7)有一种“地康法”制取氯气的反应原理如图所示:
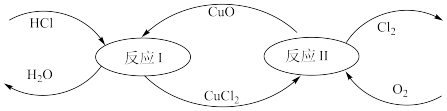
在450℃条件下,反应Ⅱ的化学方程式为_______ 。
 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色试纸,b为湿润的红色试纸。
(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生
 足量,实验过程中装置Ⅳ中的实验现象
足量,实验过程中装置Ⅳ中的实验现象(4)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是井未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(5)实验结束后,欲回收利用装置Ⅰ中未反应完的
 ,除了玻璃棒还需要的玻璃仪器有
,除了玻璃棒还需要的玻璃仪器有(6)常温下装置Ⅴ反生反应的离子方程式为
(7)有一种“地康法”制取氯气的反应原理如图所示:

在450℃条件下,反应Ⅱ的化学方程式为
您最近一年使用:0次
2023-11-29更新
|
228次组卷
|
3卷引用:广东省惠州市惠州一中2023-2024学年高一上学期第二次阶段性考试化学试卷
解题方法
10 . 肉桂酸用在食品防腐保鲜上,是具有无公害的环保防腐剂。用在葡萄酒中,使其色泽光鲜。肉桂酸具有很强的兴奋作用,可直接添加于食品中。某小组设计实验制备肉桂酸并探究其性质。
【原理】

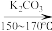
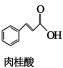
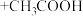
【性质】
【步骤】

【装置】利用图1装置完成步骤①,利用图2装置完成步骤②,抽滤操作用图3装置。(装置图中加热和固定装置省略)

回答下列问题:
(1)仪器A的名称是___________ 。完成步骤①选择合适的加热方式为___________ (填字母)。
a.热水浴(90℃以下) b.油浴(90~250℃) c.沙浴(250~350℃)
(2)完成步骤②,蒸馏的主要目的是___________ ,导管1与空气相通,其作用是___________ (答一条即可)。
(3)相对普通过滤,利用图3抽滤的主要优点有___________ (答一条即可)。
(4)第一次抽滤的滤渣主要成分是___________ 。
(5)证明步骤②中已达到实验目的主要现象是___________ 。
(6)探究肉桂酸的性质。取少量产品溶于水,并将溶液分成甲、乙两份进行如下实验:
上述实验结论正确的是___________ (填代号)。
【原理】

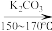

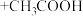
【性质】
| 物质 | 苯甲醛 | 肉桂酸 | 乙酸酐 | 乙酸 |
| 沸点 | 179℃ | 300℃ | 140℃ | 117.9℃ |
| 水溶性 | 微溶于水、无色油状液体 | 难溶于冷水、易溶于热水 | 与水反应生成乙酸 | 与水互溶 |

【装置】利用图1装置完成步骤①,利用图2装置完成步骤②,抽滤操作用图3装置。(装置图中加热和固定装置省略)

回答下列问题:
(1)仪器A的名称是
a.热水浴(90℃以下) b.油浴(90~250℃) c.沙浴(250~350℃)
(2)完成步骤②,蒸馏的主要目的是
(3)相对普通过滤,利用图3抽滤的主要优点有
(4)第一次抽滤的滤渣主要成分是
(5)证明步骤②中已达到实验目的主要现象是
(6)探究肉桂酸的性质。取少量产品溶于水,并将溶液分成甲、乙两份进行如下实验:
| 实验 | 实验操作 | 实验现象 | 实验结论 |
| a | 向甲中滴加少量的酸性 溶液 溶液 | 紫色变为无色 | 肉桂酸含碳碳双键 |
| b | 向乙中滴加少量的 溶液 溶液 | 产生气泡 | 肉桂酸的酸性比碳酸强 |
您最近一年使用:0次
2023-06-01更新
|
79次组卷
|
2卷引用:江西省2022-2023学年高二下学期5月统一调研测试化学试题



