1 . 在处理NO废气的过程中,催化剂 会逐渐失活变为
会逐渐失活变为 。
。
某小组为解决这一问题,实验研究 和
和 之间的相互转化。
之间的相互转化。
资料:i.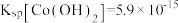 ;
;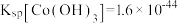 。
。
ii.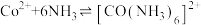
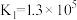 ;
;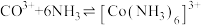
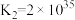 。
。
iii. 和
和 在酸性条件下均能生成
在酸性条件下均能生成 。
。
(1)探 的还原性
的还原性
实验I 粉红色的 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。
实验Ⅱ 向 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。
实验Ⅲ 按如图装置进行实验,观察到电压表指针偏转。 可以被酸性
可以被酸性 溶液氧化。乙同学补充实验IV,
溶液氧化。乙同学补充实验IV,_______ (补全实验操作及现象),否定了该观点。
②探究碱性条件下 的还原性,进行实验。
的还原性,进行实验。_______ 。
③根据氧化还原反应规律解释还原性 :
: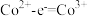 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使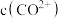 和
和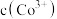 均降低,但
均降低,但_______ 降低的程度更大,还原剂的还原性增强。
(2)探究 的氧化性
的氧化性
①根据实验Ⅲ和IV推测氧化性: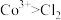 ,设计实验证明:向V中得到的棕褐色沉淀中,
,设计实验证明:向V中得到的棕褐色沉淀中,_______ (补全实验操作及现象),反应方程式为_______ 。
②向V中得到的棕褐色沉淀中,滴加 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是_______ 。
(3)催化剂 的失活与再生
的失活与再生
①结合数据解释 能被氧化为
能被氧化为 而失活的原因:
而失活的原因:_______ 。
②根据以上实验,设计物质转化流程图 实现 的再生:
的再生:_______ 。示例:
 会逐渐失活变为
会逐渐失活变为 。
。某小组为解决这一问题,实验研究
 和
和 之间的相互转化。
之间的相互转化。资料:i.
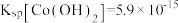 ;
;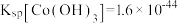 。
。ii.
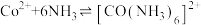
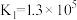 ;
;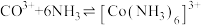
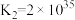 。
。iii.
 和
和 在酸性条件下均能生成
在酸性条件下均能生成 。
。(1)探
 的还原性
的还原性实验I 粉红色的
 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。实验Ⅱ 向
 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。实验Ⅲ 按如图装置进行实验,观察到电压表指针偏转。
 可以被酸性
可以被酸性 溶液氧化。乙同学补充实验IV,
溶液氧化。乙同学补充实验IV,②探究碱性条件下
 的还原性,进行实验。
的还原性,进行实验。实验V: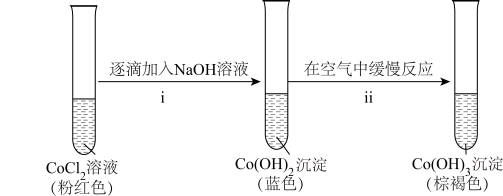
③根据氧化还原反应规律解释还原性
 :
: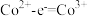 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使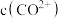 和
和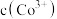 均降低,但
均降低,但(2)探究
 的氧化性
的氧化性①根据实验Ⅲ和IV推测氧化性:
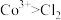 ,设计实验证明:向V中得到的棕褐色沉淀中,
,设计实验证明:向V中得到的棕褐色沉淀中,②向V中得到的棕褐色沉淀中,滴加
 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是(3)催化剂
 的失活与再生
的失活与再生①结合数据解释
 能被氧化为
能被氧化为 而失活的原因:
而失活的原因:②根据以上实验,设计物质转化
 的再生:
的再生:
您最近一年使用:0次
名校
解题方法
2 . 在处理 废气的过程中,催化剂
废气的过程中,催化剂 会逐渐失活变为
会逐渐失活变为 。某小组为解决这一问题,实验研究
。某小组为解决这一问题,实验研究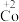 和
和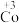 之间的相互转化。资料:
之间的相互转化。资料: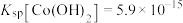 ,
,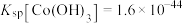
(1)探究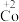 的还原性
的还原性
实验Ⅰ.粉红色的 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。
实验Ⅱ.向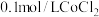 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。
实验Ⅲ.按如图装置进行实验,观察到电压表指针偏转。
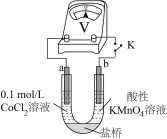
①甲同学根据实验Ⅲ得出结论: 可以被酸性
可以被酸性 溶液氧化。
溶液氧化。
乙同学补充实验Ⅳ,___________ (补全实验操作及现象),否定了该观点。
②探究碱性条件下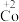 的还原性,进行实验。
的还原性,进行实验。
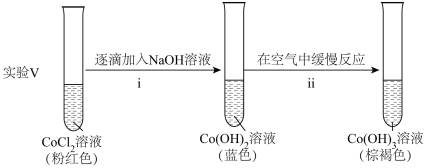
ⅱ中反应的化学方程式是___________ 。
③根据氧化还原反应规律解释:还原性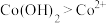 :
: 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使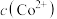 和
和 均降低,但
均降低,但___________ 降低的程度更大,还原剂的还原性增强。
(2)探究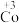 的氧化性
的氧化性
①根据实验Ⅲ和Ⅳ推测氧化性: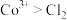 ,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,
,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,___________ (补全实验操作及现象),反应的离子方程式是___________ 。
②向Ⅴ中得到的棕褐色沉淀中滴加 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是___________ 。
(3)利用“三室两膜”装置(如图)实现“电解”制备 。
。
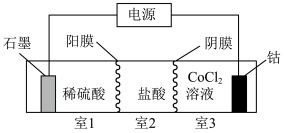
①石墨电极的电极反应式为___________
②生成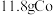 时,室1溶液质量理论上减少
时,室1溶液质量理论上减少___________ g。
 废气的过程中,催化剂
废气的过程中,催化剂 会逐渐失活变为
会逐渐失活变为 。某小组为解决这一问题,实验研究
。某小组为解决这一问题,实验研究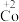 和
和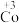 之间的相互转化。资料:
之间的相互转化。资料: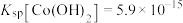 ,
,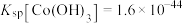
(1)探究
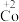 的还原性
的还原性实验Ⅰ.粉红色的
 溶液或
溶液或 溶液在空气中久置,无明显变化。
溶液在空气中久置,无明显变化。实验Ⅱ.向
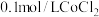 溶液中滴入2滴酸性
溶液中滴入2滴酸性 溶液,无明显变化。
溶液,无明显变化。实验Ⅲ.按如图装置进行实验,观察到电压表指针偏转。

①甲同学根据实验Ⅲ得出结论:
 可以被酸性
可以被酸性 溶液氧化。
溶液氧化。乙同学补充实验Ⅳ,
②探究碱性条件下
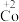 的还原性,进行实验。
的还原性,进行实验。
ⅱ中反应的化学方程式是
③根据氧化还原反应规律解释:还原性
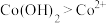 :
: 在碱性条件下,
在碱性条件下, 与
与 、
、 反应,使
反应,使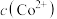 和
和 均降低,但
均降低,但(2)探究
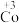 的氧化性
的氧化性①根据实验Ⅲ和Ⅳ推测氧化性:
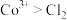 ,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,
,设计实验证明:向Ⅴ中得到的棕褐色沉淀中,②向Ⅴ中得到的棕褐色沉淀中滴加
 溶液,加入催化剂,产生无色气泡,该气体是
溶液,加入催化剂,产生无色气泡,该气体是(3)利用“三室两膜”装置(如图)实现“电解”制备
 。
。
①石墨电极的电极反应式为
②生成
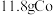 时,室1溶液质量理论上减少
时,室1溶液质量理论上减少
您最近一年使用:0次
名校
3 . 某小组探究含Cr元素的化合物间的转化,进行如下实验。
资料:
i.含Cr元素的常见粒子: (橙色)、
(橙色)、 (黄色)、CrO5(溶于水,蓝紫色,不稳定)、Cr3+(绿色)、Cr(OH)3(蓝灰色,难溶于水,可溶于强酸、强碱)、
(黄色)、CrO5(溶于水,蓝紫色,不稳定)、Cr3+(绿色)、Cr(OH)3(蓝灰色,难溶于水,可溶于强酸、强碱)、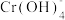 (亮绿色)。
(亮绿色)。
ii.H2O2在碱性环境中比在酸性环境中分解速率快。
iii.在碱性环境中,O2不能氧化+3价铬元素。
实验操作及现象如表:
(1)已知 (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+。请用化学平衡移动原理解释I中滴入稀硫酸后溶液橙色加深的原因:
(黄色)+2H+。请用化学平衡移动原理解释I中滴入稀硫酸后溶液橙色加深的原因:_____ 。
(2)I中,溶液由橙色变为绿色的总反应的离子方程式是_____ 。
(3)Ⅱ中,继续滴入NaOH溶液后,又有气泡生成的原因是_____ 。
(4)Ⅱ中,继续滴入NaOH溶液后,预测有Cr(OH)3沉淀生成,但实验时未观察到。
提出假设:在碱性环境中,+3价铬元素被H2O2氧化。
①甲同学设计实验证明假设成立:
取少量I中的绿色溶液,在滴入NaOH溶液前增加一步操作:______ 。然后滴入NaOH溶液,有蓝灰色沉淀生成,继续滴入NaOH溶液,沉淀溶解,溶液变为______ 色。
②乙同学进一步研究碱性环境对+3价铬元素的还原性或H2O2的氧化性的影响,设计如图实验。
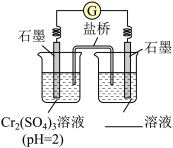
右侧烧杯的溶液中,氧化剂是_____ 。
开始时灵敏电流计指针不偏转,分别继续进行如下实验。
i.向左侧烧杯中滴入NaOH溶液,出现蓝灰色沉淀,继续缓慢滴入NaOH溶液,灵敏电流计指针向右偏转(电子从左向右运动),此时左侧的电极反应式为_____ 。
ii.向右侧烧杯中滴入NaOH溶液,有微小气泡生成,灵敏电流计指针向左偏转,左侧无明显变化。此时原电池中的总反应的化学方程式为_____ 。
(5)由上述实验, 与H2O2、
与H2O2、 与H2O2的氧化性强弱(填“>”或“<”):
与H2O2的氧化性强弱(填“>”或“<”):
酸性条件下,
_____ H2O2;碱性条件下, 
_____ H2O2。
资料:
i.含Cr元素的常见粒子:
 (橙色)、
(橙色)、 (黄色)、CrO5(溶于水,蓝紫色,不稳定)、Cr3+(绿色)、Cr(OH)3(蓝灰色,难溶于水,可溶于强酸、强碱)、
(黄色)、CrO5(溶于水,蓝紫色,不稳定)、Cr3+(绿色)、Cr(OH)3(蓝灰色,难溶于水,可溶于强酸、强碱)、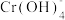 (亮绿色)。
(亮绿色)。ii.H2O2在碱性环境中比在酸性环境中分解速率快。
iii.在碱性环境中,O2不能氧化+3价铬元素。
实验操作及现象如表:
| 装置 | 步骤 | 操作 | 现象 |
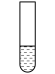 2mL0.0125mol•L-1K2Cr2O7溶液 | I | 先滴入稀硫酸至pH≈2,再滴入5滴5%H2O2溶液,振荡 | 溶液橙色加深。滴入H2O2溶液后迅速变为蓝紫色,有气泡生成。稍后,无明显气泡时,溶液由蓝紫色完全变为绿色 |
| Ⅱ | 继续缓慢滴入10滴2mol•L-1NaOH溶液,边滴,边振荡 | 又有气泡生成,溶液最终变为黄色 |
 (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+。请用化学平衡移动原理解释I中滴入稀硫酸后溶液橙色加深的原因:
(黄色)+2H+。请用化学平衡移动原理解释I中滴入稀硫酸后溶液橙色加深的原因:(2)I中,溶液由橙色变为绿色的总反应的离子方程式是
(3)Ⅱ中,继续滴入NaOH溶液后,又有气泡生成的原因是
(4)Ⅱ中,继续滴入NaOH溶液后,预测有Cr(OH)3沉淀生成,但实验时未观察到。
提出假设:在碱性环境中,+3价铬元素被H2O2氧化。
①甲同学设计实验证明假设成立:
取少量I中的绿色溶液,在滴入NaOH溶液前增加一步操作:
②乙同学进一步研究碱性环境对+3价铬元素的还原性或H2O2的氧化性的影响,设计如图实验。

右侧烧杯的溶液中,氧化剂是
开始时灵敏电流计指针不偏转,分别继续进行如下实验。
i.向左侧烧杯中滴入NaOH溶液,出现蓝灰色沉淀,继续缓慢滴入NaOH溶液,灵敏电流计指针向右偏转(电子从左向右运动),此时左侧的电极反应式为
ii.向右侧烧杯中滴入NaOH溶液,有微小气泡生成,灵敏电流计指针向左偏转,左侧无明显变化。此时原电池中的总反应的化学方程式为
(5)由上述实验,
 与H2O2、
与H2O2、 与H2O2的氧化性强弱(填“>”或“<”):
与H2O2的氧化性强弱(填“>”或“<”):酸性条件下,


您最近一年使用:0次
2023-01-07更新
|
410次组卷
|
4卷引用:北京市顺义牛栏山第一中学2022-2023学年高二下学期3月月考化学试题
4 . 亚硝酸钠(NaNO2)常用作肉类食品的防腐剂。某实验小组将NO和NO2的混合气体通入Na2CO3溶液中,并经一系列操作制得NaNO2固体,然后对其性质进行探究。
【查阅资料】
①NaNO2具有较强的氧化性和较弱的还原性,其水溶液显碱性。
② 与Ag+反应,可生成AgNO2白色沉淀或无色配离子。
与Ag+反应,可生成AgNO2白色沉淀或无色配离子。
【性质探究】将制取的NaNO2固体配制成约0.1mol/L NaNO2溶液,进行实验I和实验II。
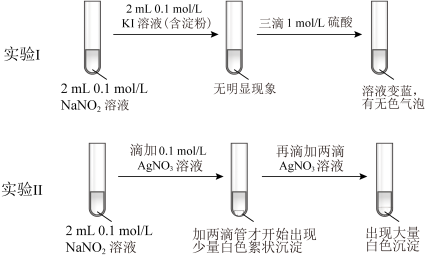
请回答下列问题:
(1)NaNO2溶液显碱性的原因是_______ (用离子方程式表示)。
(2)根据实验I,推测酸性条件下 氧化I- 的离子方程式是
氧化I- 的离子方程式是_______ 。
(3)甲同学认为依据实验I的现象可以得出结论:该条件下 能氧化I-。乙同学则认为制取的NaNO2含有副产物,仅凭实验I不能得出上述结论,还需要进行补充实验。乙同学设计实验III证明了实验I条件下氧化I- 的只有
能氧化I-。乙同学则认为制取的NaNO2含有副产物,仅凭实验I不能得出上述结论,还需要进行补充实验。乙同学设计实验III证明了实验I条件下氧化I- 的只有 。请补充完整实验III的实验方案:取2mL 0.1mol/L
。请补充完整实验III的实验方案:取2mL 0.1mol/L_______ 溶液于试管中,加入_______ ,溶液没有变蓝。
(4)①由实验II的现象得出结论:白色沉淀的生成与_______ 有关。
②仅用实验II的试剂,设计实验方案进一步证实了上述结论,实验操作及现象是_______ 。
(5)常温下AgNO2微溶于水,在沸水中可溶。除去AgNO2沉淀中的少量Ag2O杂质的方法如下:加入适量水,加热溶解,_______ ,过滤,洗涤,干燥。
【查阅资料】
①NaNO2具有较强的氧化性和较弱的还原性,其水溶液显碱性。
②
 与Ag+反应,可生成AgNO2白色沉淀或无色配离子。
与Ag+反应,可生成AgNO2白色沉淀或无色配离子。【性质探究】将制取的NaNO2固体配制成约0.1mol/L NaNO2溶液,进行实验I和实验II。

请回答下列问题:
(1)NaNO2溶液显碱性的原因是
(2)根据实验I,推测酸性条件下
 氧化I- 的离子方程式是
氧化I- 的离子方程式是(3)甲同学认为依据实验I的现象可以得出结论:该条件下
 能氧化I-。乙同学则认为制取的NaNO2含有副产物,仅凭实验I不能得出上述结论,还需要进行补充实验。乙同学设计实验III证明了实验I条件下氧化I- 的只有
能氧化I-。乙同学则认为制取的NaNO2含有副产物,仅凭实验I不能得出上述结论,还需要进行补充实验。乙同学设计实验III证明了实验I条件下氧化I- 的只有 。请补充完整实验III的实验方案:取2mL 0.1mol/L
。请补充完整实验III的实验方案:取2mL 0.1mol/L(4)①由实验II的现象得出结论:白色沉淀的生成与
②仅用实验II的试剂,设计实验方案进一步证实了上述结论,实验操作及现象是
(5)常温下AgNO2微溶于水,在沸水中可溶。除去AgNO2沉淀中的少量Ag2O杂质的方法如下:加入适量水,加热溶解,
您最近一年使用:0次
2022-10-21更新
|
200次组卷
|
2卷引用:广东省广东实验中学2022-2023学年高三上学期第一次阶段考试化学试题
名校
解题方法
5 . 在处理NO废气的过程中,催化剂[Co(NH3)6]2+会逐渐失活变为[Co(NH3)6]3+。某小组为解决这一问题,实验研究 和
和 之间的相互转化。
之间的相互转化。
资料:i.Ksp[Co(OH)2]=5.9×10-15,Ksp[Co(OH)3]=1.6×10-44
ii.Co2++6NH3 [Co(NH3)6]2+K1=1.3×105
[Co(NH3)6]2+K1=1.3×105
Co3++6NH3 [Co(NH3)6]3+K2=2×1035
[Co(NH3)6]3+K2=2×1035
iii.[Co(NH3)6]2+和[Co(NH3)6]3+在酸性条件下均能生成NH
(1)探究 的还原性
的还原性
实验I.粉红色的CoCl2溶液或CoSO4溶液在空气中久置,无明显变化。
实验II.向0.1mol/LCoCl2溶液中滴入2滴酸性KMnO4溶液,无明显变化。
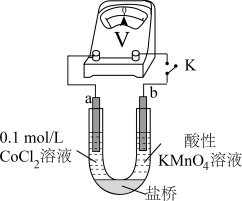
实验III.按如图装置进行实验,观察到电压表指针偏转。
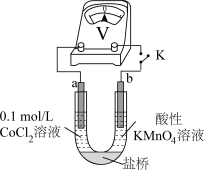
①甲同学根据实验III得出结论:Co2+可以被酸性KMnO4溶液氧化。
乙同学补充实验IV,____ (补全实验操作及现象),否定了该观点。
②探究碱性条件下 的还原性,进行实验。
的还原性,进行实验。
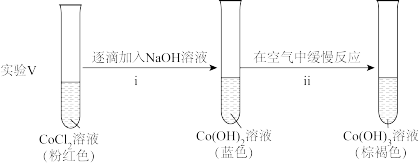
ii中反应的化学方程式是____ 。
③根据氧化还原反应规律解释:还原性Co(OH)2>Co2+:Co2+-e-=Co3+在碱性条件下,OH-与Co2+、Co3+反应,使c(Co2+)和c(Co3+)均降低,但____ 降低的程度更大,还原剂的还原性增强。
(2)探究 的氧化性
的氧化性
①根据实验III和IV推测氧化性:Co3+>Cl2,设计实验证明:向V中得到的棕褐色沉淀中,____ (补全实验操作及现象),反应的离子方程式是____ 。
②向V中得到的棕褐色沉淀中滴加H2SO4溶液,加入催化剂,产生无色气泡,该气体是____ 。
(3)催化剂[Co(NH3)6]2+的失活与再生
①结合数据解释[Co(NH3)6]2+能被氧化为[Co(NH3)6]3+而失活的原因:____ 。
②根据以上实验,设计物质转化流程图实现[Co(NH3)6]2+的再生:____ 。
示例:Co CoCl2
CoCl2 Co(OH)2
Co(OH)2
 和
和 之间的相互转化。
之间的相互转化。资料:i.Ksp[Co(OH)2]=5.9×10-15,Ksp[Co(OH)3]=1.6×10-44
ii.Co2++6NH3
 [Co(NH3)6]2+K1=1.3×105
[Co(NH3)6]2+K1=1.3×105Co3++6NH3
 [Co(NH3)6]3+K2=2×1035
[Co(NH3)6]3+K2=2×1035iii.[Co(NH3)6]2+和[Co(NH3)6]3+在酸性条件下均能生成NH

(1)探究
 的还原性
的还原性实验I.粉红色的CoCl2溶液或CoSO4溶液在空气中久置,无明显变化。
实验II.向0.1mol/LCoCl2溶液中滴入2滴酸性KMnO4溶液,无明显变化。
实验III.按如图装置进行实验,观察到电压表指针偏转。

①甲同学根据实验III得出结论:Co2+可以被酸性KMnO4溶液氧化。
乙同学补充实验IV,
②探究碱性条件下
 的还原性,进行实验。
的还原性,进行实验。
ii中反应的化学方程式是
③根据氧化还原反应规律解释:还原性Co(OH)2>Co2+:Co2+-e-=Co3+在碱性条件下,OH-与Co2+、Co3+反应,使c(Co2+)和c(Co3+)均降低,但
(2)探究
 的氧化性
的氧化性①根据实验III和IV推测氧化性:Co3+>Cl2,设计实验证明:向V中得到的棕褐色沉淀中,
②向V中得到的棕褐色沉淀中滴加H2SO4溶液,加入催化剂,产生无色气泡,该气体是
(3)催化剂[Co(NH3)6]2+的失活与再生
①结合数据解释[Co(NH3)6]2+能被氧化为[Co(NH3)6]3+而失活的原因:
②根据以上实验,设计物质转化流程图实现[Co(NH3)6]2+的再生:
示例:Co
 CoCl2
CoCl2 Co(OH)2
Co(OH)2
您最近一年使用:0次
2022-05-08更新
|
1354次组卷
|
9卷引用:北京市八一学校2022-2023学年高三上学期12月月考化学试题
6 . 某同学欲探究H2O2的氧化还原性:
(1)该同学从化合价的角度分析H2O2既有氧化性又有还原性,其原因是___________ 。
(2)探究H2O2的氧化性可以选取的物质是:___________ (填序号)
①淀粉KI溶液 ②FeSO4溶液 ③Cl2④HNO3溶液
任选一个你所选的物质进行实验,观察到___________ 现象,证明H2O2有氧化性,反应的离子方程式为___________ 。
(3)继续探究:
资料:Na2O2+2H2O=2NaOH+H2O2、2H2O2=2H2O+O2↑
①制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。
向A中加入过量稀H2SO4,得溶液B。
②检验H2O2:向溶液A、B中分别滴加适量KMnO4溶液。
Ⅰ.B中产生气泡,滴入的溶液紫色褪去。
反应的离子方程式为___________ 。
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO2,对其产生的原因提出猜想:
猜想1.KMnO4,有氧化性,能被还原为MnO2
猜想2.Mn2+有___________ 性,能与H2O2反应产生MnO2
猜想3……
③探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
iii是ii和i的对照实验。
①X是___________ 。
②a是___________ 、b是___________ 。
③取i中棕褐色固体,实验证明是MnO2。
综上所述,H2O2体现氧化性还是还原性与反应对象的性质和溶液的酸碱性有关。
(1)该同学从化合价的角度分析H2O2既有氧化性又有还原性,其原因是
(2)探究H2O2的氧化性可以选取的物质是:
①淀粉KI溶液 ②FeSO4溶液 ③Cl2④HNO3溶液
任选一个你所选的物质进行实验,观察到
(3)继续探究:
资料:Na2O2+2H2O=2NaOH+H2O2、2H2O2=2H2O+O2↑
①制备H2O2:将Na2O2溶于冰水中,产生少量气泡,得溶液A。
向A中加入过量稀H2SO4,得溶液B。
②检验H2O2:向溶液A、B中分别滴加适量KMnO4溶液。
Ⅰ.B中产生气泡,滴入的溶液紫色褪去。
反应的离子方程式为
Ⅱ.A中滴入的溶液紫色褪去,有棕褐色固体生成,产生大量气泡。推测固体可能含MnO2,对其产生的原因提出猜想:
猜想1.KMnO4,有氧化性,能被还原为MnO2
猜想2.Mn2+有
猜想3……
③探究猜想2的合理性,并分析Ⅰ中没有产生棕褐色固体的原因,设计实验如下:
| 序号 | 实验 | 试剂 | 现象 |
| i | 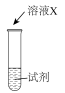 | a | 生成棕褐色固体,产生大量气泡 |
| ii | b | 有少量气泡 | |
| iii | H2O2溶液 | 有少量气泡 |
①X是
②a是
③取i中棕褐色固体,实验证明是MnO2。
综上所述,H2O2体现氧化性还是还原性与反应对象的性质和溶液的酸碱性有关。
您最近一年使用:0次
名校
解题方法
7 . 查阅资料知: 在一定条件下可以转化为
在一定条件下可以转化为 ,
, 易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒
易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒
(1)已知 能发生如下反应:
能发生如下反应: ,上述反应中氧化产物是
,上述反应中氧化产物是___________ ;HI在反应中体现了什么性质___________ 。(填字母)。
A.氧化性 B.还原性 C.酸性 D.碱性
(2)根据上题反应,鉴别 和NaCl,可选择以下物质中的___________进行实验(填字母)。
和NaCl,可选择以下物质中的___________进行实验(填字母)。
 在一定条件下可以转化为
在一定条件下可以转化为 ,
, 易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒
易溶于水且溶解时吸热,有咸味,遇酸易放出气体,人误食会中毒(1)已知
 能发生如下反应:
能发生如下反应: ,上述反应中氧化产物是
,上述反应中氧化产物是A.氧化性 B.还原性 C.酸性 D.碱性
(2)根据上题反应,鉴别
 和NaCl,可选择以下物质中的___________进行实验(填字母)。
和NaCl,可选择以下物质中的___________进行实验(填字母)。| A.食用白醋 | B.碘化钾淀粉试纸 | C.淀粉 | D.水 |
您最近一年使用:0次
名校
8 . 下表为元素周期表的一部分,请参照元素在表中的位置,回答下列问题:
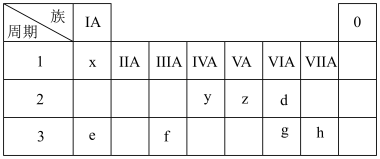
(1)比较d、e常见离子的半径大小(用化学式表示,下同):_______ >_______ ;
(2)比较g、h的最高价氧化物对应水化物的酸性强弱:_______ >_______ 。
(3)用电子式表示e、g组成的简单化合物的形成过程:_______ 。
(4)下列说法不正确的是_______。
(5)由表中两种元素的原子按 组成的常见液态化合物
组成的常见液态化合物 的稀溶液易被
的稀溶液易被 催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中
催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中 表现还原性;第二步反应中
表现还原性;第二步反应中 表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)
表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)_______ 。
(6)上述元素可组成盐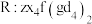 ,向盛有一定量
,向盛有一定量 盐溶液的烧杯中逐滴滴加
盐溶液的烧杯中逐滴滴加 溶液,沉淀物质的量随
溶液,沉淀物质的量随 溶液体积的变化如下图所示:
溶液体积的变化如下图所示:
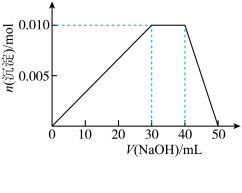
若向上述 盐溶液中改加
盐溶液中改加 溶液,充分反应后,溶液中产生沉淀的物质的量为
溶液,充分反应后,溶液中产生沉淀的物质的量为_______  。
。

(1)比较d、e常见离子的半径大小(用化学式表示,下同):
(2)比较g、h的最高价氧化物对应水化物的酸性强弱:
(3)用电子式表示e、g组成的简单化合物的形成过程:
(4)下列说法不正确的是_______。
A.最简单的氢化物的稳定性 |
B.最高价氧化物对应的水化物的碱性 |
| C.与y元素同主族的第四周期元素的单质是半导体材料 |
| D.y、h两元素组成的化合物中一定只含共价键 |
(5)由表中两种元素的原子按
 组成的常见液态化合物
组成的常见液态化合物 的稀溶液易被
的稀溶液易被 催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中
催化分解,查阅资料可知:在催化过程中发生了两步氧化还原反应,第一步反应中 表现还原性;第二步反应中
表现还原性;第二步反应中 表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)
表现氧化性;请写出第二步反应的离子方程式(Q用化学式表示)(6)上述元素可组成盐
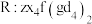 ,向盛有一定量
,向盛有一定量 盐溶液的烧杯中逐滴滴加
盐溶液的烧杯中逐滴滴加 溶液,沉淀物质的量随
溶液,沉淀物质的量随 溶液体积的变化如下图所示:
溶液体积的变化如下图所示:
若向上述
 盐溶液中改加
盐溶液中改加 溶液,充分反应后,溶液中产生沉淀的物质的量为
溶液,充分反应后,溶液中产生沉淀的物质的量为 。
。
您最近一年使用:0次
名校
9 . 某实验小组从电极反应角度探究银镜反应中物质氧化性和还原性的变化。
资料:ⅰ.[Ag(NH3)2]+⇌ [Ag(NH3)]++NH3K1=10−3.81
[Ag(NH3)]+⇌ Ag++NH3K2=10−3.24
ⅱ.AgOH不稳定,极易分解为黑色Ag2O,Ag2O溶于氨水
(1)实验发现:乙醛和AgNO3溶液水浴加热无明显现象;银氨溶液水浴加热无明显现象;滴加乙醛的银氨溶液水浴加热,试管壁逐渐出现一层光亮的银镜。
①有研究表明:配制银氨溶液时,AgNO3和氨水生成Ag(NH3)2NO3,写出生成Ag(NH3)2NO3的化学方程式_______ 。
②从氧化还原角度分析:发生银镜反应时,氧化性微粒可能是Ag+、_______ 。
(2)甲同学查阅资料:银镜反应时,Ag+被还原成Ag。
①电极反应式:
ⅰ.还原反应:Ag++e−=Ag
ⅱ.氧化反应:_______ 。(碱性条件下)
②从电极反应角度分析物质氧化性和还原性的变化:
ⅰ.随c(Ag+)降低,Ag+氧化性减弱。
ⅱ.随c(OH−)增大,乙醛还原性增强。
③补充实验验证②中的分析。
乙同学认为实验Ⅲ不能证明“随c(Ag+)降低,Ag+氧化性减弱”,理由是_______ 。
(3)设计实验进一步验证。
①乙同学认为通过实验Ⅳ能证明“随c(Ag+)降低,Ag+氧化性减弱”,你认为是否合理并说明原因_______ 。
②分析实验Ⅴ中“立即出现银镜的原因”,提出假设:随c(OH−)增大,可能是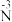 也参与了还原
也参与了还原 。经检验该假设成立,实验方案及现象是
。经检验该假设成立,实验方案及现象是_______ 。
(4)总结:ⅰ.银氨溶液和乙醛发生银镜反应时,氧化剂主要是Ag+,还原剂主要是乙醛;ⅱ.银氨溶液中滴加较浓的NaOH溶液能促进银镜反应的发生,此法不适用于检验醛基,请解释原因_______ 。
资料:ⅰ.[Ag(NH3)2]+⇌ [Ag(NH3)]++NH3K1=10−3.81
[Ag(NH3)]+⇌ Ag++NH3K2=10−3.24
ⅱ.AgOH不稳定,极易分解为黑色Ag2O,Ag2O溶于氨水
(1)实验发现:乙醛和AgNO3溶液水浴加热无明显现象;银氨溶液水浴加热无明显现象;滴加乙醛的银氨溶液水浴加热,试管壁逐渐出现一层光亮的银镜。
①有研究表明:配制银氨溶液时,AgNO3和氨水生成Ag(NH3)2NO3,写出生成Ag(NH3)2NO3的化学方程式
②从氧化还原角度分析:发生银镜反应时,氧化性微粒可能是Ag+、
(2)甲同学查阅资料:银镜反应时,Ag+被还原成Ag。
①电极反应式:
ⅰ.还原反应:Ag++e−=Ag
ⅱ.氧化反应:
②从电极反应角度分析物质氧化性和还原性的变化:
ⅰ.随c(Ag+)降低,Ag+氧化性减弱。
ⅱ.随c(OH−)增大,乙醛还原性增强。
③补充实验验证②中的分析。
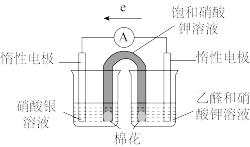
| 实验操作及现象: 实验Ⅰ.插入“饱和KNO3溶液”盐桥,电流表指针偏转; 实验Ⅱ.电流稳定后向右侧烧杯滴加NaOH溶液,指针偏转幅度增大; 实验Ⅲ.电流再次稳定后向左侧烧杯滴加氨水,指针偏转幅度减小 |
(3)设计实验进一步验证。
| 实验 | 实验操作 | 实验现象 |
| Ⅳ | 往盛有银氨溶液的试管中滴加浓氨水,无明显现象,加入3滴乙醛,振荡,水浴加热 | 闻到刺激性气味,溶液略显灰色,试管壁未见银镜 |
| Ⅴ | 往盛有银氨溶液的试管中滴加较浓的NaOH溶液至pH与实验Ⅳ相同,振荡,溶液变浑浊,加入3滴乙醛,振荡,水浴加热 | 试管壁 |
②分析实验Ⅴ中“立即出现银镜的原因”,提出假设:随c(OH−)增大,可能是
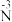 也参与了还原
也参与了还原 。经检验该假设成立,实验方案及现象是
。经检验该假设成立,实验方案及现象是(4)总结:ⅰ.银氨溶液和乙醛发生银镜反应时,氧化剂主要是Ag+,还原剂主要是乙醛;ⅱ.银氨溶液中滴加较浓的NaOH溶液能促进银镜反应的发生,此法不适用于检验醛基,请解释原因
您最近一年使用:0次
2022-04-02更新
|
1061次组卷
|
7卷引用:湖南省常德市第一中学2022-2023学年高三下学期5月月考化学试题
10 . 某研究性学习小组学生根据氧化还原反应规律,探究 、
、 与
与 反应的情况,提出假设并进行相关实验。
反应的情况,提出假设并进行相关实验。
Ⅰ.从理论上分析 和
和 都既有氧化性又有还原性,于是提出如下假设:
都既有氧化性又有还原性,于是提出如下假设:
假设1: 氧化
氧化 ;
;
假设2: 氧化
氧化 。
。
(1)甲同学设计如图装置进行实验:___________ 。
②待试管B中充满红棕色气体,关闭旋塞a和b;取下试管B,向其中加入适量 粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
结论:甲同学认为假设2正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是___________ 。乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;带火星的木条未复燃,得出结论:假设Ⅰ正确。则 和
和 反应的化学方程式是
反应的化学方程式是___________ 。
Ⅱ.该研究性学习小组同学还认为易与 发生反应,应该更易被氧化。查阅资料:
发生反应,应该更易被氧化。查阅资料: ;
;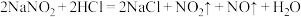 ;酸性条件下,能与
;酸性条件下,能与 反应生成
反应生成 和
和 。
。
(3)丙同学用下图所示装置(部分夹持装置略)探究 与
与 的反应。
的反应。 ,目的是
,目的是___________ 。
②B中观察到的主要现象的是___________ (填字母编号)。
a.铜片逐渐溶解,溶液变为蓝色
b.有红棕色气泡产生
c.有无色气泡产生
③C、E中所盛装的试剂不能是___________ (填字母编号)。
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④充分反应后,检验D装置中产物的方法是:取D装置中产物少许,___________ ,则产物是 。
。
 、
、 与
与 反应的情况,提出假设并进行相关实验。
反应的情况,提出假设并进行相关实验。Ⅰ.从理论上分析
 和
和 都既有氧化性又有还原性,于是提出如下假设:
都既有氧化性又有还原性,于是提出如下假设:假设1:
 氧化
氧化 ;
;假设2:
 氧化
氧化 。
。(1)甲同学设计如图装置进行实验:

②待试管B中充满红棕色气体,关闭旋塞a和b;取下试管B,向其中加入适量
 粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。结论:甲同学认为假设2正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是
 和
和 反应的化学方程式是
反应的化学方程式是Ⅱ.该研究性学习小组同学还认为易与
 发生反应,应该更易被氧化。查阅资料:
发生反应,应该更易被氧化。查阅资料: ;
;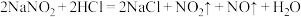 ;酸性条件下,能与
;酸性条件下,能与 反应生成
反应生成 和
和 。
。(3)丙同学用下图所示装置(部分夹持装置略)探究
 与
与 的反应。
的反应。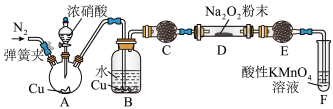
 ,目的是
,目的是②B中观察到的主要现象的是
a.铜片逐渐溶解,溶液变为蓝色
b.有红棕色气泡产生
c.有无色气泡产生
③C、E中所盛装的试剂不能是
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④充分反应后,检验D装置中产物的方法是:取D装置中产物少许,
 。
。
您最近一年使用:0次
2024-04-08更新
|
630次组卷
|
5卷引用:湖北省武汉市第二中学2023-2024学年高一下学期化学周练A卷(1)试卷



