1 . 下列物质的性质与用途具有对应关系的是
A. 溶液呈酸性,可用于腐蚀电路板上的Cu 溶液呈酸性,可用于腐蚀电路板上的Cu |
B. 易溶于水,可用作工业电解制备单质镁 易溶于水,可用作工业电解制备单质镁 |
C.浓 具有脱水性,可用作实验室干燥 具有脱水性,可用作实验室干燥 气体的干燥剂 气体的干燥剂 |
| D.等离子体含有能自由移动的带电粒子,可应用于化学合成和材料表面改性 |
您最近一年使用:0次
昨日更新
|
68次组卷
|
3卷引用:2024届甘肃省民乐县第一中学高三下学期5月模拟考试化学试卷
2 . 有关下列实验装置的说法正确的是
|
|
| ① | ② |
|
|
| ③ | ④ |
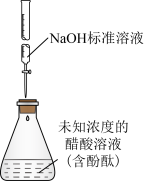
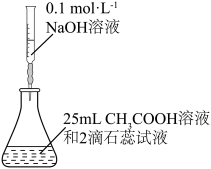
| A.装置①用于测定醋酸的浓度 |
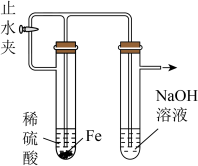
B.装置②用于 的制备,反应一开始就要关闭止水夹,让生成的氢气把左边试管中液体压入右边,以实现自动化控制 的制备,反应一开始就要关闭止水夹,让生成的氢气把左边试管中液体压入右边,以实现自动化控制 |
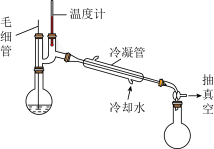
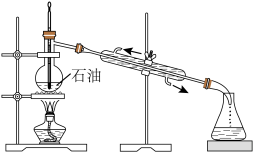
| C.装置③是减压蒸馏,减压条件下可以降低混合组分的熔沸点 |
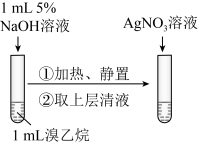
D.装置④可用于检验溴乙烷的水解产物 |
您最近一年使用:0次
解题方法
3 . 宏观辨识与微观探析是化学学科核心素养之一。常温下,下列各组粒子在指定溶液中能大量共存的是
A.0.1 mol⋅L 碳酸钠溶液( 碳酸钠溶液( )中: )中: 、 、 、 、 |
B.加入苯酚显紫色的溶液中能大量共存的离子: 、 、 、 、 、 、 |
C.0.1 mol⋅L 酸性 酸性 溶液中: 溶液中: 、 、 、 、 、 、 |
D.常温下 mol⋅L mol⋅L 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
4 . 化学实验操作是进行科学实验的基础。下列操作合理的是
|
|
| A.石油分馏 | B.用NaOH标准溶液滴定未知浓度的 溶液 溶液 |
|
|
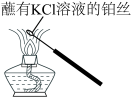
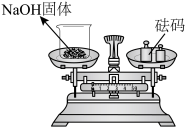
| C.观察K元素的焰色 | D.称量NaOH固体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-12更新
|
177次组卷
|
7卷引用:甘肃省白银市靖远县2024届高三下学期全真模拟化学试题
名校
5 . 氮化铍可用于新型的耐火陶瓷材料和反应堆材料,可由铍粉和干燥氮气在无氧气氛中于700~1400℃的温度下加热制得。以绿柱石(主要组成是 ,还含有少量铁元素)为原料生产氮化铍的工艺流程如图所示。
,还含有少量铁元素)为原料生产氮化铍的工艺流程如图所示。 如表所示。
如表所示。
回答下列问题:
(1)“酸浸”时绿柱石要进行粉碎,其目的是_______ 。
(2)“转化”时加入 的目的是
的目的是_______ (用离子方程式表示)。
(3)“调 ”时加入适量
”时加入适量 细粉除去
细粉除去 和
和 ,调节溶液
,调节溶液 的范围是
的范围是_______ ,其中沉淀 的离子方程式为
的离子方程式为_______ ,“滤渣2”的主要成分是_______ (填化学式)。
(4)“沉铍”时所加试剂 是
是_______ (填“氨水”或“ 溶液”)。
溶液”)。
(5)生成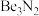 的化学方程式为
的化学方程式为_______ 。
 ,还含有少量铁元素)为原料生产氮化铍的工艺流程如图所示。
,还含有少量铁元素)为原料生产氮化铍的工艺流程如图所示。
 如表所示。
如表所示。| 金属离子 |  |  |  |  |  |
| 开始沉淀pH | 6.3 | 1.8 | 3.1 | 5.6 | 12.4 |
| 沉淀完全pH | 8.3 | 3.2 | 4.8 | 8.5 | 13.8 |
(1)“酸浸”时绿柱石要进行粉碎,其目的是
(2)“转化”时加入
 的目的是
的目的是(3)“调
 ”时加入适量
”时加入适量 细粉除去
细粉除去 和
和 ,调节溶液
,调节溶液 的范围是
的范围是 的离子方程式为
的离子方程式为(4)“沉铍”时所加试剂
 是
是 溶液”)。
溶液”)。(5)生成
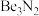 的化学方程式为
的化学方程式为
您最近一年使用:0次
2024-05-16更新
|
27次组卷
|
2卷引用:2024年甘肃省张掖市第一中学模拟化学试题
名校
6 . 黄铁矿( )在酸性条件下发生催化氧化的反应历程如图所示。下列说法错误的是
)在酸性条件下发生催化氧化的反应历程如图所示。下列说法错误的是
 )在酸性条件下发生催化氧化的反应历程如图所示。下列说法错误的是
)在酸性条件下发生催化氧化的反应历程如图所示。下列说法错误的是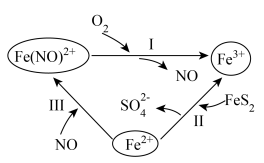
| A.反应Ⅰ、Ⅱ、Ⅲ均发生氧化还原反应 |
B.反应Ⅰ中氧化剂与还原剂的物质的量之比为 |
C.反应Ⅱ的离子方程式为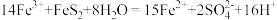 |
D.该过程的总反应为 |
您最近一年使用:0次
2024-05-16更新
|
210次组卷
|
3卷引用:2024年甘肃省张掖市第一中学模拟化学试题
名校
7 . 设 是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是
 是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是A. 由 由 和 和 组成的混合气体中所含中子数为 组成的混合气体中所含中子数为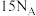 |
B. 石英晶体中含有的 石英晶体中含有的 键的数目是 键的数目是 |
C. 时, 时, 的 的 溶液中含有 溶液中含有 数为 数为 |
D.电解精炼铜时,若阳极质量减少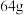 ,则电路中转移的电子数目为 ,则电路中转移的电子数目为 |
您最近一年使用:0次
2024-05-12更新
|
146次组卷
|
3卷引用:2024届甘肃省酒泉市高三下学期三模化学试题
8 . 化学与社会发展和人类进步息息相关。下列说法不正确的是
| A.华为Mate60pro系列“争气机”的芯片材料主要为晶体硅 |
| B.用机械剥离法从石墨中分离出的石墨烯能导电,石墨烯与金刚石互为同素异形体 |
| C.国产飞机C919用到的氨化硅陶瓷是新型无机非金属材料 |
| D.“神舟十七号”飞船返回舱表层材料中的玻璃纤维属于天然有机高分子 |
您最近一年使用:0次
9 . 山梨酸正丁酯具有解毒作用,可以减轻肝脏负担,促进肝细胞修复,保护肝脏健康。实验室用如图所示装置(夹持、加热装置省略)制备山梨酸正丁酯,其方法原理如下:
①在三颈烧瓶中加入 山梨酸、
山梨酸、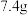 正丁醇、少量催化剂和几粒沸石,水浴加热三颈烧瓶,使反应体系保持微沸。
正丁醇、少量催化剂和几粒沸石,水浴加热三颈烧瓶,使反应体系保持微沸。
②回流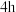 后,停止加热和搅拌,反应液冷却至室温。
后,停止加热和搅拌,反应液冷却至室温。
③滤去催化剂和沸石,将滤液倒入 水中,加入
水中,加入 乙醚,倒入分液漏斗中,分液。
乙醚,倒入分液漏斗中,分液。
④分离出的有机层先用 的
的 溶液洗涤至中性,再用水洗涤分液,收集有机层。
溶液洗涤至中性,再用水洗涤分液,收集有机层。
⑤在有机层中加入少量无水 ,静置片刻,过滤。
,静置片刻,过滤。
⑥将滤液进行蒸馏,除去杂质得到 山梨酸正丁酯。
山梨酸正丁酯。
回答下列问题:
(1)仪器A的名称是___________ ;仪器B的作用是___________ ,冷却水由___________ (填“ ”或“n”)口通入。
”或“n”)口通入。
(2)洗涤、分液过程中,加入 溶液的目的是
溶液的目的是___________ ;若改为加入过量 的浓溶液,是否可行?
的浓溶液,是否可行?___________ (填“可行”或“不可行”),原因是___________ 。
(3)在步骤⑤中加入少量无水 的目的是
的目的是___________ 。
(4)在步骤⑥中进行蒸馏,蒸馏至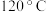 时除去的杂质是
时除去的杂质是___________ 。
(5)本实验中,山梨酸正丁酯的产率是___________ (精确至 )。
)。
(6)碳元素能形成许多物质,干冰 的晶胞结构如图所示,若该晶胞边长为
的晶胞结构如图所示,若该晶胞边长为 ,则干冰晶体的密度为
,则干冰晶体的密度为___________  。(已知:
。(已知:
 ,
, 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)

| 物质 | 相对分子质量 | 密度 | 沸点 | 水溶性 |
| 山梨酸 | 112 | 1.204 | 228 | 易溶 |
| 正丁醇 | 74 | 0.8089 | 117 | 溶 |
| 山梨酸正丁酯 | 168 | 0.926 | 195 | 难溶 |
| 乙醚 | 74 | 0.714 | 34.6 | 难溶 |

①在三颈烧瓶中加入
 山梨酸、
山梨酸、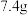 正丁醇、少量催化剂和几粒沸石,水浴加热三颈烧瓶,使反应体系保持微沸。
正丁醇、少量催化剂和几粒沸石,水浴加热三颈烧瓶,使反应体系保持微沸。②回流
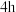 后,停止加热和搅拌,反应液冷却至室温。
后,停止加热和搅拌,反应液冷却至室温。③滤去催化剂和沸石,将滤液倒入
 水中,加入
水中,加入 乙醚,倒入分液漏斗中,分液。
乙醚,倒入分液漏斗中,分液。④分离出的有机层先用
 的
的 溶液洗涤至中性,再用水洗涤分液,收集有机层。
溶液洗涤至中性,再用水洗涤分液,收集有机层。⑤在有机层中加入少量无水
 ,静置片刻,过滤。
,静置片刻,过滤。⑥将滤液进行蒸馏,除去杂质得到
 山梨酸正丁酯。
山梨酸正丁酯。回答下列问题:
(1)仪器A的名称是
 ”或“n”)口通入。
”或“n”)口通入。(2)洗涤、分液过程中,加入
 溶液的目的是
溶液的目的是 的浓溶液,是否可行?
的浓溶液,是否可行?(3)在步骤⑤中加入少量无水
 的目的是
的目的是(4)在步骤⑥中进行蒸馏,蒸馏至
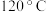 时除去的杂质是
时除去的杂质是(5)本实验中,山梨酸正丁酯的产率是
 )。
)。(6)碳元素能形成许多物质,干冰
 的晶胞结构如图所示,若该晶胞边长为
的晶胞结构如图所示,若该晶胞边长为 ,则干冰晶体的密度为
,则干冰晶体的密度为 。(已知:
。(已知:
 ,
, 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
您最近一年使用:0次
2024-05-08更新
|
166次组卷
|
2卷引用:甘肃省陇南市部分学校2023-2024学年高三下学期化学押题考试(三模)化学试题
10 . 氢能是一种绿色能源,工业上采用多种途径制备 。
。
Ⅰ.甲醇( )是潜在储氢材料。甲醇制氢的反应历程如下:
)是潜在储氢材料。甲醇制氢的反应历程如下: (g)分解制氢的热化学方程式:
(g)分解制氢的热化学方程式:_______ 。
(2)上述反应历程中,控速步骤的方程式为_______ 。
Ⅱ.天然气制备 。反应原理如下:
。反应原理如下:
反应1:

反应2:
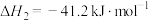
(3)工业制 中,将混合气体通入KOH溶液吸收
中,将混合气体通入KOH溶液吸收 ,便于提高
,便于提高 纯度和产率。
纯度和产率。

 ,宜选择的条件是_______(填字母)。
,宜选择的条件是_______(填字母)。
(4)研究表明, 的反应速率方程为
的反应速率方程为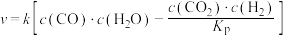 ,其中,
,其中, 为压强平衡常数,k为反应速率常数且随温度升高而增大。在气体组成和催化剂一定条件下,反应速率与温度关系如图2所示。温度高于
为压强平衡常数,k为反应速率常数且随温度升高而增大。在气体组成和催化剂一定条件下,反应速率与温度关系如图2所示。温度高于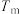 时,v逐渐减小的原因是
时,v逐渐减小的原因是_______ 。 (g)和
(g)和 (g)初始投料比一定,在某催化剂作用下发生反应1和2,经过相同时间测得如下数据(反应未达到平衡状态):
(g)初始投料比一定,在某催化剂作用下发生反应1和2,经过相同时间测得如下数据(反应未达到平衡状态):
已知: 的选择性
的选择性 。
。
数据表明,升高温度, 的转化率增大,而
的转化率增大,而 的选择性降低,可能的原因是
的选择性降低,可能的原因是_______ 。
(6)在1.0L恒容密闭容器中投入1mol (g)和1mol
(g)和1mol  (g)发生反应1和2,实验测得
(g)发生反应1和2,实验测得 平衡转化率与温度、压强关系如图3,540℃、
平衡转化率与温度、压强关系如图3,540℃、 下,Q点
下,Q点
_______  (填“>”“<”或“=”,下同)。
(填“>”“<”或“=”,下同)。
_______  。T点,CO选择性为80%,对应温度下反应1的化学平衡常数K为
。T点,CO选择性为80%,对应温度下反应1的化学平衡常数K为_______  (结果保留1位小数)。
(结果保留1位小数)。
 。
。Ⅰ.甲醇(
 )是潜在储氢材料。甲醇制氢的反应历程如下:
)是潜在储氢材料。甲醇制氢的反应历程如下:
 (g)分解制氢的热化学方程式:
(g)分解制氢的热化学方程式:(2)上述反应历程中,控速步骤的方程式为
Ⅱ.天然气制备
 。反应原理如下:
。反应原理如下:反应1:


反应2:

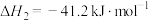
(3)工业制
 中,将混合气体通入KOH溶液吸收
中,将混合气体通入KOH溶液吸收 ,便于提高
,便于提高 纯度和产率。
纯度和产率。

 ,宜选择的条件是_______(填字母)。
,宜选择的条件是_______(填字母)。| A.高温、高压 | B.低温、低压 | C.低温、高压 | D.高温、低压 |
(4)研究表明,
 的反应速率方程为
的反应速率方程为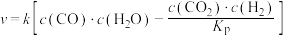 ,其中,
,其中, 为压强平衡常数,k为反应速率常数且随温度升高而增大。在气体组成和催化剂一定条件下,反应速率与温度关系如图2所示。温度高于
为压强平衡常数,k为反应速率常数且随温度升高而增大。在气体组成和催化剂一定条件下,反应速率与温度关系如图2所示。温度高于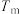 时,v逐渐减小的原因是
时,v逐渐减小的原因是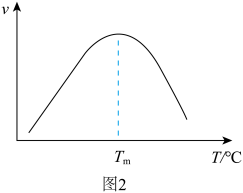
 (g)和
(g)和 (g)初始投料比一定,在某催化剂作用下发生反应1和2,经过相同时间测得如下数据(反应未达到平衡状态):
(g)初始投料比一定,在某催化剂作用下发生反应1和2,经过相同时间测得如下数据(反应未达到平衡状态):| T/K |  的转化率/% 的转化率/% |  的选择性/% 的选择性/% |
| 543 | 12.3 | 23.1 |
| 553 | 15.6 | 18.5 |
 的选择性
的选择性 。
。数据表明,升高温度,
 的转化率增大,而
的转化率增大,而 的选择性降低,可能的原因是
的选择性降低,可能的原因是(6)在1.0L恒容密闭容器中投入1mol
 (g)和1mol
(g)和1mol  (g)发生反应1和2,实验测得
(g)发生反应1和2,实验测得 平衡转化率与温度、压强关系如图3,540℃、
平衡转化率与温度、压强关系如图3,540℃、 下,Q点
下,Q点
 (填“>”“<”或“=”,下同)。
(填“>”“<”或“=”,下同)。
 。T点,CO选择性为80%,对应温度下反应1的化学平衡常数K为
。T点,CO选择性为80%,对应温度下反应1的化学平衡常数K为 (结果保留1位小数)。
(结果保留1位小数)。
您最近一年使用:0次
2024-05-06更新
|
76次组卷
|
3卷引用:甘肃省张掖市某校2023-2024学年高三下学期模拟考试化学试题