名校
解题方法
1 . 钠及其化合物有非常重要的用途。
(1)钠的化学性质非常活泼。画出钠的原子结构示意图________ 。
钠与水反应的实验过程如图①、②、③所示。
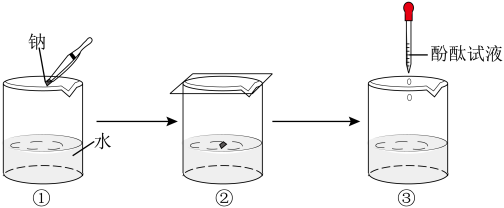
①将图②中的现象与解释用直线连接起来。_________
实验现象 解释
钠熔成小球 产生了气体
钠四处游动,嘶嘶作响 钠的密度比水小
钠浮在水面上 钠与水反应放热且钠的熔点低
②在③中酚酞变红,说明溶液呈_______ (填“酸”或“碱”或“中”)性。
③钠与水反应的化学方程式是_________ 。
(2)过氧化钠可在潜水艇中作为氧气的来源。写出过氧化钠与水反应的化学方程式___ ,与二氧化碳反应的化学方程式___ 。
(3)为探究Na2CO3和NaHCO3的热稳定性,某同学设计了如下实验:
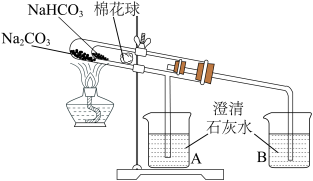
加热一段时间后,________ (填“A”或“B”)中澄清石灰水变浑浊,写出澄清石灰水变浑浊的离子方程式:________ 。写出试管中发生反应的化学方程式________ 。
(4)我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)。含有氮元素、钾元素、磷元素的某些盐可以作为化肥。
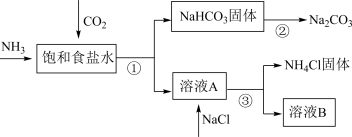
①联合制碱法所制得的“碱”是指_______ (填化学式)。
②在①-③所涉及的操作方法中,包含过滤的是_______ (填序号)。
③根据图,将化学方程式补充完整:NH3+CO2+___ +___ =NaHCO3↓+NH4Cl
④NaHCO3溶于水电离的方程式___ 。
⑤下列说法中,正确的是___ (填字母)
a.CO2可循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH4+、Cl-
(1)钠的化学性质非常活泼。画出钠的原子结构示意图
钠与水反应的实验过程如图①、②、③所示。

①将图②中的现象与解释用直线连接起来。
实验现象 解释
钠熔成小球 产生了气体
钠四处游动,嘶嘶作响 钠的密度比水小
钠浮在水面上 钠与水反应放热且钠的熔点低
②在③中酚酞变红,说明溶液呈
③钠与水反应的化学方程式是
(2)过氧化钠可在潜水艇中作为氧气的来源。写出过氧化钠与水反应的化学方程式
(3)为探究Na2CO3和NaHCO3的热稳定性,某同学设计了如下实验:

加热一段时间后,
(4)我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)。含有氮元素、钾元素、磷元素的某些盐可以作为化肥。

①联合制碱法所制得的“碱”是指
②在①-③所涉及的操作方法中,包含过滤的是
③根据图,将化学方程式补充完整:NH3+CO2+
④NaHCO3溶于水电离的方程式
⑤下列说法中,正确的是
a.CO2可循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH4+、Cl-
您最近一年使用:0次
解题方法
2 . 生活污水和某些工业废水中的含氮化合物经转化最终会以硝酸盐的形式进入水体,若大量排放会造成水体富营养化。用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。Fe还原水体中NO3-的反应原理如右图所示。______ (填字母)。
a.加剧水资源短缺 b.危害人体健康
(2)NO3-中氮元素的化合价为______ 。
(3)Fe在反应过程中发生的是______ (选填“氧化”或“还原”)反应。
(4)将足量铁粉投入某水体样本中,经一段时间后,测得溶液中离子浓度的有关数据如下(其他离子忽略不计)。
表中y =______ 。

a.加剧水资源短缺 b.危害人体健康
(2)NO3-中氮元素的化合价为
(3)Fe在反应过程中发生的是
(4)将足量铁粉投入某水体样本中,经一段时间后,测得溶液中离子浓度的有关数据如下(其他离子忽略不计)。
离子 | Na+ | H+ | NO3− | NH4+ | Fe2+ |
浓度/(mol·L−1) | 5.0×10−2 | 5.0×10−2 | 6.4×10−1 | y | 2.4×10−1 |
您最近一年使用:0次



